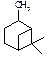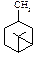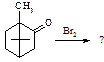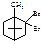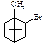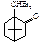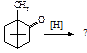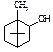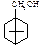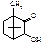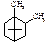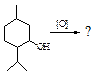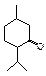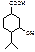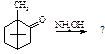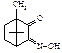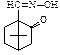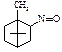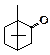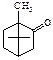Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Розділ 25. Нуклеїнові кислоти. ТестиСодержание книги
Поиск на нашем сайте
1. Структурними компонентами нуклеїнових кислот є: A. * рибоза [дезоксирибоза], азотисті основи, фосфорна кислота B. α, L-амінокислоти C. α, D-амінокислоти D. рибоза [дезоксирибоза], гідроксипурини, фосфорна кислота E. дезоксиглюкоза [глюкоза], пуринові і піримідинові основи, фосфорна кислота
2. У нуклеїнових кислотах піримідинова або пуринова основа зв’язана з залишком A.*рибози B. арабінози C. глюкози D. фруктози E. ксилози
3. Яке з похідних пурину входить до складу нуклеїнових кислот? A.* Аденін B. Ксантин C. Гіпоксантин D. Кофеїн E. Теобромін
4. АТФ у багатьох біохімічних процесах виступає як «депо» енергії. При розщепленні яких зв’язків в молекулі АТФ вивільняється ця енергія? A.* Макроергічних зв’язків B. Ангідридних зв’язків C. N-глікозидних зв’язків D. Складно-ефірних зв’язків E. Водневих зв’язків
5. Аденін-Тимін, Гуанін-Цитозин – пари комплементарних основ, що забезпечують існування подвійної спіралі молекули ДНК. Вкажіть тип зв’язку, що утворюється між комплементарними основами: A. *Водневий звязок B. Ковалентний π-звязок C. Іонний звязок D. Ковалентний σ-звязок E. Семіполярний звязок
6. Яка із перерахованих сполук після взаємодії з нітритною кислотою буде комплементарною аденіну? А. *4-Аміно-2-гідрокси-5-метилпіримідин. В. 2-аміно-6-гідроксипурин С. 6-амінопурин D. 5-амінопіримідин E. 5-аміно-2-гідрокси-4-метилпіримідин
7. Вкажіть вид таутомерії, притаманний для піримідинових основ – тиміну, урацилу, цитозину: A. * лактим-лактамна B. нітро-аци-нітро C. кето-енольна D. тіон-тіольна E. азольна
Розділ 26. Неомилювані ліпіди Терпени 1. До терпенових вуглеводів відносяться ненасичені вуглеводні складу (С5Н8)n. З яких фрагментів складаються молекули терпенів? A. * Ізопрену B. Хлоропрену C. Бутадієну D. Метилізопрену E. Диметилізопрену
2. Терпени є одним з класів органічних сполук. З яких фрагментів побудовані молекули терпенів? A. * Ізопрену B. Хлорпрену C. Бутадієну D. Метилізопрену E. Диметилізопрену
3. Терпенові вуглеводи є ненасиченими органічними сполуками. Яку кількість ізопренових фрагментів містять монотерпени? A. * два B. Три C. Чотири D. П’ять E. Вісім
4. Терпени є ненасиченими кисневмісними органічними сполуками, які класифікують в залежності від кількості фрагментів. Яке число монофрагментів містять монотерпени? A. * два B. Три C. Чотири D. П’ять E. Вісім
5. Терпени відносяться до неомилюваних ліпідів і включають терпенові вуглеводні і терпеноїди. Терпеноїди це: A. *Кисневмісні похідні терпенових вуглеводнів B. Азотвмісні похідні терпенових вуглеводнів C. Фосфорвмісні похідні терпенових вуглеводнів D. Сірковмісні похідні терпенових вуглеводнів E. Кремнійвмісні похідні терпенових вуглеводнів
Хімічні властивості 6. З наведених структурних формул виберіть ту, яка відповідає камфорі: A.* B. C. D.
7. Вкажіть продукт реакції бромування камфори
A.* B. C. D. E.
8. Вкажіть продукт відновлення камфори:
A.* B. C. D. 9. Вкажіть механізм реакції одержання бромкамфори із камфори A. *Радикальне заміщення B. Електрофільне приєднання C. Нуклеофільне заміщення D. Електрофільне заміщення E. Нуклеофільне приєднання
10. При окислені ментолу дихроматом калію в сірчаній кислоті (хромова суміш) утворюється:
A.* B. C. D. E.
11. Вітаміни - це аміни життя. Крім вітамінів існують речовини провітаміни, які утворюють вітаміни. Повітаміном якого вітаміну є β-каротин? A. * А1 B. В1 C. В12 D. С E. Д
12. Холестерин входить до складу клітинних мембран, особливо нервових. За будовою є спиртом. До яких спиртів його можна віднести? A. * Ненасичених гетероциклічного ряду B. Ненасичених ароматичного ряду C. Насичених аліфатичного ряду D. Насичених ароматичного ряду E. Ненасичених аліфатичного ряду
Ідентифікація 13. Вкажіть продукт реакції камфори з гідроксиламіном:
A.* B. C. D. E.
14. Камфора відноситься до біциклічних терпенів
Вкажіть реагент за допомогою якого можна підтвердити наявність кетонної групи в молекулі камфори: А. *C6H5NHNH2 В. [Ag(NH3)2]OH С. бромна вода D. розчин KMnO4 E. HNO3 15. Вкажіть реагент, який підтверджує наявність в складі камфори кето-групи:
A. *Фенілгідразин B. Амоніачний розчин аргентум оксиду C. Бромна вода D. Розчин перманганату калію E. Нітратна кислота
16. Камфора – представник біциклічних моно терпенів. В яку із перерахованих нижче реакцій камфора не буде вступати? A. *Реакція естерифікації B. Відновлення до відповідного спирту. C. Взаємодія з гідроксил аміном. D. Бромування E. Приєднання ціанідної кислоти. Стероїди
17. Тестостерон – представник чоловічих статевих гормонів. Який вуглеводень лежить в основі тестостерону? A. *Андростан B. Естран C. Холан D. Прегнан E. Холестан
18. Із перерахованих назв насичених вуглеводнів виберіть ті, що входять до складу жіночих статевих гормонів? A.* Естран B. Андростан C. Стеран D. Холан E. Холестан
Аналітична хімія Зміст
ЗАГАЛЬНІ ТЕОРЕТИЧНІ ПИТАННЯ 1. Чим характеризується міра здатності реагенту давати добре фіксований аналітичний ефект при взаємодії з шуканою речовиною? A. * Чутливістю реакції B. Вибірністю реакції C. Специфічністю реакції D. Розбавленням E. Причини, які подані в пунктах А і В
2. Що є мірою специфічності аналітичних реакцій? A. * Граничне співвідношення концентрацій іонів як тих, що визначаються, так і сторонніх B. Гранична концентрація іона, який визначається C. Граничні співвідношення концентрацій сторонніх іонів D. Чутливість аналітичних реакції E. Концентрація сторонніх іонів
3. Як називаються реакції і реагенти, що дають можливість визначити даний іон у присутності інших іонів? A. * Специфічними B. Вибірковими C. Груповими D. Характерними E. Причини, які подані в пунктах В і D
4. При проведенні контролю якості лікарських засобів застосовуються аналітичні реакції. Хімічна реакція може бути використана як аналітична у тому випадку, коли вона: A. * Проходить із видимими змінами у реакційній системі. B. Проходить з виділенням тепла. C. Відбувається із утворенням гетерофази. D. Є оборотною E. Проходить повільно
5. Виявлення досліджуваних іонів за допомогою дробного методу аналізу вимагає виконання наступних аналітичних операцій: A. * Використання специфічного реактиву. B. Концентрування досліджуваного розчину C. Застосування групового реактиву. D. Застосування високочутливого реактиву. E. Застосування маскуючого реактиву.
6. Характеристикою термодинамічного стану системи осад–насичений розчин є: A. * Добуток розчинності B. Іонний добуток C. Константа стійкості D. Іонна силу розчину E. Константа дисоціації
7. Напрямок проходження оксидаційно-відновної реакції визначається: A. * Різницею стандартних електродних потенціалів учасників реакції B. Величиною стандартних електродних потенціалів учасників реакції C. Величиною стрибка потенціалу в ході оксидаційно-відновної реакції D. Величиною водневого показника системи E. Температурою системи
8. В аналізі та при виробництві ліків широко застосовується рівноважна екстракція. Кількісною характеристикою процесу екстракції є: A. * Константа розподілу B. Константа дисоціації C. Константа солюбілізації D. Константа гідролізу E. Константа стійкості
9. Згідно теорії електролітичної дисоціації усі електроліти поділяються на сильні та слабкі. Слабким електролітом називається хімічна сполука, яка має: A. * Малу константу іонізації B. Низький ступінь окислення C. Малу величину константи нестійкості D. Низьке значення оптичної густини E. Незначний добуток розчинності
10. Поділ іонів (катіонів/аніонів) на аналітичні групи проводиться відповідно до: A. * Хімічних властивостей їх сполук із певними реактивами D. Положення елементів у періодичній системі C.Розчинності їх сполук у воді D.Оксидаційно-відновних властивостей цих іонів E.Фізичних властивостей їх сполук
11. Як називається прийом зв’язування іонів як тих, що визначаються, так і сторонніх? A.*Аналітичним «маскуванням» B.Дробним порядком аналізу C. Систематичним порядком аналізу D. Підвищенням чутливості E. Підвищенням вибірковості
12. Яким є процес дисоціації потужного електроліту і чи можна до нього застосувати закон дії мас? A. * Зворотним, і до нього можна застосувати закон дії мас B. Незворотним і до нього не можна застосувати закон дії мас C. Зворотним, і до нього не можна застосувати закон дії мас D. Незворотним, і до нього можна застосувати закон дії мас E. Не можна застосувати закон дії мас
13. Як називається співвідношення активної концентрації іонів до їх загальної аналітичної концентрації? A. * Коефіцієнтом активності B. Активністю C. Іонною силою розчину D. Константою дисоціації E. Ступеню дисоціації
14. Розчин яких із наведених сумішей не є буферним? A. * NaOH+NaCI B. CH3COOH+CH3COONa C. NH4CI+NH3·H2O D. Na2CO3+NaHCO3 E. NaH2PO4+Na2HPO4
15. Як перебігає процес дисоціації комплексних іонів? A. * Зворотно, за типом слабких електролітів B. Зворотно, за типом сильних електролітів C. Необоротно, за типом слабких електролітів D. Необоротно, за типом сильних електролітів E. Дисоціює, за типом слабких та сильних електролітів
16. Чому при аналізі суміші катіонів в першу чергу виявляють іони NH4+, Fe2+, Fe3+? A. * Іони амонію заважають виявленню іонів К+, а на іони Fe2+ i Fe3+ є специфічні реакції B. Іони амонію можуть сприяти помилці у виявленні іонів калію, а іони Fe2+ i Fe3+ додаються в ході аналізу C. Іони амонію вносяться в подальшому ході аналізу суміші, а на іони Fe2+ i Fe3+ є специфічні реакції D. Іони амонію заважають виявленню іонів К+ і вносяться в подальшому аналізі, іони Fe2+ будуть окисненні у Fe3+, на іони Fe3+ є специфічна реакція E. Іони амонію заважають виявленню іонів калію і вносяться в ході аналізу, іони Fe2+ в подальшому окиснюються, а іони Fe3+ необхідні для кращого осадження фосфатів
17. В аналізі широко застосовують буферні розчини для: A. * Підтримування сталим певного значення рН середовища B. Забарвлення розчинів C. Утворення комплексних сполук D. Досягнення повноти осадження аналітичної групи катіонів E. Зміни рН середовища
18. В дробовому ході аналізу іони різних аналітичних груп виявляють: A. * В окремих порціях розчину в будь-якій послідовності B. При строгій послідовності операцій з виявлення C. Після розділення іонів на аналітичні групи
19. На розчинність важкорозчинних солей, утворених катіонами металів, які легко утворюють аміакати найбільший вплив має: A. * Концентрація молекул аміаку B. Концентрація іонів амонію C. Концентрація амінів D. Концентрація іонів гідрогену E. Концентрація амідів
20. Розчинники, які використовують в аналітичній хімії, класифікують за їх здатністю приєднувати або відщеплювати протони. Вкажіть, до яких розчинників відносяться спирти: A. * Амфіпротні B. Протогенні C. Протофільні D. Апротонні E. Протогені і амфіпротні
21. Аналіз невідомої суміші слід починати з A. * Виявлення катіонів B. Виявлення аніонів мінеральних кислот C. Виявлення аніонів органічних кислот D. Виявлення осадів E. Вимірювання маси
22. Деякі окислювально–відновні реакції супроводжуються перебігом побічних індукованих (спряжених) реакцій, в якіх одна реакція перебігає самодовільно, а друга тільки при проходженні першої. Яку назву має речовина, яка приймає участь в обох реакціях? A. * Актор B. Індуктор C. Акцептор D. Каталізатор E. Індикатор
23.Чутливість аналітичних реакцій визначає можливість виявлення речовин у розчині.Чутливість реакції характеризують усі перелічені нижче величини крім: A. * Мінімальний об’єм реагенту B. Гранична концентрація C. Граничне розведення D. Границя виявлення E. Мінімальний об’єм
24. При порівнянні двох методик аналізу за відтворюваністю викорисовують: A. * Критерій Фішера B. Коефіцієнт Стьюдента C. Число Фарадея D. Число Авогадро E. Критерій Бартлета
25. Для підтримання сталого pH у розчинах досліджуваних сполук застосовують буферні суміші. Яка за наведених сумішей є буферною? A. * NH4Cl + NH4OH B. HCl + NaOH. C. NH4Cl +HCl. D. NaCl+NaOH. E. H2SO4 + CH3COOH.
26. Для ідентифікації компонентів в суміші, застосовують хімічні аналітичні реакції. Яким вимогам вони повинні відповідати? A. * Бути специфічними, характерними, чутливими B. Бути широкого спектру дії C. Бути селективними D. Проходити повільно E. Бути незворотними
27. В аналізі часто застосовують водні розчини солей, що гідролізують і викликають зміну рН середовища. Яке рН середовища у водному розчині натрію карбонату? A. * Слаболужне B. Кисле C. Сильнолужне D. Нейтральне E. Слабокисле
28. Вказані препарати можуть використовуватися для корекції кислотно-основної та іонної рівноваги. При однаковій молярній концентрації максимальною величиною іонної сили характеризується розчин: А. * Кальцію хлориду В. Калію йодиду С. Калію хлориду Д. Натрію фториду Е. Натрію йодиду ЯКІСНИЙ АНАЛІЗ
Катіони Катіони 1 аналітичної групи
1. Який аналітичний ефект спостерігається під час визначення катіону калію розчином натрій гексанітрокобальтату (ІІІ)? А. * Жовтий осад В. Білий осад С. Жовте забарвлення розчину D. Чорний осад Е. Червоний осад
2. На аналіз поступила безбарвна кристалічна речовина, яка добре розчинна у воді. При проведенні проб з груповими реагентами (2н HCl, 2н H2SO4, 2н NaOH, концентрованим NH4OH) всі реакції дали негативний результат. Проба з реактивом Неслера також дала негативний результат. При додаванні до розчину гексанітрокобальтату (ІІІ) натрію утворився жовтий кристалічний осад, що свідчить про наявність в розчині: A. * Катіонів калію B. Катіонів амонію C. Катіонів натрію D. Катіонів літію E. Катіонів магнію
3. Для зв'язування іонів водню при ідентифікації іонів калію з винною кислотою використовують розчин: А. * Ацетату натрію В. Гідроксиду натрію С. Аміаку D. Сірчаної кислоти Е. Соляної кислоти
4. Яка пара йонів не заважає один одному при виявленні? А. * K+, Na+ В. NH4+, K+ С. NH4+, Na+ D. Li+, NH4+ Е. Такої пари для І аналітичної групи немає
5. Який катіон знаходиться в розчині, якщо при нагріванні з лугом виділяється газ з різким запахом: А.*Амонію В. Свинцю (ІІ) С. Ртуті (І) D. Срібла E. Ртуті (ІІ)
6. В лабораторії необхідно ідентифікувати катіон амонію. Можна використати розчин: A. * Реактиву Несслера B. Калію хромату C. Цинку уранілацетату D. Реактиву Чугаєва E. Натрію сульфату
7. Яка із вказаних реакцій визначення катіонів амонію є специфічною? A. * Реакція з гідроксидами лужних металів при нагріванні B. Реакція з калію гексагідроксоантимонатом C. Реакція з натрію гексанітрокобальтом(Ш) D. Реакція з калію тетрайодогідраргіратом (П) в лужному середовищі E. Реакція з натрію гексанітрокобальтом(Ш) в кислому середовищі
8. При проведенні аналізу сумішей катіонів за систематичним ходом необхідно відділити катіони першої аналітичної групи. Груповим реактивом для іонів першої аналітичної групи є: A. * Жоден з цих реактивів B. Гідроксид натрію C. Гідроксид амонію D. Хлоридна кислота E. Сульфатна кислота
9. Аналізуючий розчин містить катіони калію і натрію. Вкажіть реагент, який дозволяє виявити в цій суміші катіони калію: A. * Кислота винна B. Кислота щавелева C. Кислота оцтова D. Кислота бензойна
10. При дії на аналізований розчин лугом при нагріванні виділяється газ, що змінює забарвлення червоного вологого лакмусового паперу на синє. Це свідчить про присутність в розчині: A. * Іонів амонія B. Карбонат-іонів C. Іонів свинцю D. Іонів вісмуту
11. Досліджуваний розчин містить катіони амонію і натрію. Вкажіть реагент, який дозволяє виявити в цьому розчині катіони натрію. A. * Цинкуранілацетат B. Калію гексагідроксостібат C. Реактив Несслера D. Кислота винна E. Кислота бензойна
12. В фармакопейному аналізі для ідентифікації іонів натрію використовують реакцію з: A. * 2-метоксі-2-фенілоцетовою кислотою B. 8-оксихіноліном C. Дифеніламіном D. Діацетилдіоксимом E. Тетрафенілборатом
13. Який висновок про склад досліджуваного розчину можна зробити, виходячи з того факту, що він не утворює осадів ні з: 1) HCl; 2) H2S; 3) (NH4)2S; 4) (NH4)2CO3 A. * Солі Натрію і Алюмінію B. Солі Калію і Плюмбуму C. Солі Магнію і Кальцію D. Солі Літію і Натрію E. Солі Літію і Стронцію
14. Яким аналітичним ефектом супроводжується реакція виявлення калію реагентом гідротартратом натрію? A. * Утворюється білий кристалічний осад B. Розчин набуває жовтого забарвлення C. Утворюється білий аморфний осад D. Випадає бурий осад E. Випадає жовтий осад
15. Яка з названих реакцій виявлення катіону амонію є надчутливою? A. * Реакція з лугом під час нагрівання у газовій камері B. Реакція з дигідроантимонатом калію C. Реакція з гексанітрокобальтом [ІІІ] натрію D. Реакція з тетрайодомеркуратом [ІІ] калію у лужному середовищі E. Реакція з гексанітрокобальтом [ІІІ] натрію у кислому середовищі
16. Розчин натрію дигідрофосфату є: A. * Розчином двоосновної кислоти. B. Розчином амфоліту C. Розчином середньої солі D. Насиченим розчином малорозчинної сполуки E. Розчином суміші солей (дигідрофосфату і гідрофосфату)
17. В якому розчині присутні катіони лише I аналітичної групи? A. * Na+, K+, NH4+ B. Na+, Fe2+, Fe3+ C. NH4+, Cu2+, Hg22+ D. K+, Ag+, Al3+ E. K+, NH4+, Zn2+
18. Чому І аналітична група катіонів не має групового реагенту? A. * Більшість сполук катіонів I групи добре розчинні B. Більшість розчинів солей безбарвні C. Катіони I групи забарвлюють полум’я пальника D. Катіони I групи слабкі комплексоутворювачі E. Солі слабких кислот цих катіонів піддаються гідролізу
19. Досліджуваний розчин містить катіони калію і амонію. Вкажіть реагент, який дозволяє виявити в цьому розчині катіони амонію. A. * Калію тетрайодомеркурат (ІІ) B. Натрію гідротартрат. C. Натрію ацетат D. Калію гексаціаноферат(ІІ) E. Цинкуранілацетат. 20. Для виявлення катіону амонію до проби додали реактив калію тетрайодомеркурату (ІІ). Якого кольору утвориться осад при наявності катіону амонію? A. * Цегляно-червоного. B. Білого. C. Чорного. D. Жовтого. E. Коричневого
21. Запропонуйте послідовний ряд реагентів для визначення калій - та ацетат - іонів у фармпрепараті: A. * Натрій гідрогентартрат, сульфатна кислота B. Натрій гексанітрокобальтат (11), амоній хлорид C. Натрій тетрафенілборат, натрій йодид D. Реактив Неслера, сульфатна кислота E. Натрій карбонат, хлоридна кислота
22. Сухий залишок, одержаний після випарювання розчину, що аналізується, забарвлює безбарвне полум’я пальника в жовтий колір, а при розгляді через синє скло – у фіолетовий.Які катіони знаходились в сухому залишку? A. * Na+, K+ B. Ca2+, K+ C. Na+, Sr2+ D. Li+, Ba2+ E. Na+, Ca2+
23. Необхідно провести ідентифікацію суміші, що містить катіони І аналітичної групи (Li+, Na+, K+, NH4 +). Який з цих катіонів виявляють реактивом Неслера? А. * Амоній В. Натрій С. Літій Д. Калій Е. Усі зазначені катіони
24. Провізор-аналітик проводить ідентифікацію калію ацетату. За допомогою якого реактиву він підтверджує наявність калію в досліджуваній речовині? А. * Розчин тартратної кислоти В. Розчин калію перманганату С. Розчин заліза (ІІІ) хлориду Д. Розчин натрію гідроксиду Е. Розчин форміатної кислоти
Катіони ІІ аналітичної групи
1. На чому ґрунтується розділення аргентум хлориду від гідраргірум (І) хлориду: А. * На різній розчинності у розчині амоніаку В. На різній розчинності у соляній кислоті С. На різній розчинності у лугах D. На різній розчинності у гарячій воді Е. На різній розчинності у сірчаній кислоті
2. На чому ґрунтується відокремлення плюмбум (ІІ) хлориду від інших хлоридів ІІ аналітичної групи: А. * На різній розчинності у гарячій воді В. На різній розчинності у соляній кислоті С. На різній розчинності у лугах D. На різній розчинності у розчині аміаку Е. На різній розчинності у сірчаній кислоті
3. До розчину, який містить катіони ІІ аналітичної групи (за кислотно-основною класифікацією) додали невелику кількість концентрованого розчину амоніаку і 3-4 краплі розчину формальдегіду. Пробірку занурили у гарячу воду і на стінках пробірки з’явилась дзеркальна плівка. Наявність якого катіону обумовлює цю реакцію? A. * Катіон арґентуму B. Катіон гідраргіруму (І) C. Катіон плюмбуму D. Катіон барію E. Катіон літію
4. При аналізі фармпрепарату необхідно розділити суміш хлоридів катіонів 2 аналітичної групи (аргентум (+1) та меркурій (+1)). Запропонуйте розчин реагенту для такого розділення: А. * Амоніаку В. Хлоридної кислоти С. Сульфатної кислоти D. Калій гідроксиду Е. Калій карбонату
5. При додавання розведенного розчину хлорводневої кислоти до розчину, що аналізується, утворився білий сирнистий осад. Про присутність яких іонів це свідчить? А. * Аргентум В. Ферум (ІІ) С. Барій D. Амоній Е. Йод
6. Для визначення якісного складу препарату на зразок досліджуваного розчину подіяли 2 Н розчином HCl. Випав білий осад, розчинний в водному розчині аміаку. На наявність яких катіонів вказує цей аналітичний ефект: A. * Аргентуму (І) B. Плюмбуму (ІІ) C. Меркурію (І) D. Меркурію (ІІ)
7. До досліджуваного розчину додали 2М розчин HCl. При цьому утворився білий осад, який при обробці розчином аміаку почорнів. Який катіон присутній у розчині: A. * Hg22+ B. Ag+ C. Pb2+ D. Ba2+ 8. До розчину, якій містить катіони меркурію(I), додали розчин хлоридної кислоти. До утвореного осаду додали розчин аміаку. Вкажіть хімічний склад осаду: A. * [HgNH2]Cl+Hg; B. Hg2O; C. [HgNH2]Cl; D. Hg(OH)2; 9. Відомо, що до складу досліджуваної суміші входять катіони другої аналітичної групи. До другої аналітичної групи належать катіони, які утворюють: A. * Осади із хлоридною кислотою B. Осади із нітратною кислотою C. Осади із гідрофосфатом натрію D. Осади із нітратом натрію
10. До досліджуваного розчину додали розчин калію йодиду. Випав золотисто-жовтий осад, який розчиняється в гарячій воді, надлишку реагенту і в оцтовій кислоті. Це свідчить про присутність в розчині: A. * Катіонів свинцю (ІІ) B. Катіонів срібла (І) C. Катіонів вісмуту (ІІІ) D. Катіонів ртуті (ІІ) E. Катіонів ртуті (І) 11. До досліджуваного розчину додали 1М розчин сірчаної кислоти. Випав осад білого кольору, який розчиняється в лугах. Це свідчить про присутність в розчині: A. * Катіонів свинцю (ІІ) B. Катіонів кальцію (ІІ) C. Катіонів барію (ІІ) D. Катіонів срібла (І) E. Катіонів ртуті (І) 12. За кислотно-основною класифікацією катіонів груповими реагентами можуть бути: HCl, H2SO4, NaOH або KOH, розчин NH3. До другої групи катіонів належать катіони Pb2+, Ag+, Hg22+. Вказати груповий реагент для другої групи катіонів. A. * Розчин HCl B. Розчин H2SO4 C. Група не має групового реагенту D. Розчин NaOH E. Розчин NH3 13. Реакція утворення золотисто-жовтого осаду (реакція «золотого дощу») - це реакція: A. * Утворення осаду PbІ2 B. Утворення осаду PbCl2 C. Утворення осаду AgІ D. Утворення осаду HgІ2 E. Утворення осаду Hg2І2 14. В якісному аналізі характерною реакцією на катіони срібла є: A. * Реакція утворення сирнистого осаду AgCl, що розчиняється в розчині аміаку, який знову утворюється при додаванні НNО3. B. Реакція "золотого дощу" C. Реакція утворення червоного розчину роданіду заліза D. Реакція утворення турнбулевої сині E. Реакція утворення берлінської лазурі 15. Користуючись таблицею добутку розчинності, визначте, яким із реагентів можна повніше осадити іони срібла із розчину нітрату срібла? A. * Сульфідом натрію B. Хроматом натрію C. Оксалатом амонію D. Сульфітом натрію E. Сульфатом натрію 16. За якою реакцією можна визначити форміатну кислоту: A. * З [Ag(NH3)2]OH; B. З Br2; C. З розчином KMnO4; D. З розчином FeCl3; E. З NaOH. 17. Які катіони містилися в розчині, якщо при додаванні до нього хлорводневої кислоти утворюється осад, після обробки якого розчином аміаку, відбувається часткове розчинення і почорніння нерозчинного осаду? A. * Срібло і ртуті(I) B. Срібла і барію C. Срібла і свинцю D. Срібло і ртуть(П) E. Ртуть(П) і ртуть(I) 18. На розчин, одержаний після обробки осаду хлоридів катіонів II групи гарячою водою, подіяли розчином калію дихромату. Утворився жовтий осад, нерозчинний в оцетовій кислоті, але розчинний в лужному середовищі. Які катіони містив досліджуваний розчин? A. * Свинцю (ІІ) B. Ртуть (ІІ) C. Барію D. Срібло (І) E. Кальцію 19. Які катіони I-III аналітичних груп знаходяться в досліджуваному розчині, якщо з розчином лугу утворюється осад, розчинний в надлишку лугу? A. * Свинцю (ІІ) B. Ртуть(I) C. Барію D. Срібло (І) E. Кальцію 20. При виконанні систематичного ходу аналізу по кислотно-основному методу для відділення свинцю (II) сульфату від сульфатів катіонів III групи осад обробляють розчином: A. * 30%-го амонія ацетату B. Амонія оксалата C. Амонія карбонату D. Натрію тіосульфату E. Натрію фториду 21. При аналізі суміші катіонів (Сa2+, Ba2+, Pb2+) ці іони осадили сульфатною кислотою. Як можна відокремити домішку PbSO4 від суміші сульфатів барію та кальцію? A. * Промиванням осаду розчином лугу. B. Перекристалізацією осаду. C. Промиванням осаду концентрованою H2SO4. D. Промиванням осаду розчином ацетатної кислоти. E. Промиванням осаду розчином аміаку.
22. До другої групи катіонів належать катіони Pb2+, Ag+, Hg22+. Вказати груповий реагент для другої групи катіонів. A. * Розчин HCl B. Розчин H2SO4 C. Група не має групового реагенту D. Розчин NaOH E. Розчин NH3
23. При визначенні одного з катіонів ІІ аналітичної групи використовують реакцію «золотого дощу». Продуктом цієї реакції є: A. * Утворення осаду PbІ2 B. Утворення осаду PbCl2 C. Утворення осаду AgІ D. Утворення осаду HgІ2 E. Утворення осаду Hg2І2
24. Виберіть реагент, що дозволяє відділити осад BaSO4 від осаду PbSO4: A. * NH4CH3COO B. NH4Cl C. Na2CO3 D. (NH4)2CO3 E. KHCO3
25. При додаванні до досліджуваного розчину лугу випав чорний осад, а при нагріванні утворився газ з різким запахом. Вкажіть яка пара катіонів знаходиться в розчині: A. * Ртуті(I) і амонію B. Натрію і амонію C. Ртуті(I) и ртуті(II) D. Калію і амонію E. Свинцю і амонію
26. Укажіть, який реагент використовують для відокремлення осаду AgCl вiд AgI? A. * Водний розчин аміаку B. Концентрована нітратна кислота C. Розведена нітратна кислота D. Концентрований розчин калію хлориду E. Розчин сульфатної кислоти
27. Досліджуваний розчин утворив з розчином нітрату срібла білий сирнистий осад, розчинний в розчині аміаку. Вкажіть склад отриманого осаду. A. * Срібла хлорид B. Срібла бромід C. Срібла йодид D. Срібла роданід E. Срібла сульфід
28. При дії групового реагенту на катіони ІІ аналітичної групи утворюється осад PbCl2,який розчиняється у: А. * Гарячій воді В. 0,2М розчин натрію карбонату С. 2М розчині сульфатної кислоти Д. Етанолі Е. Насиченому розчині натрію карбонату
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-06-22; просмотров: 531; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.147 (0.012 с.) |