
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кинетическая классификация реакций.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Химические реакции можно классифицировать по числу молекул, участвующих в каждом элементарном химическом акте. Мономолекулярными (одномолекулярными) называются реакции, в которых такой акт представляет собой химическое превращение одной молекулы (изомеризация, диссоциация и пр.). Бимолекулярные (двухмолекулярные такие, элементарный акт которых осуществляется при столкновении двух молекул (различных или одинаковых). В тримолекулярных (трёхмолекулярных) реакциях элементарный акт осуществляется при столкновении трёх молекул. Экспериментальное изучение кинетики той или иной реакции только в исключительных случаях позволяет отнести её к одной из указанных групп. Это удаётся сделать только для простых реакций, протекающих в одну стадию, уравнение которой совпадает со стехиометрическим уравнением реакции в целом (например, разложение NO2 и некоторые др.). Большинство химических реакций является совокупностью нескольких последовательных (или параллельных) элементарных реакций, каждая из которых может принадлежать к любой из кинетических групп. В простейшем случае, если одна из элементарных реакций протекает значительно медленнее остальных, наблюдаемый кинетический закон будет соответствовать именно этой реакции. Если же скорости отдельных стадий сравнимы, кинетика может быть ещё больше осложнена. Поэтому для характеристики кинетики реальных процессов вводится понятие порядкареакции, отличное от понятия молекулярности. Порядок химической реакции по данному веществу это число, равное степени- ni, в которой концентрация этого вещества входит в кинетическое уравнение реакции. Сумма показателей степеней n1 + n2 + n3¼+ ni определяет порядок реакции в целом. Вследствие сложности большинства химических процессов порядок реакции обычно не совпадает с ее молекулярностью и не соответствует стехиометрическому уравнению. Элементарный механизм отдельных стадий сложного процесса-порядок реакции характеризует формально-кинетическую зависимость скорости реакции от концентрации реагирующих веществ, а молекулярность. Реакции разделяют также по природе частиц, участвующих в элементарном акте реакции. Реакции, в которых участвуют молекулы, называют молекулярными. Реакции с участием атомов или свободных радикалов называются цепными. Реакции с участием ионов называются ионными. Реакции классифицируют по числу фаз, участвующих в реакции. Реакции, протекающие в одной фазе, называются гомогенными. Реакции, протекающие на границе раздела фаз, называются гетерогенными. Можно классифицировать реакции по степени сложности. В этом плане можно выделить двусторонние и односторонние (обратимые и необратимые), изолированные (реакции, в ходе которых образуется продукт только одного типа) и параллельные, сопряженные, последовательные (консекутивные) -реакции. Теоретическое изучение этих реакций основывается на том, что при протекании в системе одновременно нескольких реакций каждая из них идет независимо от других и подчиняется закону действия масс принцип независимого протекания реакций. 5. Влияние температуры на скорость реакции: температурный коэффициент, энергия активации. Правило Вант-Гоффа — эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °C до 100 °C).Я. Х. Вант-Гофф на основании множества экспериментов сформулировал следующее правило: При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза. Уравнение, которое описывает это правило следующее: С.Аррениус рассчитал долю активных (т.е. приводящих к реакции) соударений реагирующих частиц a, зависящую от температуры: - a = exp(-E/RT). и вывел уравнение Аррениуса для константы скорости реакции: k = koe-E/RT, где ko и E d зависят от природы реагентов. Е - это энергия, которую надо придать молекулам, чтобы они вступили во взаимодействие, называемая энергией активации.
|
||||
|
Последнее изменение этой страницы: 2016-04-21; просмотров: 687; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.189.192.214 (0.007 с.) |

 , где
, где  — скорость реакции при температуре
— скорость реакции при температуре 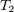 ,
,  — скорость реакции при температуре
— скорость реакции при температуре  ,
, 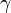 — температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов). Правило Вант-Гоффа применимо только для реакций с энергией активации 60-120 кДж/моль в температурном диапазоне 10-400oC. Правилу Вант-Гоффа также не подчиняются реакции, в которых принимают участие громоздкие молекулы, например белки в биологических системах. Из уравнения Вант-Гоффа температурный коэффициент вычисляется по формуле:
— температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов). Правило Вант-Гоффа применимо только для реакций с энергией активации 60-120 кДж/моль в температурном диапазоне 10-400oC. Правилу Вант-Гоффа также не подчиняются реакции, в которых принимают участие громоздкие молекулы, например белки в биологических системах. Из уравнения Вант-Гоффа температурный коэффициент вычисляется по формуле:  . Температурную зависимость скорости реакции более корректно описывает уравнение Аррениуса. К реакции приводит не каждое столкновение молекул реагентов, а только наиболее сильные столкновения. Лишь молекулы, обладающие избытком кинетической энергии, способны к химической реакции.
. Температурную зависимость скорости реакции более корректно описывает уравнение Аррениуса. К реакции приводит не каждое столкновение молекул реагентов, а только наиболее сильные столкновения. Лишь молекулы, обладающие избытком кинетической энергии, способны к химической реакции.


