Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кислота хлористоводородная (HCl)Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
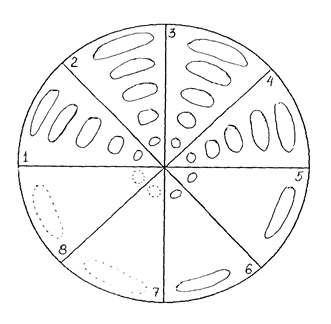
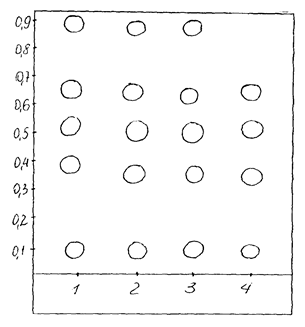
подлинность: определение рН (проба на H+) реакция с серебра нитратом (проба на Cl–); количественное определение: субстанция – кислотно-основное титрование; дилюции до Х3 – кислотно-основное титрование; потенциометрическое титрование; кислота уксусная (CH3COOH) подлинность: определение рН (проба на H+) реакция со спиртом этиловым (проба на ацетат-ион); количественное определение: субстанция – кислотно-основное титрование; тритурации, дилюции до Х3 – кислотно-основное титрование; потенциометрическое титрование; прямая потенциометрия; железа сульфат (FeSO4 ·H2O) подлинность: реакция с калия гексацианоферратом (III) K3[Fe(CN)6] (проба на Fe2+); реакция с бария нитратом (проба на SO42–); количественное определение: субстанция – перманганометическое титрование; тритурации, дилюции до Х3 – аналогично; серебра нитрат (AgNO3) подлинность: реакция с хлористоводородной кислотой (проба на Ag+) количественное определение: субстанция – прямое тиоцианатометрическое титрование по Фольгарду; тритурации, дилюции до Х3 – прямое тиоцианатометрическое титрование по Фольгарду; прямая ионометрия; Железо металлическое (Fe) получение: восстановление водородом из железа (II) оксида; подлинность: растворение в серной кислоте и реакция на Fe2+ действием калия гексацианоферрата (III) K3[Fe(CN)6; количественное определение: субстанция – растворение в серной кислоте, затем перманганометрическое титрование; тритурации до Х3 – аналогично. Если препарат не является фармакопейным, то в качестве субстанций используют химические реактивы квалификации не менее «ч. д. а.». Их качество должно соответствовать ГОСТу на данный химический реактив и подтверждаться стандартными методиками. Для примера можно привести следующие препараты: цинк (Zn) марки «ч. д. а.» либо полученный электролизом раствора подлинность: растворение без остатка в хлористоводородной кислоте; количественное определение: субстанция – комплексонометрическое титрование; тритурации – комплексонометрическое титрование – до Х3; фотоколориметричеси с дитизоном – до Х5; Серебро (Ag) подлинность: растворение без остатка в азотной кислоте; субстанция – растворение в азотной кислоте, затем прямое тиоцианатометрическое титрование по Фольгарду; тритурации до Х3 – аналогично; свинец (Pb) подлинность: растворение без остатка в азотной кислоте; количественное определение: субстанция – растворение в азотной кислоте, затем комплексонометрическое титрование; тритурации до Х3 – аналогично; кислота азотная (HNO3) подлинность: определение рН (проба на H+) реакция с железа сульфатом и серной кислотой (проба на NO3–) или реакция с дифениламином (проба на NO3–); количественное определение: субстанция – кислотно-основное титрование; дилюции до Х3 – кислотно-основное титрование; потенциометрическое титрование; кислота серная (H2SO4) подлинность: определение рН (проба на H+) реакция с бария нитратом (проба на SO42–); количественное определение: субстанция – кислотно-основное титрование; дилюции до Х3 – кислотно-основное титрование; потенциометрическое титрование. В случае отсутствия соответствующих химических реактивов, субстанции получают особыми (специальными) методами. Например: кальциум карбоникум, кальция карбонат (CaCO3) получение: белоснежные внутренние чешуйчатые кусочки разбитых раковин превращают в мелкий порошок; подлинность: растворение в азотной кислоте и реакция с молибденовокислым аммонием (проба на Ca2+); количественное определение: субстанция, тритурации – не стандартизуются; алюмина, обожжённый глинозём (Al2O3) получение: из криолита или из раствора алюминиево-калиевых квасцов под действием аммиака; подлинность: щелочное плавление, затем реакция с ализарином (проба на Al3+); количественное определение: субстанция, тритурации – не стандартизуются; калия арсенит (KAsO2·HAsO2·H2O) получение: реакция мышьяковистого ангидрида с калия карбонатом; подлинность: реакция с сероводородом, реакция с серебра нитратом (пробы на AsO2–); количественное определение: субстанция – иодометрически; броматометрически; тритурации до Х3 – иодометрически; хлористое золото, тетрахлороаурат (III) водорода (H[AuCl4]·H2O) получение: растворение золота в царской водке (смеси хлороводородной и азотной кислот); подлинность: реакция с молочным сахаром и раствором формальдегида (проба на Au3+); количественное определение: субстанция, дилюции до Х6 – фотоколориметрически с толуидиновым реактивом. Контроль качества базисных гомеопатических препаратов из растительного сырья (эссенции, настойки) с целью их дальнейшей стандартизации также рекомендуется проводить по содержанию биологически активных веществ. Для этого используют: Ø качественные реакции на основные группы биологически активных соединений; Ø хроматографический анализ в различных системах растворителей; Ø количественное определение инструментальными (газожидкостная хроматография, УФ- и ИК-спектрофотометрия, фотоколориметрия) и другими методами. Широко распространёнными в растительном сырье классами соединений являются: алкалоиды, кардиотонические (сердечные) гликозиды, флавоноиды, сапонины, дубильные вещества, антраценпроизводные, кумарины, витамины, полисахариды и др. Для обнаружения основных групп биологически активных веществ (БАВ) в растительном сырье и препаратах наиболее часто используют цветные качественные реакции или реакции осаждения. Алкалоиды обнаруживают следующими общими осадочными реакциями: þ с реактивом Майера (растворы ртути дихлорида и калия йодида) – бурый осадок; þ с реактивами Вагнера и Бушарда (растворы йода в растворе калия йодида) – бурый осадок; þ с реактивом Драгендорфа (раствор висмута нитрата основного, калия йодида и кислоты уксусной) – оранжево-красный или кирпично-красный осадок; þ с реактивом Марме (раствор кадмия йодида и калия йодида) – белый или желтоватый осадок; þ с реактивом Зонненшейна (раствор фосфорномолибденовой кислоты) – желтоватый осадок; þ с раствором кремневольфрамовой кислоты – беловатый осадок; þ с раствором пикриновой кислоты – жёлтый осадок; þ с раствором танина –беловатый или желтоватый осадок. При определении кардиотонических гликозидов проводят цветные реакции на различные фрагменты молекулы: на стероидную часть молекулы карденолида: þ реакцию Либермана-Бурхарда (ледяная уксусная кислота, уксусный ангидрид и концентрированная серная кислота) – на границе слоёв окраска от розовой до зелёной и синей; þ реакция Розенгейма (спиртовый раствор трихлоруксусной кислоты) – окраска от розовой до лиловой и синей; на бутенолидное (лактонное) кольцо: þ реакция Раймонда (бензольный раствор м-динитробензола и спиртовый раствор калия гидроксида); þ реакция Легаля (растворы нитропруссида натрия и натрия гидроксида) – на границе слоёв красное окрашивание в виде кольца; þ на сахарный компонент: þ реакция Келлер-Килиани (ледяная уксусная кислота со следами железа сульфата и концентрированная серная кислота) – верхний слой окрашивается в васильково-синий цвет; þ реакция с реактивом Фелинга – оранжевый осадок после гидролиза. Последняя из указанных реакций используется также для определения восстанавливающих сахаров. Наличие флавоноидов устанавливают с помощью таких реакций: þ цианидиновая проба (порошок металлического магния и концентрированная хлороводородная кислота) – флавоны, флавонолы и флавононы дают красное или оранжевое окрашивание; þ борно-лимонная реакция – 5-оксифлавоны и 5-оксифлавонолы образуют ярко-жёлтое окрашивание с жёлто-зелёной флуоресценцией; þ реакция с трёххлористой сурьмой – 5-оксифлавоны и 5-оксифлавонолы дают жёлтое или красное окрашивание; þ реакции с раствором аммиака или спиртоводным раствором натрия (калия) гидроксида – флавоны, флавонолы, флавононы и флавононолы образуют жёлтое окрашивание, при нагревании переходящее в оранжевое или красное; халконы и ауроны дают сразу красное или пурпурное окрашивание; þ реакция с хлоридом окисного железа – при наличии полифенолов появляется зеленовато-синее окрашивание; þ реакция с раствором ванилина в концентрированной хлороводородной кислоте – катехины дают красно-малиновое окрашивание; þ реакция со средним ацетатом свинца – флавоны, халконы, ауроны, содержащие свободные ортогидроксильные группировки в кольце В, образуют осадки, окрашенные в ярко-жёлтый и красный цвета. Для обнаружения сапонинов и установления их химической природы используют следующие реакции: þ проба на пенообразование (в присутствии кислоты и щёлочи) – равная по объёму и стойкости пена образуется в обеих пробирках при наличии тритерпеновых сапонинов; в случае содержания сапонинов стероидной природы в щелочной среде образуется пена в несколько раз больше по объёму и стойкости; þ реакция со спиртовым раствором холестерина – обе группы сапонинов образуют осадки; þ реакция с баритовой водой – обе группы сапонинов дают осадки; þ реакция с растворами ацетата свинца – тритерпеновые сапонины осаждаются средним ацетатом свинца, а стероидные – основным; þ реакция Либермана-Бурхарда – стероидные сапонины (как и сердечные гликозиды) дают окраску от розовой до зелёной и синей; þ реакция Лафона (раствор меди сульфата и концентрированная серная кислота) – при нагревании появляется сине-зелёное окрашивание; þ реакция Сальковского (хлороформ и концентрированная серная кислота) – наблюдается появление окраски от жёлтой до красной; þ реакция с пятихлористой сурьмой (хлороформный раствор) – появляется красное окрашивание, переходящее в фиолетовое; þ реакция с раствором натрия нитрата (в присутствии концентрированной серной кислоты) – ярко-красное окрашивание; þ реакция с ванилином (спиртовый раствор) и концентрированной серной кислотой – появляется красное окрашивание, при разбавлении водой тритерпеноиды образуют синие хлопья. Наличие кумаринов можно обнаружить с помощью: þ реакции со щёлочью и диазотированной сульфаниловой кислотой – при нагревании с раствором калия гидроксида раствор желтеет, а после добавления диазотированной сульфаниловой кислоты окраска изменяется от коричнево-красного до вишнёвого цвета; þ лактонной пробы: после нагревания препарата со спиртовым раствором калия гидроксида, разбавления водой очищенной и добавления хлороводородной кислоты помутнение или выпадение осадка указывает на вероятное наличие кумаринов. Обнаружение дубильных веществ проводят следующими качественными реакциями: þ с раствором желатина – образование мути; þ с раствором хинина гидрохлорида – аморфный осадок; þ с растворами железо-аммониевых квасцов или хлорида окисного железа появляется окрашивание: чёрно-синее – при наличии гидролизуемых дубильных веществ, и чёрно-зелёное – в присутствии конденсированных; þ с бромной водой – при наличии конденсированных дубильных веществ сразу образуется осадок; þ с раствором средней соли свинца ацетата в уксуснокислой среде – осадок выпадает при наличии гидролизуемых дубильных веществ; при добавлении к фильтрату раствора железо-аммониевых квасцов и кристаллического натрия ацетата в присутствии конденсированных дубильных веществ появляется чёрно-зелёное окрашивание; þ с кристаллическим натрия нитратом в присутствии хлороводородной кислоты – при наличии гидролизуемых дубильных веществ появляется коричневое окрашивание. Другие классы соединений определяют отдельными специфическими качественными реакциями, описание которых изложено в методических материалах по химическому анализу лекарственных растений (Гринкевич Н. И., Сафронич Л. Н., М, 1983; Ковалёв В. Н., Солодовниченко Н. М., Харьков, 1987). Для хроматографического анализа алкалоидов используют следующие системы растворителей: а) для хроматографии на бумаге: н-бутанол – уксусная кислота – вода (5:1:4); этилацетат – уксусная кислота – вода (11:21:85); н-бутанол, насыщенный водой – ледяная уксусная кислота (100:5) и др.; б) для тонкослойной хроматографии: хлороформ – ацетон – диэтиламин (5:4:1); хлороформ – диэтиламин (9:1); хлороформ – метанол – уксусная кислота (18:1:1); хлороформ – этанол (9:1) или (8:2); ацетон – раствор аммиака (95:5). Проявителями для хроматограмм служат реактив Драгендорфа, пары йода, хлороформный раствор сурьмы трихлорида. Обнаружение кардиотонических (сердечных) гликозидов методами ТСХ и хроматографии на бумаге проводят в системах: хлороформ – ацетон – вода (84:15:0,7); хлороформ – бензол – н-бутанол (78:12:5); этилацетат – бензол – вода (84:16:50); бензол – хлороформ (9:1), (7:5) или (3:7). Для проявления хроматограмм используют реактивы Раймонда (растворы м-динитробензола и калия гидроксида спиртовый) или Йенсена (25%-хлороформный раствор трихлоруксусной кислоты). Для обнаружения флавоноидов методом хроматографии на бумаге и в тонком слое сорбента рекомендуемые системы растворителей: 15% уксусная кислота; н-бутанол – уксусная кислота – вода (4:1:2); этилацетат – муравьиная кислота – вода (70:15:17) или (10:2:3); метанол – уксусная кислота – вода (18:1:1) и др. В качестве проявителей используют: 1% спиртовый раствор алюминия хлорида, 10% спиртовый раствор натрия (калия) гидрооксида, пары аммиака в УФ-свете и т. д. Дубильные вещества методом ТСХ чаще всего анализируют в системе: н-бутанол – уксусная кислота – вода (40:12:28) и обрабатывают 1% раствором ванилина в концентрированной хлороводородной кислоте. Хроматографирование сапонинов в тонком слое сорбента проводят в системах бензол – метанол (8:2); хлороформ – метанол – вода (61:32:7); изопропанол – вода – хлороформ (30:10:5); хлороформ – метанол (3:1); н-бутанол – этанол – 25% раствор аммиака (7:2:5) и др. Проявление хроматограмм проводят соответственно парами йода, 20% раствором серной кислоты и 10% спиртовым раствором фосфорновольфрамовой кислоты. Для анализа кумаринов предлагают такие системы растворителей: а) для хроматографии на бумаге: петролейный эфир – бензол – метанол (5:4:1); б) в тонком слое: бензол – этилацетат (2:1); ацетон – гексан (2:8); гексан – бензол – метанол (5:4:1). Обработку хроматограмм проводят 10% раствором калия гидроксида и диазотированной сульфаниловой кислотой. Кроме того, методами хроматографии обнаруживают такие классы химических соединений: каротиноиды – системы: хлороформ – ацетон (9:1); бензол – метанол (1:1) и др.; реактивы для проявления хроматограмм – 10% спиртовый раствор фосфорномолибденовой кислоты, пары йода; антраценпроизводные –системы: этилацетат – муравьиная кислота – вода (10:2:3), этилацетат – метанол – вода (100:17:13); реактив для проявления хроматограмм – 5% спиртовый раствор гидроксида калия (натрия); аминокислоты – системы: бутанол – уксусная кислота – вода (4:1:1), этанол – вода (95:5), изопропанол – аммиак – вода (10:1:1), изопропанол – уксусная кислота – вода (7:2:1), н-бутанол – муравьиная кислота – вода (75:15:10); реактив для проявления хроматограмм – 0,2% спиртовый или бутанольный раствор нингидрина. Примеры хроматограмм в тонком слое и на бумаге приведены на рисунке.
Количественное содержание БАВ в матричных настойках и других базисных препаратах в частных статьях фармакопей зарубежных стран указывается лишь в редких случаях, в частности при анализе настоек, содержащих ядовитые и сильнодействующие вещества (аконит, строфант, чилибуха, игнация, белладонна и др.). В нормативные документы, предназначенные для гомеопатической фармакопеи Российской федерации, включены современные методы анализа, позволяющие осуществлять контроль качества гомеопатических лекарственных средств с учётом содержания БАВ. Для этой цели можно использовать газожидкостную хроматографию, спектрофотометрию, фотоколориметрию и другие инструментальные методы, в некоторых случаях целесообразно использовать титриметрические методы анализа. ГЛАВА 8 Все лекарственные средства, используемые в гомеопатической практике для внутреннего и наружного применения, обычно готовят из основных исходных (базисных) препаратов (эссенций, настоек, растворов, тритураций) в точном соответствии с указаниями §§1–9, изложенными в руководстве В. Швабе «Гомеопатические лекарственные средства» (гомеопатическая фармакопея). При описании лекарственных средств, входящих в фармакопею, указывается параграф, согласно которому из этих средств готовятся лекарственные препараты и степень их разведения. Твёрдые лекарственные формы К группе гомеопатических лекарственных форм твёрдой консистенции относятся растирания (порошки, тритурации), гранулы (крупинки, сахарные пилюли) и таблетки, которые назначаются для внутреннего применения. В отличие от аллопатических лекарственных форм гомеопатические лекарства не глотают, а рассасывают во рту, не запивая водой, но предварительно прополоскав ротовую полость. Сублингвальное назначение обеспечивает более быстрое и полное всасывание лекарственных веществ слизистой оболочкой полости рта. Порошки (Тriturationes). Порошки готовят и отпускают в виде соответствующих разведений твердых и жидких лекарственных средств. Для дозирования порошков рекомендуют использовать специальные стеклянные или костяные лопаточки, или кофейную ложечку. Доза на один прием составляет приблизительно 0,2г. Примеры: Manganum aceticum 3 trit. На кончике кофейной ложки согласно расписанию. Количество порошка не указано, поэтому необходимо отпустить 10,0. Готовят тритурацию по правилам, изложенным в §7 (глава 7). Для этого провизор-технолог из базисной тритурации Х1 (Д1) готовит в течение 1 часа тритурацию Х2 (или С1),смешивая 1,0 тритурации Х1 и 9,0 молочного сахара. Затем аналогично готовит тритурации Х3 и Х4 (С2). Последнюю тритурацию, т. е. С2, он должен выставить на вертушку в ассистентской комнате после соответствующего контроля качества и оформления к использованию. Схема 15 Алгоритм технологии порошковых растираний из базисных
Фармацевт отвешивает 9,9 молочного сахара и 0,1 тритурации С2, после чего по всем правилам в течение 1 часа готовит тритурацию С3 (см. схемы 11 и 15). Полученную тритурацию подвергают контролю согласно показателям, указанным в разделе 7.6, после чего помещают во флакон или пакет и оформляют к отпуску соответствующим номером рецепта и порядковым номером препарата в рецепте, указывается № аптеки, масса отпускаемого препарата, дата и подпись фармацевта, приготовившего лекарство. После приготовления препарата фармацевт, как и в обычной аллопатической аптеке, заполняет паспорт письменного контроля (ППК): ППК Дата № рецепта Sacchari lactatis 9,9 Trit. Manganum acetici C2 0,1 –––––––––––––––––––––––––––––– m = 10,0 Приготовил: Проверил: Примечание: при отсутствии базисных тритураций Х3 и Х4 провизор-технолог может приготовить тритурацию С2 непосредственно из тритурации С1, взяв её в количестве 0,1 и смешав по правилам с 9,9 молочного сахара (см. схему 15). Тритурации из жидкостей любой природы готовят согласно правилам, приведенным в §§8–9 (глава 7). Пример: Valeriana X4 20,0 trit. На кончике кофейной ложки согласно расписанию. Провизор-технолог готовит по всем правилам тритурацию Х3 из настойки валерианы Х1 (1:10), взяв 0,1 (5 кап.) настойки и 9,9 молочного сахара, выставляет её на вертушку. Фармацевт отвешивает 18,0 молочного сахара и по правилам §7 в течение 1 часа смешивает с ним 2,0 тритурации Х3. Приготовленную тритурацию Х4 отдаёт на контроль, после чего упаковывает её и оформляет к отпуску номером рецепта, порядковым номером, указывая на пакете номер аптеки, массу препарата, дату и свою подпись. ППК Дата № рецепта Sacchari lactatis 18,0 Trit. Valerianae Х 3 2,0 –––––––––––––––––––––––––––––– m = 20,0 Приготовил: Проверил: Тритурации в количестве более 1 кг в качестве внутриаптечной заготовки рекомендуется готовить механическим способом. Для этого используют машины (смесители), снабжённые соскабливающим приспособлением, обеспечивающие получение тритураций требуемого качества по размеру частиц и другим показателям. При изготовлении тритураций с помощью машины сначала растирают и смешивают треть лактозы. После этого прибавляют всё количество лекарственного вещества и смешивают его с лактозой. Далее добавляют последовательно вторую, а затем третью порцию лактозы и тщательно смешивают. Время изготовления тритурации с помощью машины также должно быть не меньше 1 часа. Контроль качества порошков проводится по общим показателям: сыпучесть; равномерность распределения; соответствие окраски, вкуса, запаха; однородность и размер частиц; капиллярно-люминесцентный анализ. Определение подлинности и количественного содержания лекарственных веществ проводят в тритурациях Х1, Х2 и Х3 (как указано в частных статьях). Отклонения в содержании лекарственного вещества (если нет других указаний) не должны превышать: – ±5% при содержании 10% или 1% вещества (первое или второе десятичное разведение); – ±10% при содержании 0,1% вещества (третье десятичное разведение). Тритурации Х4, содержащие ядовитые или сильнодействующие лекарственные вещества, требующие осторожного обращения и особого хранения, должны быть проверены по методикам, приведенным в частных статьях. Методики определения приведены в разделе 7.6. Гранулы (Granulae) готовят из чистого тростникового сахара высшего качества. Они должны растворяться в воде очищенной без осадка. Гомеопатические гранулы получают путём нанесения (насыщения) на сахарные гранулы жидких препаратов (эссенций, настоек), растворов лекарственных веществ или их смесей. Технология гомеопатических гранул основана на адсорбции действующего лекарственного вещества из водно-спиртового раствора на гранулы сахара. Для получения равномерного нанесения лекарственного вещества исходные гранулы сахара должны быть строго определённого размера. Размер и класс (№) каждой партии исходных гранул определяются размерами соседних сит, через которые эти гранулы проходят (dmax) и на которых задерживаются (dmin), а также путём подсчёта количества штук в определённой массе навески гранул. Среднее количество штук подсчитывают в двух параллельных пробах массы навески гранул, взвешенной с точностью до 0,01 г. Допустимое отклонение от среднего количества гранул составляет 7%. При насыщении гранул лекарственным средством нужно исходить из того, что каждая крупинка должна соответствовать примерно одной капле лекарственного вещества. Количество лекарственного вещества, нанесенное на исходные гранулы сахара, существенно не изменяет их размер и другие показатели, поэтому характеристика гомеопатических гранул по размеру, среднему диаметру и т. д. соответствует характеристике исходных гранул. В соответствии с руководством В. Швабе гранулы бывают массой от 2 мг до 500 мг и размеров от 1 до 10. Согласно же требованиям проекта фармакопейной статьи «Гранулы гомеопатические – Granulae homoeopathica» для Российской гомеопатической фармакопеи они могут быть классов от №1 до №8 массой от 2,8 мг до 500 мг (см. таблицу сравнения). Таблица 20 Характеристика исходных сахарных гранул
Чаще употребляются гранулы 4-го и 5-го номеров (по руководству В.Швабе) или соответствующие им согласно Российской гомеопатической фармакопее. После высушивания каждая гранула имеет массу 0,032 – 0,033 г. Если в рецепте количество гранул не прописано, то их отпускают 10,0 г. Следует учитывать размер гранул при указании врачом дозировки препаратов в рецептах: если гранулы №4–5, то их прописывают в среднем по 6–7 на 1 приём; если же они мельче – дозу увеличивают до 10 гранул на приём. Насыщение гранул соответствующими жидкостями проводят следующим образом: на 1 кг исходных сахарных гранул берут 10,0 раствора лекарственного вещества соответствующего разведения, приготовленного на 60% (по массе) этиловом спирте. Для равномерного распределения наносимого вещества исходные сахарные гранулы предварительно смачивают 60% этиловым спиртом из расчёта 10,0 на 1 кг гранул. Нанесение лекарственных средств на исходные гранулы сахара производят при тщательном перемешивании (встряхивании) вручную в стеклянных плотно закрывающихся сосудах или в механических смесителях без движущихся рабочих органов (барабанные смесители, «пьяные» бочки и др.). Рабочий объём используемого смесителя должен быть в 1,5–2 раза больше загружаемой массы исходных гранул. Процесс перемешивания при ручном способе производится в течение 10 минут, в механических смесителях – в течение 3–4 минут. Приготовленные гомеопатические гранулы выкладывают на деревянные щиты, покрытые пергаментной бумагой, и высушивают на воздухе при комнатной температуре (до полного высыхания), после чего их пересыпают в соответствующую тару (см. схему 16). Нельзя насыщать гранулы лекарственными средствами, приготовленными из летучих и пахучих веществ, а также из всех кислот в разведениях ниже С3 (3-го сотенного). При изготовлении гранул необходимо соблюдать санитарные требования в соответствии с действующей Инструкцией по санитарному режиму аптек (приказ МЗ Украины от 14.06.93 №139). Схема 16 Алгоритм технологии гомеопатических гранул (крупки)
Готовые гомеопатические гранулы должны быть однородны по окраске и размеру, иметь шаровидную форму и белый с серым или желтоватым оттенком цвет (если нет других указаний в частных статьях). Примеры: а) Hypericum X3 10,0 gran. По 5–7 гранул по расписанию Фармацевт во флакон емкостью 50 мл отвешивает 10,0 сахарных гранул, откапывает каплемером 3 капли 60% спирта (0,1) и смачивает гранулы, несколько раз переворачивая и встряхивая флакон. Затем отмеривает 3 капли (0,1) настойки зверобоя Х1 и энергично перемешивает (потенцирует) в течение 10 минут, плотно закрыв горлышко флакона кружочком пергаментной бумаги или целлофана. После этого насыщенные крупинки высыпает горкой на пергаментную капсулу и сушит на воздухе. Готовые гранулы переносит во флакон для отпуска или бумажный пакет, проводит контроль качества согласно требуемым параметрам и оформляет к отпуску аналогично ранее приведенным препаратам. После этого фармацевт заполняет паспорт письменного контроля: ППК Дата № рецепта Granulae saccharati 10,0 Spiritus aethylici 60% gtts. III (0,1) Tincturae Hyperici Х1 gtts. III (0,1) –––––––––––––––––––––––––––––––––– m = 10,0 Приготовил: Проверил:
б) Belladonna 3 10,0 По 6–8 гранул согласно расписанию Для приготовления данного препарата провизор-технолог должен выставить на вертушку разведение красавки Х4 (С2), приготовленное по всем правилам из настойки Х1. Фармацевт помещает во флакон 10,0 гранул, добавляет 0,1 (3 капли) 60% спирта этилового, 0,1 (3 капли) разведения красавки С2 и насыщает гранулы по правилам, приведенным выше. Затем гранулы высушивают, проверяют качество, помещают во флакон или пакет и оформляют к отпуску как указано ранее. Затем, как обычно, фармацевт пишет паспорт письменного контроля: ППК Дата № рецепта Granulae saccharati 10,0 Spiritus aethylici 60% gtts. III (0,1) Dil. Belladonnae C2 gtts. III (0,1) ––––––––––––––––––––––––––––––- m = 10,0 Приготовил: Проверил: Контроль качества гранул проводится по следующим показателям: – внешний вид: производят визуальный осмотр невооруженным глазом 2,0 гранул, взвешенных с точностью до 0,01; – количество слипшихся гранул не должно превышать 1%: определяют в массе навески 5,0 гранул, взвешенных с точностью до 0,01; – распадаемость: 10,0 гранул помещают в коническую колбу вместимостью 100 мл, прибавляют 50 мл воды очищенной, имеющей температуру 37°С; колбу медленно покачивают 1–2 раза в секунду (производят не менее 3-х определений). Время распадаемости насыщенных сахарных гранул должно составлять не более 5 мин. (если нет других указаний в частных статьях). Для чистых гранул сахара время распадаемости составляет в среднем около 2 мин. (в зависимости от завода-изготовителя), для насыщенных гранул – в среднем около 5 мин. – общая масса: отклонение массы гранул одной упаковки от требуемой по прописи определяют взвешиванием (с точностью до 0,01) содержимого не менее 5 отдельных упаковок от каждой серии; допустимые отклонения при фасовке до 1,0 –5%, свыше 1,0 до 10,0 – 3%; – потеря в массе при высушивании: для сахарных гранул от 1% до 10% в зависимости от завода-изготовителя, для насыщенных гранул примерно от 3% до 5% в зависимости от наименования; – капиллярно-люминесцентный анализ: методика исследования препаратов в крупинках указывается для каждого препарата отдельно; обычно его проводят с 5,0 измельченных гранул аналогично тритурациям (см. раздел 7.6); По микробиологической чистоте гранулы должны соответствовать требованиям действующей ГФ. Определение подлинности и количественного содержания лекарственных веществ в гомеопатических гранулах проводят в соответствии с требованиями частных статей. Примечание: гранулы как лекарственная форма не должны назначаться больным сахарным диабетом – в этом случае врач должен прописать лекарство в виде спирто-водного раствора, дозируя его каплями. Таблетки (Tabulettae) издавна применяли в гомеопатии наряду с гранулами и тритурациями, а также пастилками, лепешками (пластинками). Таблетки готовили из тритураций путём прессования без добавления других вспомогательных веществ, причем каждая таблетка имела массу около 0,2, В настоящее время некоторые зарубежные фирмы выпускают гомеопатические таблетки
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 1443; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.33 (0.015 с.) |