
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тканевые факторы свертыванияСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Участвуют во всех фазах. Сюда относятся активные тромбопластические факторы, подобные III, VII,IX,XII,XIII факторам плазмы. В тканях есть активаторы V и VI факторов. Много гепарина, особенно в легких, предстательной железе, почках. Есть и антигепариновые вещества. Особенно важны вещества, содержащиеся в сосудистой стенке. Все эти соединения постоянно поступают из стенок сосудов в кровь и осуществляют регуляцию свертывания. Ткани обеспечивают также и выведение продуктов свертывания из сосудов. 6-9. Вторичный (коагуляционный) гемостаз: последовательность процессов (3 фазы, факторы, участвующие в каждой фазе, схема, отражающая процесс взаимодействия этих факторов), оценка состояния системы вторичного гемостаза. Ферментативная теория свертывания. Первая теория, объясняющая процесс свертывания крови работой специальных ферментов, была разработана в 1902 г. русским ученым Шмидтом. Он считал, что свертывание протекает в две фазы. В первую один из белков плазмы протромбин под влиянием освобождающихся из разрушенных при травме клеток крови, особенно тромбоцитов, ферментов (тромбокиназы) и ионов Са переходит в фермент тромбин. На второй стадии под влиянием фермента тромбина растворенный в крови фибриноген превращается в нерастворимый фибрин, который и заставляет кровь свертываться. В последние годы жизни Шмидт стал выделять в процессе гемокоагуляции уже 3 фазы: 1- образование тромбокиназы, 2- образование тромбина. 3- образование фибрина. Дальнейшее изучение механизмов свертывания показало, что это представление весьма схематично и не полностью отражает весь процесс. Основное заключается в том, что в организме отсутствует активная тромбокиназа, т.е. фермент, способный превратить протромбин в тромбин (по новой номенклатуре ферментов этот следует называть протромбиназой). Оказалось, что процесс образования протромбиназы очень сложен, в нем участвует целый ряд т.н. тромбогенных белков-ферментов, или тромбогенных факторов, которые, взаимодействуя в каскадном процессе, все необходимы для того, чтобы свертывание крови осуществилось нормально. Кроме того, было обнаружено, что процесс свертывания не кончается образованием фибрина, ибо одновременно начинается его разрушение. Таким образом, современная схема свертывания крови значительно сложнее Шмидтовой. Современная схема свертывания 5 фаз, последовательно сменяющих друг друга. Фазы эти следующие: 1. Образование протромбиназы. 2. Образование тромбина. 3. Образование фибрина. 4. Полимеризация фибрина и организация сгустка. 5. Фибринолиз. За последние 50 лет было открыто множество веществ, принимающих участие в свертывании крови, белков, отсутствие которых в организме приводит к гемофилии (не свертываемости крови). Рассмотрев все эти вещества, международная конференция гемокоагулологов постановила обозначить все плазменные факторы свертывания римскими цифрами, клеточные - арабскими. Это было сделано для того, чтобы исключить путаницу в названиях. И теперь в любой стране после общепринятого в ней названия фактора (они могут быть разными) обязательно указывается номер этого фактора по международной номенклатуре. Имеется три группы факторов, участвующих в коагуляционном гемостазе плазменные, клеточные и тканевые. Таблица 1. Плазменные факторы свертывания крови.
В последние годы были обнаружены и другие факторы свертывания, которые еще не утверждены международной классификацией. Важнейшими из них являются следующие:
Активация плазменных факторов происходит главным образом за счет протеолиза и сопровождается отщеплением пептидных ингибиторов. Активное состояние фактора обозначается присоединением к его номеру буквы «а» (фактор IIа, Va, VIIa и т. д.). Плазменные факторы делят на 2 группы: витамин К-зависимые (образуются преимущественно в печени под влиянием витамина К) и витамин К-независимые (для синтеза которых витамин К не требуется). В эритроцитах обнаружены многие соединения, аналогичные тромбоцитарным факторам (см. раздел 6.2.3). Важнейшим из них является фосфолипидный фактор, или частичный тромбопластин (напоминает фактор Р3), который входит в состав мембраны. Кроме того, эритроциты содержат большое количество АДФ, фибриназу и другие факторы. При травме сосуда около 1% наименее стойких эритроцитов вытекающей крови разрушается, что способствует образованию тромбоцитарной пробки и фибринового сгустка. Особенно велика роль эритроцитов в свертывании крови в случае их массового разрушения (переливание несовместимой крови, резус-конфликт матери и плода, гемолитические анемии и др.) Лейкоциты содержат факторы свертывания, получившие наименование лейкоцитарных. В частности, моноциты и макрофаги при стимуляции антигеном синтезируют белковую часть тромбопластина — апопротеин III, что значительно ускоряет свертывание крови. Эти же клетки являются продуцентами витамин К-зависимых факторов свертывания — II, VII, IX и X. Приведенные факторы являются одной из основных причин возникновения диссеминированного (распространенного) внутрисосудистого свертывания крови (ДВС-синдром) при многих воспалительных и инфекционных заболеваниях, что значительно отягощает течение патологического процесса, а иногда служит причиной смерти больных. Важная роль в процессе свертывания крови отводится тканевым факторам, к которым в первую очередь относится тромбопластин (фактор 3). Концентрация тромбопластина высока в коре большого мозга, легких, плаценте и стимулированном антигенами эндотелии сосудов. При разрушении тканей и стимуляции эндотелия большое количество тромбопластина поступает в кровоток, что может вызывать развитие ДВС-синдрома. Современная схема гемостаза. Попытаемся теперь объединить в одну общую систему все факторы свертывания и разберем современную схему гемостаза. Цепная реакция свертывания крови начинается с момента соприкосновения крови с шероховатой поверхностью раненного сосуда или тканью. Это вызывает активацию тромбопластических факторов плазмы и затем происходит поэтапное образование двух отчетливо различающихся по своим свойствам протромбиназ - кровяной и тканевой.. Однако прежде, чем закончится цепная реакция образования протромбиназы, в месте повреждения сосуда происходят процессы, связанные с участием тромбоцитов (т.н. сосудисто-тромбоцитарный гемостаз). Тромбоциты за счет своей способности к адгезии налипают на поврежденный участок сосуда, налипают друг на друга, склеиваясь тромбоцитарным фибриногеном. Все это приводит к образованию т.н. пластинчатого тромба ("тромбоцитарный гемостатический гвоздь Гайема"). Адгезия тромбоцитов происходит за счет АДФ, выделяющейся из эндотелия и эритроцитов. Этот процесс активируется коллагеном стенки, серотонином, XIII фактором и продуктами контактной активации. Сначала (в течение 1-2 минут) кровь еще проходит через эту рыхлую пробку, но затем происходит т.н. вискозное перерождение тромба, он уплотняется и кровотечение останавливается. Понятно что такой конец событий возможен только при ранении мелких сосудов, там, где артериальное давление не в состоянии выдавить этот "гвоздь". 1 фаза свертывания. В ходе первой фазы свертывания, фазе образования протромбиназы, различают два процесса, которые протекают с разной скоростью и имеют различное значение. Это - процесс образования кровяной протромбиназы, и процесс образования тканевой протромбиназы. Длительность 1 фазы составляет 3-4 минуты. однако, на образование тканевой протромбиназы тратится всего 3-6 секунд. Количество образующейся тканевой протромбиназы очень мало, ее недостаточно для перевода протромбина в тромбин, однако тканевая протромбиназа выполняет роль активатора целого ряда факторов, необходимых для быстрого образования кровяной протромбиназы. В частности, тканевая протромбиназа приводит к образованию малого количества тромбина, который переводит в активное состояние V и VIII факторы внутреннего звена коагуляции. Каскад реакций, заканчивающихся образованием тканевой протромбиназы (внешний механизм гемокоагуляции), выглядит следующим образом: 1. Контакт разрушенных тканей с кровью и активация III фактора - тромбопластина. 2. III фактор переводит VII в VIIa (проконвертин в конвертин). 3.Образуется комплекс (Ca++ + III + VIIIa) 4. Этот комплекс активирует небольшое количество Х фактора - Х переходит в Ха. 5. (Хa + III + Va + Ca) образуют комплекс, который и обладает всеми свойствами тканевой протромбиназы. Наличие Va (VI) связано с тем, что в крови всегда есть следы тромбина, который активирует V фактор. 6. Образовавшееся небольшое количество тканевой протромбиназы переводит небольшое количество протромбина в тромбин. 7. Тромбин активирует достаточное количество V и VIII факторов, необходимых для образования кровяной протромбиназы. В случае выключения этого каскада (например, если со всею предосторожностью с использованием парафинированных игл, взять кровь из вены, предотвратив ее контакт с тканями и с шероховатой поверхностью, и поместить ее в парафинированную пробирку), кровь свертывается очень медленно, в течение 20-25 минут и дольше. Ну, а в норме одновременно с уже описанным процессом запускается и другой каскад реакций, связанных с действием плазменных факторов, и заканчивающийся образованием кровяной протромбиназы в количестве, достаточном для перевода большого количества протромбина с тромбин. Реакции эти следующие (внутренний механизм гемокоагуляции):
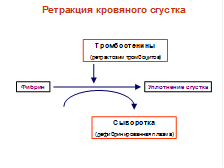
2.Активный ХII фактор превращает XI в активное состояние и образуется новый комплекс XIIa +Ca++ +XIa + III(ф3) 3. Под влиянием указанного комплекса IX фактор активизируется и образуется комплекс IXa + Va + Cа++ +III(ф3). 4. Под влиянием этого комплекса происходит активация значительного количества Х фактора, после чего в большом количестве образуется последний комплекс факторов: Xa + Va + Ca++ + III(ф3), который и носит название кровяная протромбиназа. На весь этот процесс затрачивается в норме около 4-5 минут, после чего свертывание переходит в следующую фазу. 2 фаза свертывания - фаза образования тромбина заключается в том, что под влиянием фермента протромбиназы II фактор (протромбин) переходит в активное состояние (IIa). Это протеолитический процесс, молекула протромбина расщепляется на две половинки. Образовавшийся тромбин идет на реализацию следующей фазы, а также используется в крови для активации все большего количества акцелерина (V и VI факторов). Это пример системы с положительной обратной связью. Фаза образования тромбина продолжается несколько секунд. 3 фаза свертывания - фаза образования фибрина - тоже ферментативный процесс, в результате которого от фибриногена благодаря воздействию протеолитического фермента тромбина отщепляется кусок в несколько аминокислот, а остаток носит название фибрин-мономер, который по своим свойствам резко отличается от фибриногена. В частности, он способен к полимеризации. Это соединение обозначается как Im. 4 фаза свертывания - полимеризация фибрина и организация сгустка. Она тоже имеет несколько стадий. Вначале за несколько секунд под влиянием рН крови, температуры, ионного состава плазмы происходит образование длинных нитей фибрин-полимера Is который, однако, еще не очень стабилен, так как способен растворяться в растворах мочевины. Поэтому на следующей стадии под действием фибрин-стабилизатора Лаки-Лоранда (XIII фактора) происходит окончательная стабилизация фибрина и превращение его в фибрин Ij. Он выпадает из раствора в виде длинных нитей, которые образуют сетку в крови, в ячейках которой застревают клетки. Кровь из жидкого состояния переходит в желеобразное (свертывается). Следующей стадией этой фазы является длящаяся достаточно долго (несколько минут) ретракия (уплотнение) сгустка, которая происходит за счет сокращения нитей фибрина под действием ретрактозима (тромбостенина). В результате сгусток становится плотным, из него выжимается сыворотка, а сам сгусток превращается в плотную пробку, перекрывающую сосуд - тромб.
5 фаза свертывания - фибринолиз. Хотя она фактически не связана с образованием тромба, ее считают последней фазой гемокоагуляции, так как в ходе этой фазы происходит ограничение тромба только той зоной, где он действительно необходим. Если тромб полностью закрыл просвет сосуда, то в ходе этой фазы этот просвет восстанавливается (происходит реканализация тромба). Практически фибринолиз всегда идет параллельно с образованием фибрина, предотвращая генерализацию свертывания и ограничивая процесс. Растворение фибрина обеспечивается протеолитическим ферментом плазмином (фибринолизином) который содержится в плазме в неактивном состоянии в виде плазминогена (профибринолизина). Переход плазминогена в активное состояние осуществляется специальным активатором, который в свою очередь образуется из неактивных предшественников (проактиваторов), высвобождающихся из тканей, стенок сосудов, клеток крови, особенно тромбоцитов. В процессах перевода проактиваторов и активаторов плазминогена в активное состояние большую роль играют кислые и щелочные фосфатазы крови, трипсин клеток, тканевые лизокиназы, кинины, реакция среды, XII фактор. Плазмин расщепляет фибрин на отдельные полипептиды, которые затем утилизируются организмом.
Послефаза процесса свертывания крови: ретракция сгустка и фибринолиза. Три фазы фибринолиза. Противосвертывающая система: понятие, первичные и вторичные антикоагулянты. Регуляция процессов свертывания крови. Фибринолиз - это процесс растворения фибрина. Хотя он фактически не связан с образованием тромба, фибринолиз считают послефазой гемокоагуляции, так как в ходе его происходит ограничение тромба только той зоной, где он действительно необходим. Если тромб полностью закрыл просвет сосуда, то в ходе этой фазы этот просвет восстанавливается (происходит реканализация тромба). Практически фибринолиз всегда идет параллельно с образованием фибрина, предотвращая генерализацию свертывания и ограничивая процесс.
Рис. 1. Схема образования плазмина и фибринолиз. Фибринолиз, как и процесс свертывания крови, может протекать по внешнему и внутреннему механизму (пути). Внешний механизм активации фибринолиза осуществляется при участии тканевых активаторов, которые синтезируются главным образом в эндотелии сосудов. К ним относятся тканевый активатор плазминогена (ТАП) и урокиназа. Последняя также образуется в юкстагломеруляриом комплексе (аппарате) почки). Внутренний механизм активации фибринолиза осуществляется плазменными активаторами, а также активаторами форменных элементов крови — лейкоцитов, тромбоцитов и эритроцитов и разделяется на Хагеман-зависимый и Хагеман-независимый. Хагеман-зависимый фибринолиз протекает под влиянием факторов XIIа и калликреина, которые переводят плазминоген в плазмин. Хагеман-независимый фибринолиз осуществляется наиболее быстро и носит срочный характер. Его основное назначение сводится к очищению сосудистого русла от нестабилизированного фибрина, образующегося в процессе внутрисосудистого свертывания крови. В плазме находятся и ингибиторы фибринолиза. Важнейшими из них являются α2-антиплазмин, связывающий плазмин, трипсин, калликреин, урокиназу, ТАП и, следовательно, вмешивающийся в процесс фибринолиза как на ранних, так и на поздних стадиях. Сильным ингибитором плазмина служит α1-протеазный ингибитор. Кроме того, фибринолиз тормозится α2-макроглобулином, C1-протеазным ингибитором, а также рядом ингибиторов активатора плазминогена, синтезируемых эндотелием, макрофагами, моноцитами и фибробластами. Фибринолитическая активность крови во многом определяется соотношением активаторов и ингибиторов фибринолиза. При ускорении свертывания крови и одновременном торможении фибринолиза создаются благоприятные условия для развития тромбозов, эмболии и ДВС-синдрома. Наряду с ферментативным фибринолизом, по мнению профессора Б. А. Кудряшова, существует так называемый неферментативный фибринолиз, который обусловлен комплексными соединениями естественного антикоагулянта гепарина с ферментами и гормонами. Неферментативный фибринолиз приводит к расщеплению нестабилизированного фибрина, очищая сосудистое русло от фибрин-мономеров и фибрина s (Fs). Антикоагулянты. Несмотря на то, что в циркулирующей крови имеются все факторы, необходимые для образования тромба, в естественных условиях при наличии целостности сосудов кровь остается жидкой. Это обусловлено наличием в кровотоке противосвертывающих веществ, получивших название естественных антикоагулянтов, или фибринолитического звена системы гемостаза. Естественные антикоагулянты делят на первичные и вторичные. Первичные антикоагулянты всегда присутствуют в циркулирующей крови, вторичные — образуются в результате протеолитического расщепления факторов свертывания крови в процессе образования и растворения фибринового сгустка. Первичные антикоагулянты можно разделить на три основные группы: 1) антитромбопластины — обладающие антитромбопластическим и антипротромбиназным действием; 2) антитромбины — связывающие тромбин; 3) ингибиторы самосборки фибрина — дающие переход фибриногена в фибрин. Следует заметить, что при снижении концентрации первичных естественных антикоагулянтов создаются благоприятные условия для развития тромбозов и ДВС-синдрома. К вторичным антикоагулянтам относят «отработанные» факторы свертывания крови (принявшие участие в свертывании) и продукты деградации фибриногена и фибрина (ПДФ), обладающие мощным антиагрегационным и противосвертывающим действием, а также стимулирующие фибринолиз. Роль вторичных антикоагулянтов сводится к ограничению внутрисосудистого свертывания крови и распространения тромба по сосудам.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 2683; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.102 (0.01 с.) |

 крови включает в себя
крови включает в себя
 1. Контакт с шероховатой или чужеродной поверхностью приводит к активации XII фактора: XII -- XIIa. Одновременно начинает образовываться гемостатический гвоздь Гайема (сосудисто-тромбоцитарный гемостаз).
1. Контакт с шероховатой или чужеродной поверхностью приводит к активации XII фактора: XII -- XIIa. Одновременно начинает образовываться гемостатический гвоздь Гайема (сосудисто-тромбоцитарный гемостаз).


 Общая схема свертывания крови и фибринолиза.
Общая схема свертывания крови и фибринолиза. Растворение фибрина обеспечивается протеолитическим ферментом плазмином (фибринолизином) который содержится в плазме в неактивном состоянии в виде плазминогена (профибринолизина). Переход плазминогена в активное состояние осуществляется специальным активатором, который в свою очередь образуется из неактивных предшественников (проактиваторов), высвобождающихся из тканей, стенок сосудов, клеток крови, особенно тромбоцитов. В процессах перевода проактиваторов и активаторов плазминогена в активное состояние большую роль играют кислые и щелочные фосфатазы крови, трипсин клеток, тканевые лизокиназы, кинины, реакция среды, XII фактор. Плазмин расщепляет фибрин на отдельные полипептиды, которые затем утилизируются организмом.
Растворение фибрина обеспечивается протеолитическим ферментом плазмином (фибринолизином) который содержится в плазме в неактивном состоянии в виде плазминогена (профибринолизина). Переход плазминогена в активное состояние осуществляется специальным активатором, который в свою очередь образуется из неактивных предшественников (проактиваторов), высвобождающихся из тканей, стенок сосудов, клеток крови, особенно тромбоцитов. В процессах перевода проактиваторов и активаторов плазминогена в активное состояние большую роль играют кислые и щелочные фосфатазы крови, трипсин клеток, тканевые лизокиназы, кинины, реакция среды, XII фактор. Плазмин расщепляет фибрин на отдельные полипептиды, которые затем утилизируются организмом.


