
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теплота процесса в различных условияхСодержание книги
Поиск на нашем сайте
Изохорный процесс (V = const) Работа изохорного процесса W = 0. Тогда, как следует из первого начала термодинамики, теплота процесса в изохорных условиях QV равна изменению внутренней энергии:
Так как внутренняя энергия является функцией состояния, то в изохорных условиях теплота
приобретает свойства функции состояния.
Изотермический процесс (T = const) По закону Гей-Люсака-Джоуля внутренняя энергия идеального газа зависит только от температуры и не зависит от объема и давления. Следовательно, в изотермическом процессе не происходит изменения внутренней энергии (Δ U = 0). Тогда из первого начала термодинамики следует
Таким образом, вся теплота в изотермическом процессе идет на совершение работы, Работа изотермического процесса совершается за счет подведенной теплоты.
Изобарный процесс (p = const)
или для конечного процесса
Функция H = U + pV называется энтальпией. Энтальпия, как и внутренняя энергия, является функцией состояния, поэтому в изобарных условиях теплота QP приобретает свойства функции состояния. Изохорный и изобарный тепловые эффекты связаны соотношением
Методы расчета и измерения тепловых эффектов химических реакций рассматриваются в разделе физической химии – термохимии. Рассмотрим практически важные из них. Закон Гесса является основным законом термохимии. Он гласит: Тепловой эффект процесса не зависит от пути его протекания (промежуточных стадий), а определяется начальным и конечным состоянием системы при условии, что давление и температура или объем системы и температура в ходе всего процесса остаются постоянными. Закон Гесса позволяет рассчитывать тепловые эффекты реакций, если известны тепловые эффекты других реакций с участием тех же веществ. Из закона Гесса следует два важных следствия: 1. Тепловой эффект химической реакции равен разности сумм теплот образования продуктов реакции и исходных веществ (с учетом стехиометрических коэффициентов). Теплотой образования вещества называется тепловой эффект реакции образования одного моля вещества из простых веществ. Простым веществом называется химическое соединение, состоящее из атомов одного элемента, в наиболее устойчивой модификации при данных условиях. В изобарных условиях теплота образования (энтальпия образования) обозначается Δ f H (f – сокращение от английского слова formation – образование). Значения теплот образования при стандартных условиях
2. Тепловой эффект химической реакции равен разности сумм теплот сгорания исходных веществ и продуктов реакции (с учетом стехиометрических коэффициентов). Теплотой сгорания вещества Δ c H (c – сокращение от английского слова combustion – горение) называется тепловой эффект реакции сгорания одного моля вещества в избытке кислорода до CO2, H2O(ж.), N2, SO2 и галогеноводородов. Стандартные теплоты сгорания
|
|||||||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 197; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.243.130 (0.007 с.) |

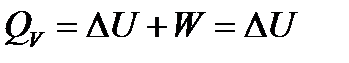
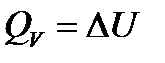
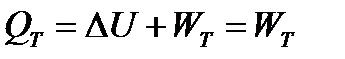
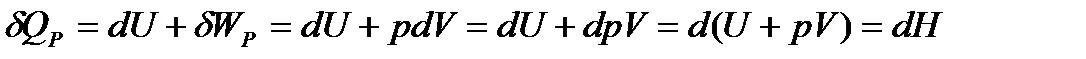
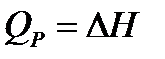
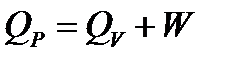
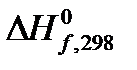 для большого количества веществ приведены в таблицах стандартных термодинамических величин в справочниках (см., например, [2]). Стандартные условия – нормальное атмосферное давление 101320 Па (1 атм или 760 мм рт. ст.). Для термодинамических функций, стандартные условия указываются надстрочным индексом “0”. Например, H 0.
для большого количества веществ приведены в таблицах стандартных термодинамических величин в справочниках (см., например, [2]). Стандартные условия – нормальное атмосферное давление 101320 Па (1 атм или 760 мм рт. ст.). Для термодинамических функций, стандартные условия указываются надстрочным индексом “0”. Например, H 0. можно найти в справочниках, однако, они приведены для значительно меньшего количества веществ (в основном органических), чем теплоты образования.
можно найти в справочниках, однако, они приведены для значительно меньшего количества веществ (в основном органических), чем теплоты образования.


