Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Раздел. 1. Статическая биохимияСодержание книги
Поиск на нашем сайте
БИОХИМИЯ Задания для контрольных работ студентам заочного обучения ветеринарно-медицинского и биолого-технологического факультетов Барнаул 2014
УДК
Биохимия. Задания для контрольных работ студентам заочного обучения ветеринарно-медицинского и биолого-технологического факультетов / Сост.: Л.Г.Протопопова, Т.Э.Шпис – Изд-во АГАУ, 2014. – с.
Рецензент –
Предназначено студентам, обучающимся по специальностям «Зоотехния», «Технология производства и переработки сельскохозяйственной продукции», «Продукты питания животного происхождения», «Ветеринария», «Ветеринарно-санитарная экспертиза», «Товароведение и экспертиза продовольственных товаров», изучающим дисциплины «Биохимия» и «Биохимия сельскохозяйственной продукции»
Настоящие методические указания предназначены для самостоятельного изучения и написания контрольной работы студентами заочного обучения по курсу «Биохимия»
Рекомендовано к печати методической комиссией агрономического факультета (протокол от 2014 г.)
© Алтайский государственный аграрный университет, 2014
Введение Огромные масштабы проникновения химии во все области сельского хозяйства требуют от специалистов высшей квалификации фундаментальных химических знаний.
Цель дисциплин: формирование современных представлений, знаний и умений о превращениях веществ и энергии в живых организмах, химическом составе сельскохозяйственной продукции растительного и животного происхождения, биохимических процессах, происходящих в ней при хранении и переработке. Освоение данных дисциплин направлено на формирование у обучающихся следующих компетенций: 1. Владение культурой мышления, способностью к обобщению, анализу, восприятию информации, постановке цели и выбору путей ее достижения 2. Умение логически верно, аргументированно и ясно строить устную и письменную речь 3. Способность использовать основные законы естественнонаучных дисциплин в профессиональной деятельности, применять метода математического анализа и моделирования, теоретического и экспериментального исследования 4. Способностью проводить эксперименты по заданной методике и анализировать результаты В результате изучения курса студент должен
знать: состав, строение, свойства и биологические функции основных групп углеводов, липидов, азотистых, фенольных и терпеноидных соединений, витаминов, органических кислот, алкалоидов и гликозидов, эфирных масел; современные сведения о ферментах и методах биохимии; особенностях функционирования ферментных систем в клетках организмов и применении ферментов в технологиях производства и переработки сельскохозяйственной продукции; принципы осуществления биоэнергетических превращений в организмах; биохимические процессы синтеза, превращений и распада органических веществ в организмах; химический состав молока, мяса и вторичного мясного и молочного сырья; химический состав зерна злаковых и зернобобовых культур, семян масличных растений, клубней картофеля, корнеплодов, овощей, плодов и ягод; причины и параметры изменения химического состава и животных и растительных продуктов в зависимости от различных факторов, биохимические процессы при хранении и переработке.
уметь: работать с химической информацией; применять полученную информацию для решения поставленных задач; адаптировать знания к решению конкретных задач, связанных с профессиональной деятельности; аргументированно и ясно излагать ход размышлений при решении практических задач, формулировать выводы; прогнозировать ход биохимических процессов в соответствии с принципами биохимической энергетики и в зависимости от условий окружающей среды; организовывать и проводить эксперименты по заданной методике и анализировать полученные результаты; применять знания о химическом составе и биохимических процессах при обосновании технологий производства, хранения и переработки животной и растительной продукции;
владеть: навыками аналитической работы с фундаментальной и справочной химической литературой; терминами и понятиями биохимии при оценке химического состава, технологических свойств сельскохозяйственной продукции; методологией исследования; методами обработки экспериментальных данных
Общие методические указания
В обязательный план обучения входит посещение лекций, выполнение контрольной работы, выполнение лабораторного практикума, сдача зачета по лабораторному практикуму, сдача экзамена по всему курсу. Лекции. Для студентов заочного обучения читаются лекции по важнейшим разделам курса. Контрольные задания. Студент выполняет одну контрольную работу по своему варианту. Контрольная работа выполняется в отдельной тетради или на листах формата А-4. Для определения варианта контрольной работы берутся две последние цифры номера зачетной книжки. Например, студент с шифром 99135 выполняет контрольные задания варианта 35, которые указаны в таблице вариантов (см. приложение № 1). При оформлении контрольной работы на титульном листе указываются наименование университета, факультет и специальность (название и шифр), дисциплина, Ф.И.О. студента (см. приложение № 2). При выполнении задания необходимо переписать условие задачи. Для замечаний рецензента оставляют поля. В конце работы указывают используемую литературу, ставят подпись и дату выполнения работы. Если контрольная работа не зачтена, то неверно решенные задачи исправляются студентом в этой же тетради на чистых листах. Лабораторные занятия. Выполняются студентом по основным разделам курса. Для выполнения лабораторных работ студенту необходимо иметь лабораторную тетрадь. Зачет. После выполнения лабораторного практикума студенты сдают зачет по практическому материалу. Для сдачи зачета в объеме курса необходимо уметь объяснять ход выполнения опытов, принципы методов, делать выводы, составлять уравнения реакций. Экзамен. К сдаче экзамена допускаются студенты, которые выполнили контрольную работу, получили зачет по лабораторному практикуму.
Контрольные задания
Тема. Биохимия печени 264. Перечислите основные функции печени. 265. Какие биохимические реакции протекают в печени? Напишите реакцию дезаминирования глутаминовой кислоты. 266. Охарактеризуйте роль печени в обмене углеводов. 267. Какие изменения углеводного обмена происходят при болезнях печени? 268. Какую роль играет печень в липидном обмене? 269. Перечислите и охарактеризуйте основные патологии липидного обмена в печени. Роль липотропных веществ. 270. Опишите роль печени в обмене аминокислот, белков. 271. Какие изменения белкового обмена происходят при болезнях печени? 272. Какую биохимическую роль играет печень в обмене гормонов, минеральных веществ и витаминов. 273. Какие виды обезвреживания (детоксикации) происходят в печени? 274. Приведите примеры обезвреживания чужеродных веществ (ксенобиотиков) и эндогенных токсинов в печени. 275. Экскреторная функция печени. Химический состав желчи. Функциональные пробы, отражающие экскреторную функцию печени.
Тема. Биохимия мышц и мяса
276. Назовите отличия в строении поперечнополосатой мышечной ткани от гладкой мышечной. Назовите основные компоненты мышечной ткани. 277. Химический состав мышц: важнейшие белки (миозин, актин, актомиозин, тропонин) и экстрактивные вещества. Биосинтез креатинина, обмен креатинфосфата. Биохимические механизмы мышечного сокращения и расслабления. 278. Саркоплазматические белки: миоглобин, его строение и функция. Особенности энергетического обмена в мышцах. Биохимические изменения при мышечных дистрофиях. Креатинин и креатинурия у детей. 279. Важнейшие белки межклеточного матрикса: коллаген, эластин. Биосинтез и созревание коллагена. Участие витамина С в синтезе коллагена. Экскреция оксипролина — показатель скорости распада коллагена. 280. Структурная организация и основные функции межклеточного матрикса и соединительной ткани. Протеогликаны. Гликозаминогликаны. Роль соединительной ткани в заживлении ран. 281. Назовите основные биогенные молекулы мышц, участвующих в энергетических процессах. Дайте им характеристику. Синтез креатинфосфата. Его биологическая роль. 282. Напишите формулы карнитина, карнозина, ансерина. Их биологическая роль. 283. Дайте характеристику основных липидов мышечной ткани. 284. Опишите процессы перекисное окисление липидов. Высоко- и низкомолекулярные антиоксиданты мышц. Возможности использования антиоксидантов в животноводстве. 285. Охарактеризуйте пищевую и энергетическую ценность мяса (говядина, телятина, свинина, баранина). 286. Охарактеризуйте пищевую и энергетическую ценность мяса птиц и кроликов. 287. Охарактеризуйте влияние возраста животного, пола, породы, кормов, здоровья на качество мяса и его биохимический состав. 288. Опишите биологическое значение белков мяса и их химический состав. КБП (качественный белковый показатель). КИБ (коэффициент использования белка). 289. Дайте характеристику биологического значения липидов мяса (триглицериды, фосфолипиды, холистерин) и их химического состава. Температура плавления и йодное число жиров. 290. Перечислите минеральные вещества и витамины мяса, их биологическую роль и содержание в мясе. 291. Охарактеризуйте биохимические процессы послеубойного окоченения. 292. Опишите процессы созревания (ферментации) мяса. 293. Назовите и охарактеризуйте основные пороки созревания мяса (виды порчи) 294. Охарактеризуйте физические и биохимические изменения при замораживании и хранении мяса. 295. Опишите способы повышения устойчивости мяса и мясопродуктов при хранении и переработке. Действие химических консервантов, антибиотиков, фитонцидов. 296. Опишите химические изменения мяса при посоле. Действие поваренной соли, сахара, нитратов и нитритов. 297. Охарактеризуйте физико-химические изменения мяса при термической обработке, копчении. 298. Раскройте роль стрессовых факторов, влияющих на качество мяса. Профилактика предубойных стрессов. 299. Перечислите посторонние вещества (антибиотики, пестициды, нитраты, тяжелые металлы, радиоактивные изотопы и др.) мяса. Тема. Биохимия молока 300. Охарактеризуйте основные этапы образования и выделения молока, апокриловый и мерокриловый типы секреции молока. 301. Охарактеризуйте молозивный, основной, стародойный периоды лактации. 302. Назовите основные компоненты молока – средний химический состав, сухой остаток, СОМО. 303. Опишите особенности химического состава и физико-химических свойств молозива. 304. Дать характеристику казеинов молока. 305. Дать характеристику основных сывороточных белков молока. 306. Дать характеристику небелковых азотистых соединений молока (мочевина, пептиды и аминокислоты, креатин, креатинин, аммиак, мочевая кислота). 307. Дать характеристику ферментов молока – оксидоредуктазы (дегидрогеназы, оксидазы, пероксидазы, каталаза), гидролазы (липаза, фосфатаза, лактаза, амилаза, протеиназы), лактозосинтетаза, декарбоксилаза. 308. Напишите структурную формулу лактозы и охарактеризуйте ее свойства. Объясните образование лактулозы. Моносахара молока. Строение, содержание. Их фосфорные эфиры. 309. Охарактеризуйте гормоны молока – пролактин, окситоцин, кортикостериоды, андрогены, эстрагены, тироксин. 310. Дать характеристику основных витаминов молока. 311. Дать характеристику макро- и микроэлементов молока. 312. Дать характеристику липидов молока. 313. Дать характеристику фосфолипидов и стеринов молока. 314. Опишите физико-химические свойства молочного жира: число омыления, йодное число, число Рейхерта-Мейссля и др. 315. Назовите посторонние вещества (антибиотики, микотоксины, пестициды, нитраты, тяжелые металлы, радиоактивные изотопы и др.) молока. 316. Опишите физико-химические свойства молока (плотность, кислотность и др.). 317. Раскройте роль возраста животного, сезонов и периода лактации на качество молока и его биохимический состав. 318. Раскройте роль здоровья животного на качество молока и его биохимический состав. 319. Раскройте роль кормов на качество молока и его биохимический состав. 320. Раскройте роль породы животного на качество молока и его биохимический состав. 321. Опишите состав и свойства молока других сельскохозяйственных животных (козье, овечье, кобылье). 322. Охарактеризуйте физико-химические изменения молока при его охлаждении и замораживании 323. Охарактеризуйте физико-химические изменения молока при его нагревании. 324. Объясните проявления бактерицидных свойств молока. Микрофлора молока. 325. Опишите биохимические процессы при разных видах брожения углеводов молока (молочнокислое, пропионовокислое, спиртовое, маслянокислое). 326. Дайте характеристику основным биохимическим процессам при производстве кисломолочных продуктов. 327. Дайте характеристику основным биохимическим процессам при производстве сыров. 328. Дайте характеристику основным биохимическим процессам при производстве масла. 329. Назовите основные пороки молока биохимического происхождения.
Тема. Биохимия крови 330. Как проводится отбор образцов крови для анализов? 331. Опишите физико-химические свойства крови (рН, осмотическое давление, вязкость) и их клинико-диагностическое значение. 332. Охарактеризуйте химический состав крови. 333. Перечислите и охарактеризуйте белки плазмы крови. 334. Опишите альбумины крови по схеме: строение, биосинтез, период полураспада, изоэлектрическая точка, содержание в плазме крови в норме и при патологиях. 335. Охарактеризуйте глобулины крови (α, β, γ) по схеме: строение, биологическая роль, содержание в норме и при патологиях. 336. Опишите специфические белки плазмы крови: церулоплазмин, интерферон, пропердин, их биологическую роль, содержание в норме и при патологиях. 337. Изобразите строение гемоглобина и его патологических форм. 338. Что такое анемия? Опишите основные виды анемий (серповидная, геминовая, смешанная, инфекционная). 339. Опишите липо- и гликопротеиды крови по схеме: состав, формы, биологическая роль и их клинико-диагностическое значение. 340. Приведите методы разделения липопротеидов плазмы крови, характеристика отдельных фракций, диагностическое значение, их определения (ЛПОН, ХМ, ЛПНП, ЛПВП). 341. Охарактеризуйте фибриноген крови по схеме: строение, биологическая роль, клинико-диагностическое значение. Приведите основные патологии свертывания крови. 342. Опишите ферменты крови, энзимодиагностика в клинической биохимии. 343. Перечислите небелковые азотистые вещества крови и их клинико-диагностическое значение. 344. Что называется остаточным азотом плазмы крови? Опишите его клинико-диагностическое значение. 345. Охарактеризуйте мочевину и мочевую кислоту плазмы крови по схеме: строение, биосинтез, содержание в норме и при патологиях, клинико-диагностическое значение. 346. Опишите билирубин плазмы крови по схеме: строение, содержание в норме и при патологиях, клинико-диагностическое значение. 347. Охарактеризуйте углеводы плазмы крови по схеме: строение, содержание в норме и при патологиях, клинико-диагностическое значение. 348. Опишите холестерин крови по схеме: строение, содержание в норме и при патологиях, клинико-диагностическое значение. 349. Перечислите и охарактеризуйте электролиты крови и их клинико-диагностическое значение. 350. Опишите биологическую роль и клинико-диагностическое значение 351. макроэлементов крови. 352. Перечислите жирорастворимые витамины крови, признаки гипо-, гипер- и авитаминозов, содержание в норме и клинико-диагностическое значение. 353. Какие витамины крови относятся к антианемическим? Опишите их биологическую роль, содержание в норме и их клинико-диагностическое значение. 354. Какие витамины крови относятся к антидерматитным? Опишите их биологическую роль, содержание в норме и их клинико-диагностическое значение. 355. Охарактеризуйте дыхательную функцию крови. Как происходит перенос кислорода и углекислого газа в организме? 356. Как происходит адаптация организма при гипоксии? 357. Опишите биологическую роль и клинико-диагностическое значение микроэлементов крови. 358. Назовите буферные системы плазмы крови и эритроцитов. 359. Опишите биологическую роль и клинико-диагностическое значение щелочного резерва и кислотной емкости крови.
Тема. Биохимия мочи
360. Охарактеризуйте химический состав мочи различных животных. 361. Опишите клинико-диагностическое значение физических свойств мочи животных. 362. Какую реакцию среды имеет моча плотоядных и травоядных животных? Назовите причины различия и их клинико-диагностическое значение. 363. Перечислите и охарактеризуйте постоянные азотистые вещества мочи. Какое клинико-диагностическое значение они имеют? 364. Опишите клинико-диагностическое значение определения мочевины в моче, содержание в норме и при патологиях. 365. Охарактеризуйте клинико-диагностическое значение определения клиренса креатинина в моче, содержание креатина и креатинина в норме и при патологиях. 366. Опишите клинико-диагностическое значение определения мочевой кислоты в моче животных, содержание в норме и при патологиях. 367. Охарактеризуйте клинико-диагностическое значение животного индикана в моче, его строение и происхождение. 368. Перечислите и охарактеризуйте постоянные безазотистые вещества мочи и их клинико-диагностическое значение. 369. Опишите и перечислите минеральные вещества мочи, их клинико-диагностическое значение. 370. Назовите и охарактеризуйте патологические компоненты мочи, их клинико-диагностическое значение. 371. Перечислите и опишите виды и причины протеинурий. 372. Опишите и перечислите виды и причины глюкозурии. Охарактеризуйте алиментарную и патологическую глюкозурию. 373. Какое клинико-диагностическое значение имеет определение кетоновых тел в моче? 374. Охарактеризуйте желчные пигменты в моче и их клинико-диагностическое значение. 375. Какое клинико-диагностическое значение имеет появление в моче крови и кровяных пигментов? Перечислите причины гемоглобинурии. 376. Охарактеризуйте осадки кислой мочи. 377. Перечислите и охарактеризуйте осадки щелочной мочи. 378. Охарактеризуйте неорганизованные осадки патологической мочи. 379. Опишите особенности химического состава мочи птиц. 380. Охарактеризуйте неспецифические лабораторные маркеры заболеваний мочевыделительной системы (бактериурия, пиурия, протеинурия, альбуминурия, кетонурия, гемоглобинурия, гематурия). 381. Какие биохимические изменения происходят при острой и хронической почечной недостаточности? Перечислите определяемые лабораторные показатели.
Тема. Биохимия яйца 392. Охарактеризуйте химический состав скорлупы яйца. 393. Охарактеризуйте химический состав яичного белка. 394. Какой химический состав имеет желток яйца? 395. Какие витамины представлены в яйце? 396. Как кормление птиц влияет на химический состав яйца и цвет желтка?
Тема. Биохимия растений 397. Дайте характеристику органических кислот в растениях. Оксибензойные и оксикоричные кислоты. 398. Дайте характеристику катехинов, лейкоантоцианов, антоцианов, флаванонов, флавонов и флавонолов растений. 399. Дайте характеристику дубильных веществ в растительной продукции. Лигнин, меланины. 400. Дайте характеристику терпеноидных соединений – мирцен, линалоол, гераниол, цитронеллол, a- и b-цитрали, ментол и карвон, лимонен, a-терпинеол, пинен, камфен, борнеол, камфора. Растительные смолы 401. Опишите строение, свойства и классификацию алкалоидов – производных пиридина и пирролидина, хинолина и изохинолина, индола, пурина, тропана, ароматических соединений. Изменение содержания алкалоидов в процессе роста и развития растений. 402. Опишите строение, свойства и классификацию гликозидов – амигдалина, пруназина, вицианина, линамарина, ванилина, глюконастурцина, арбутина, сердечных и флавоноидных гликозидов, сапонинов. Особенности строения S-гликозидов и N-гликозидов. 403. Опишите механизмы ассимиляции растениями нитратного азота и причины накопления нитратов в растительной продукции; особенности действия нитратредуктазы и нитритредуктазы. 404. Охарактеризуйте химический состав зерна злаковых культур, белки зерна; химический состав и качество клейковины пшеницы; изменение содержания углеводов, липидов, витаминов, азотистых веществ и качества клейковины при созревании зерна; биохимические процессы при послеуборочном дозревании и хранении зерна. 405. Охарактеризуйте химический состав зерна зернобобовых культур; биохимические процессы при созревании, послеуборочном дозревании и хранении. 406. Охарактеризуйте химический состав семян масличных растений; биохимические процессы при созревании, послеуборочном дозревании и хранении. 407. Назовите особенности аминокислотного и фракционного состава белков злаковых культур (на примере пшеницы) по сравнению с белками бобовых и масличных культур. 408. Охарактеризуйте химический состав клубней картофеля; изменение химического состава при созревании и хранении. 409. Охарактеризуйте химический состав корнеплодов; биохимические процессы при созревании и хранении. 410. Охарактеризуйте химический состав плодов и ягод; биохимические процессы при созревании и хранении. 411. Охарактеризуйте химический состав овощей; биохимические процессы в созревающих овощах. Что такое ферменты? а) сложные белки, являющиеся структурным материалом клетки б) биокатализаторы белковой природы в) неорганические катализаторы г) микроэлементы, повышающие скорость химических процессов Установить соответствие:
20. Биологическая роль витамина А: а) обеспечивает нормальную работу эпителия б) является антиоксидантом в) участие в построении клеточных мембран г) участие в процессах фоторецепции сумеречного зрения Содержание витамина А (ретинол, антиксерофтальмический) в молоке в мг/кг а) 0,6-12 (в молозиве) б) 1,0-1,5 в) 0,08-1,0 г) 0,02-0,05 22. Биологическая роль витамина D (кальциферол, антирахитический): а) является антиоксидантом б) регулирует процессы остеогенеза и ремоделирования костной ткани в) поддержание оптимальной концентрации ионов кальция и фосфора в плазме крови г) участие в процессах фоторецепции сумеречного зрения Содержание витамина D в молоке в мкг/кг а) 0,6-12 б) 1,0-1,5 в) 0,5-1,5 г) 0,02-0,05 24. Биологическая роль витамина Е: а) является антиоксидантом б) предотвращает гибель половых клеток в) поддержание оптимальной концентрации ионов кальция и фосфора в плазме крови г) участие в процессах фоторецепции сумеречного зрения Содержание витамина Е (токоферол, антиоксидантный, антистерильный) в молоке в мг/кг а) 0,6-12 б) 0,7-1,9 в) 0,08-1,0 г) 0,02-0,05 Установить соответствие гормоны синтезируются в железе 1) тироксин а) щитовидной 2) пролактин б) гипофизе 3) соматотропин (СТГ) в) семенниках 4) альдостерон г) поджелудочной 5) андрогены д) коре надпочечников В период лактации показан а) липокаин б) альдостерон в) пролактин г) АКТГ
Зарастанию ран способствует а) дофамин б) кальцитонин в) альдостерон г) кортизол
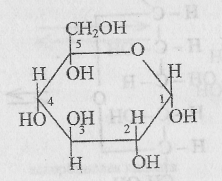
6. Для лечения тяжелых форм гипогликемии применяют а) инсулин б) альдостерон в) глюкагон г) СТГ Назвать углевод
Фруктоза входит в состав а) мальтозы б) сахарозы в) лактозы г) трегалозы 4. При гидролизе сахаразы образуются а) два остатка глюкозы б) глюкоза и галактоза в) глюкоза и фруктоза г) глюкоза и манноза Установить соответствие Кислота Название НООС-(СНОН)4-СООН а) глюкуроновая О=СН- (СНОН)4-СООН б) глюконовая СН2ОН-(СНОН)4- НООС в) глюкаровая Назвать углевод
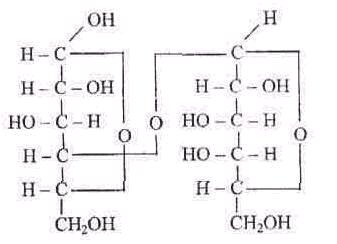
Назвать углевод
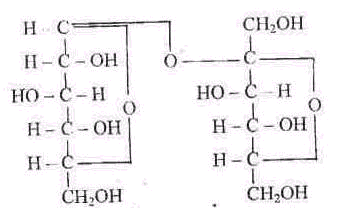
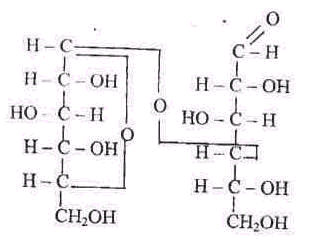
Назвать углевод
11. При полном гидролизе целлюлозы образует ся а) глюкоза б) галактоза в) фруктоза 12. Какие углеводы содержат 1-4 –гликозидные связи, соединяющие остатки глюкозы а) крахмал б) клетчатка г) гликоген в) мальтоза Состояние лактозы в молоке а) коллоидный раствор б) эмульсия или суспензия в) молекулярно-дисперсное г) эмульсия Основной углевод мышц:
Установить соответствие Кислота число атомов углерода: : число двойных связей в радикале 1) стеариновая а) 18:1 2) линолевая б) 16:0 3) олеиновая в) 18:3 4) линоленовая г) 18:2 5) пальмитиновая д) 18:0 Назвать триглицерид СН2-О-СО-(СН2)14-СН3 │ СН- О-СО-(СН2)7-СН=СН-(СН2)7-СН3 │ СН2-О-СО-(СН2)7-СН=СН-СН2-СН=СН-(СН2)4-СН3 а) 1-стеаро-2-олеино-3-линолен б) 1-меристено-2-линоло-3-олеин в) 1-пальмито-2-нервоно-3-линилен г) 1-пальмито-2-олеино-3-линолен Йодное число пищевых масел а) 140-180 б) 20-40 в) 90-130 г) 50-70 26. При каких значениях кислотного числа (в г КОН на 1 г жира) свойства масла ухудшаются и его нельзя использовать на пищевые цели а) 2 б) 5 в) 10 г) 15 В процессе созревания семян а) усиливается синтез насыщенных кислот б) усиливается синтез ненасыщенных кислот в) меняется соотношение высших жирных кислот в зависимости от культуры г) соотношение высших жирных кислот не изменяется Назовите данный трипептид
NН2- СН - С - NН - СН - С - NН - СН - СООН | || │ || |
а) лизил- аланил-тирозин б) аланин- тирозил-лизин в) тирозин- лизин-аланин г) тирозил-аланил-лизин 4. Какие продукты образуются при гидролизе данного вещества под действием карбоксипептидазы NН2- СН - С- NН - СН - С - NН - СН - СООН | || │ || |
а) серин, валилметионин б) метионин, валилсерин в) метионин, серилвалин г) серилгистидин, цистеин
5. В состав сухого вещества коровьего молока входит белков а) 1,1-1,8% б) 2,2-2,5% в) 2,7-3,7% г) 4,5-6% Казеин является белком а) полноценным б) неполноценным 11. Казеин может связывать большое количество воды (около 3,7 г на 1 г белка) за счет а) неполярных групп на поверхности казеиновых мицелл б) наличия в пептидных цепях остатков фенилаланина и триптофана в) того, что все виды казеина (α, β, λ) соединены между собой ионами Са++ г) полярных групп (-NH2,-COOH,-OH и др.) на поверхности и внутри казеиновых молекул Сывороточные белки являются а) полноценными б) неполноценными Актин является белком а) тонких филаментов поперечнополосатых мышц б) толстых филаментов поперечнополосатых мышц Комплекс актомиозина: а) обладает АТФ-азной активностью, стимулируемой ионами магния б) обладает АТФ-азной активностью, стимулируемой ионами натрия в) не обладает АТФ-азной активностью г) осуществляет обратимое связывание О₂ и СО₂; Тропомиозин с тропонином а) обладают АТФ-азной активностью б) осуществляют мембранный транспорт катионов в) обеспечивают энергией процесс мышечного сокращения г) участвуют в регуляции взаимодействия актина с миозином; Вся клейковина содержится в а) эндосперме б) зародыше в) покровных оболочках г) алейроновом слое Ситуационные задачи
1. Известно, что употребление в пищу сырых яиц может вызвать гиповитаминоз витамина Н. В составе яиц содержится белок авидин, который способен взаимодействовать с витамином Н и препятствовать его всасыванию в желудочно-кишечном тракте. Объясните, почему вареные яйца таким эффектом не обладают?
2. При длительном приеме антибиотиков или сульфаниламидных препаратов у животного может развиться гиповитаминоз витамина В6. Чем это может быть обусловлено? 3. Соли тяжелых металлов токсичны для живых организмов. Объясните механизм токсического действия данной группы соединений. В качестве первой помощи при отравлении солями тяжелых металлов пострадавшему можно дать выпить сырой яичный белок. Обоснуйте целесообразность таких действий. 4. Витамины А и D можно применять сразу за один прием в таком количестве, которого достаточно для поддержания их уровня в течение нескольких недель, витамины же группы В необходимо принимать значительно чаще. Почему? 5. Объясните, почему при интенсивной физической нагрузки у лошади активируется скорость реакций цитратного цикла? Напишите реакции, скорость которых при этом возрастает. Объясните почему? 6. Непосредственно в реакциях цикла Кребса кислород не участвует, но он является аэробным процессом. Объясните, почему он ингибируется в отсутствии кислорода? 7. При дефиците витаминов группы В возможно снижение процесса окислительного декарбоксилирования пирувата. Объясните причину этого снижения. Напишите суммарную реакцию окислительного декарбокислирования пирувата, заполните таблицу:
8. В физиологических условиях температура животного выше температуры окружающей среды. Объясните, какими биохимическими процессами обусловлена эта разница? Какую роль в этом играют митохондрии? Ответ обоснуйте. 9. При увеличении концентрации АДФ в клетке скорость цикла трикарбоновых кислот быстро увеличивается. Увеличение активности какого фермента (ферментов) приводит к ускорению реакций всего цикла? Каков механизм активирующего эффекта избытка АДФ? 10. У животного с повышенной функцией щитовидной железы наблюдается уменьшение веса, субфебрильная температура, по
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 195; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.193.166 (0.014 с.) |