Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Рефрактометрическое определение концентрации спиртаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
В водно-спиртовых растворах при содержании спирта до 60 % наблюдается линейная зависимость между показателем преломления и концентрацией. При установлении крепости спирта в более концентрированных растворах их приходится разбавлять. Это разведение учитывают при расчетах. Определение необходимо проводить при температуре 20°С. На призму рефрактометра наносят 5-7 капель водно-спиртовой смеси и немедленно измеряют величину показателя преломления, чтобы избежать ошибок, связанных с летучестью спирта. Если определение проводят не при t=20°C, то следует вносить поправки на температуру. Величина поправки на 1 °С приведена в таблице «Показатели преломления спирто-водных растворов, концентрация которых выражена в об.%». Эта поправка прибавляется, если температура выше 20°С, и вычитается, если меньше. Пример: Анализ 40% спирта проводится при 23°С. Показание рефрактометра— 1,3541. Согласно таблице, поправка на 1 °С для показателя преломления, близкого к полученному (1,35500), равна 0,24 * 10-4, т.е. 0,00024. Поскольку исследование проводилось при 23°С, то поправка будет составлять 0,00024 • 3 = 0,00072. Показатель преломления, приведенный к 20°С, равен: 1,3541 + 0,00072 = 1,35482 По таблице определяем соответствующую данному показателю преломления концентрацию спирта. Найденной величины показателя преломления (1,35482) в таблице нет. Близкому по величине показателю преломления 1,35500 соответствует 40% спирта. Необходимо определить, какая концентрация спирта соответствует разности показателей преломления: 1,35500 - 1,35482 = 0,00018. Поправка на 1% спирта равна 4,0 • 10"4, т.е. 0,0004. Следовательно: 0,00018: 0,0004 = 0,45% Истинное содержание спирта в исследуемом растворе равно: 40% - 0.45% = 39,55% По ГФ X в 40% спирте содержание последнего может колебаться в пределах 39,5% - 40,5%. Определите концентрацию этилового спирта в водно-спиртовом растворе другими способами: • С помощью спиртометра. • С помощью ареометра установите плотность раствора и найдите концентрацию спирта по алкоголеметрическим таблицам ГФ XI, соответствующую данной плотности. Сравните полученные результаты. Сделайте выводы. Составьте самостоятельно алгоритм внутриаптечного контроля спирта этилового при разведении в аптеке.
ЗАНЯТИЕ 2 АЛЬДЕГИДЫ. УГЛЕВОДЫ. ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ ПРОСТЫХ ПОРОШКОВ ГЕКСАМЕТИЛЕНТЕТРАМИНА Задачи • Коррекция и совершенствование знаний по теме «Альдегиды», «Углеводы». • Освоить обязательные и выборочные виды внутриаптечного контроля простых разделенных порошков. • Освоить химический контроль гексаметилентетрамина. • Совершенствовать навыки расчетов содержания лекарственного вещества и ориентировочного объема титранта. • Совершенствовать навыки оформления результатов анализа. Продолжительность занятия 2 академических часа (90 минут). Вопросы для самоподготовки • Связь между химическим строением альдегидов и их действием на организм. Русские, латинские, химические названия, способы получения, свойс тва, подлинность, испытания на чистоту, количественное определение, применение, хранение и отпуск лекарственных препаратов: раствора формальдегида, гексаметилентетрамина, глюкозы. • Специфические показатели качества порошков. • Обязательные и выборочные виды внутриаптечного контроля порошков. Алгоритм внутриаптечного контроля. • Химический контроль гексаметилентетрамина. Почему фармакопейные реакции подлинности и количественного определения не используют во внугриаптечном контроле? Материальное обеспечение Реактивы: • кислота серная разведенная; • кислота серная концентрированная; • кислота салициловая; • раствор едкого натра. Титрованные растворы и индикаторы: • 0,1 моль/л раса вор кислоты хлористоводородной; • мегиловый оранжевый; • мешленовый синий.
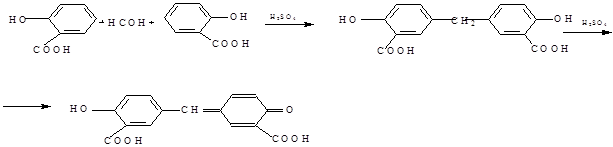
Посуда, приборы, оборудование: • титровальная установка; • ручные весочки; • водяная баня; • фарфоровая чашка; • пробирки; • склянка для титрования. Rp: Hexamethylentetramini 0,25 D.t.d. №12 S.по 1 порошку 3 раза в день Белый однородный порошок без запаха, жгучего, сладковатого, затем Подлинность • Кислотный гидролиз и доказательство составных частей При нагревании с разведенной серной кислотой выделяется формаль- (CH,)6N4+ 2H2S04+ 6Н,0 -> 6НСO + 2(NH4)2S04 Затем добавляют избыток щелочи и снова нагревают. Появляется за- (NH4)2S04+ 2NaOH ->Na2S04+ 2NH3+ 2Н20 Во внутриаптечном контроле обычно ограничиваются первым эффек- • Реакция образования ауринового красителя При нагревании препарата с концентрированной серной и салицило- (CH2)6N4+ 2H2S04+ 6Н20 -» 6НСO+ 2(NH4)2S04
ауриновый краситель Количественное определение Метод нейтрализации. Прямое титрование. 0,05 препарата растворяют в 1 мл воды и титруют 0,1 моль/л раствором хлористоводородной кислоты в присутствии смешанного индикатора (2 капли метилового оранжевого и 1 капля метиленового синего) до перехода зеленого окрашивания в фиолетовое. (CH2)6N4+ НС1 ->(CH2)6N4* НС1 1 мл 0,1 моль/л раствора НС1 соответствует 0,014 г гексаметилентетрамина Vориент = m = 0,05 =3,57 ml T 0,014 где: m - минимальная навеска, взятая на титрование Т - титр рабочего раствора по определяемому веществу
m = V*K*T*A нав.
А— масса одного порошка (одной дозы) нав. - минимальная навеска, равная 0,05 V - объём титранта, фактически пошедший на титрование
доп. откл =?
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 3286; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.139.235.100 (0.006 с.) |