Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основы теории химической связиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
ОСНОВЫ ТЕОРИИ ХИМИЧЕСКОЙ СВЯЗИ Совокупность сил, удерживающих атомы в молекулах простых и сложных веществ, называется химической связью. Протекание химических реакций обусловлено разрывом старых и образованием новых связей. Согласно современным представлениям химическая связь образуется за счет перекрывания электронных облаков взаимодействующих атомов, при этом происходит перераспределение электронной плотности. В зависимости от характера распределения электронной плотности различают три основных типа химической связи: ковалентную, ионную и металлическую. Общие свойства химической связи Энергия связи Е, кДж/моль – энергия, которая выделяется при образовании химической связи, или которую нужно затратить для разрыва связи. Например, энергии связей в молекулах водорода, кислорода и азота составляют: H + H = H2 + 435кДж/моль Есв(О2) = 493кДж/моль, Есв(N2) = 945кДж/моль Длина lсв, Ả - расстояние между ядрами взаимодействующих атомов. Поскольку происходит перекрывание электронных облаков, то длина связи меньше суммы радиусов взаимодействующих атомов: lA-B < rA + rB Например rH = 0,53Ả, lH-H = 0,74Ả Полярность связи. При образовании связи возможны три случая: 1) связь образуется двумя одинаковыми атомами (∆æ=0). В этом случае электронная плотность поровну распределена между связывающимися атомами. Возникает неполярная ковалентная связь; 2) связь образуется двумя атомами со слабо отличающимися электроотрицательностями (∆æ<1,5). Возникает полярная ковалентная связь (диполь); 3) связь образуют два атома с резко различающимися электро-отрицательностями (∆æ>1,5). Возникает ионная связь. Примеры.
Отметим, что деление связей на ковалентные неполярные, ковалентные полярные и ионные во многом условно, поскольку не существует резкой границы между этими типами связи. Можно говорить о ковалентной связи с некоторой долей ионности, о преобладании доли ионной связи и т.д. Идеальная ковалентная связь существует лишь в частицах, состоящих из одинаковых атомов (Н2, N2 и т.д.). Если образуется связь между различными атомами, то электронная плотность смещается к одному из ядер атомов, то есть происходит поляризация связи. Смещение электронной плотности облака в направлении одного из партнеров по связи приводит к асимметрии центров положительных и отрицательных сил, расстояние между которыми l, называемое длиной диполя связи, служит мерой ее полярности. Длина диполя, а следовательно и полярность связи зависит от разности электроотрицательностей ∆æ взаимодействующих атомов lдип =f·(∆æ). Полярность связи обычно выражают при помощи ее дипольного момента µ, представляющего собой произведение длины диполя lдип на величину заряда электрона q, выраженного в абсолютных электростатических единицах (q = 4,80 • 10-10 абс. эл.-ст. ед.). Так как длина диполя lдип имеет порядок атомных размеров, т. е. 10-8 см, то дипольный момент связи µсв= lдип·q, характеризуется величиной порядка 10-18 и размерностью абс. эл.-ст. ед. • см. Для удобства пользования дипольными моментами величину 10-18 называют Дебаем и обозначают буквой D. Так, если длина диполя связи НСl равна l = 0,216 • 10-8 см, то дипольный момент ее равен: µ = 0,216 • 10-8 • 4,80 • 10-10 = 1,04 • 10-8 эл.-ст. ед. • см = 1,04 D. В системе СИ дипольный момент имеет размерность кулон-метр. Переход от одной размерности к другой может быть сделан исходя из следующих соображений: заряд электрона составляет 4,80 • 10-10 абс. эл.-ст. ед. = 1,6 • 10-19 Кл и, следовательно:
1 D = 1 • 10-10 абс. эл.-ст. ед. • 10-8 см = 0,33 • 10-19 • 10-10 = 0,33 • 10-29 Кл • м В зависимости от полярности связи условно считаются: ковалентной полярной, если µсв <4Д и ионной, если µсв = 4 – 11Д. Эффективный заряд атома. В результате перераспределения электронной плотности на атомах возникает некоторый заряд, который называют эффективным зарядом атомов в молекуле. В настоящее время неизвестны соединения, в которых эффективный заряд был бы больше двух. Для одного и того же атома, чем выше валентность, тем меньше эффективный заряд, т.е. больше доля ковалентной связи. Ниже представлены эффективные заряды атомов в некоторых молекулах: H+0,17Cl-0,17 Zn+0,86S-0,86 Na+0,8Cl-0,8 Эти молекулы полярны. Их можно рассматривать как системы, состоящие из двух равных по абсолютной величине, но противоположных по знаку зарядов, расположенных на определенном расстоянии друг от друга. Такие системы называются электрическими диполями. Теория ковалентной связи Для объяснения образования ковалентной связи применяют два приближенных метода расчета систем, состоящих из ядер и электронов: - метод валентных связей (ВС), - метод молекулярных орбиталей. Рассмотрим метод валентных связей (локализованных электронных пар). Ионная связь. Свойства ионной связи. Электроны в ионных соединениях в высшей степени локализованы, т.е. принадлежат одному из атомов. В отличие от ковалентной связи ионная связь ненаправлена, так как силовое поле ионов равномерно распределяется во всех направлениях. Ионная связь теоретически ненасыщаема, так как энергетически выгодно, когда каждый ион окружен максимальным числом ионов противоположного знака. Однако из-за отталкивания одноименных ионов устойчивость системы достигается лишь при определенной взаимной координации ионов, характеризуемой координационным числом. При нормальных условиях ионные соединения представляют собою кристаллические вещества. В узлах кристаллической решетки ионных соединений в определенной последовательности чередуются катионы и анионы. Каждый катион оказывается окруженным определенным количеством анионов и наоборот.
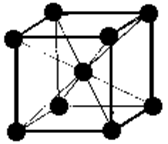
Рис. 18 Структура кристаллов NaCl и CsCl
Рис. 19 Взаимная координация ионов в кристаллах NaCl (а) и CsCl (б) Следует заметить, однако, что вследствие волновой природы электрона полное разделение зарядов невозможно. Поэтому даже в таком ионном соединении, как СsF, доля ионной связи составляет 96%. Большую роль играет и поляризация ионов, благодаря чему связь становится менее полярной. При стандартных условиях соединения с ионными связями существуют в виде твердых кристаллических тел. В ионных кристаллах нет отдельных молекул. В растворах ионных соединений нет молекул. При растворении в полярных растворителях (вода, спирты и т.п.) ионные соединения полностью диссоциируют, а в неполярных (СС l 4, С6Н6 и т.п.) – они обычно нерастворимы. Ионные молекулы можно обнаружить только в парах ионных соединений, при этом помимо молекул в парах обнаруживаются различные частицы – ассоциаты из нескольких молекул, а также простые и сложные ионы. Например, в парах хлорида натрия кроме молекул NаС l присутствуют такие частицы: (NаС l)2, (NаС l)3, Nа2С l +, NаС l2 –. Соединения с ионными кристаллическими решетками имеют высокие температуры плавления и кипения. Многие ионные кристаллы относятся к классу диэлектриков. При стандартных условиях их электропроводность на десятки порядков ниже, чем у металлов. С ростом температуры наблюдается увеличение электропроводности. Металлическая связь. Некоторые свойства металлов, такие, например, как высокая тепло- и электропроводность, ковкость, способность образовывать кристаллические решетки с высокими координационными числами (8, 12) дают основание заключить, что электроны в металле не связаны с какими-либо конкретными атомами, а перемещаются по всей конденсированной фазе достаточно свободно, что обусловливает их высокие тепло- и электропроводность. Наличие делокализованных электронов связано с ненаправленным характером химических связей, поэтому атомы металлов легко перемещаются из одного равновесного положения в другое, что обусловливает ковкость этих веществ. В металлах, очевидно, небольшое число электронов одновременно связывает большое число ядер.
Таким образом, химическая связь в металлах не локализована и не направлена. Металл можно рассматривать как плотно упакованную структуру из катионов, связанных друг с другом «электронным газом».
ОСНОВЫ ТЕОРИИ ХИМИЧЕСКОЙ СВЯЗИ Совокупность сил, удерживающих атомы в молекулах простых и сложных веществ, называется химической связью. Протекание химических реакций обусловлено разрывом старых и образованием новых связей. Согласно современным представлениям химическая связь образуется за счет перекрывания электронных облаков взаимодействующих атомов, при этом происходит перераспределение электронной плотности. В зависимости от характера распределения электронной плотности различают три основных типа химической связи: ковалентную, ионную и металлическую.
|
||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 913; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.253.21 (0.007 с.) |


 ;
;