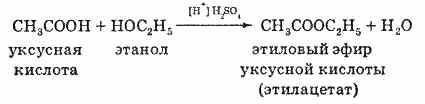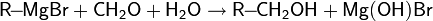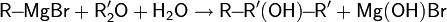Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химические свойства алкинов.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Химические свойства алкинов.
Химические свойства алкинов объясняет наличие тройной связи в молекуле алкина. Типичная реакция для алкинов – реакция присоединения, которая протекает в 2 стадии. На первой происходит присоединение и образование двойной связи, а на второй – присоединение к двойной связи. Реакция у алкинов протекает медленнее, чем и алкенов, т.к. электронная плотность тройной связи «размазана» более компактно, чем у алкенов, и поэтому менее доступна для реагентов. 1. Галогенирование. Галогены присоединяются к алкинам в 2 стадии. Например,
А суммарно:
Алкины также как алкены обесцвечивают бромную воду, поэтому эта реакция является качественной и для алкинов. 2. Гидрогалогенирование. Галогенводороды присоединяются к тройной связи несколько тружднее, чем к двойной. Для ускорения (активации) процесса используют сильную кислоту Льюиса – AlCl3. Из ацетилена при таких условиях модно получить винилхлорид, который идет на производства полимера – поливинилхлорида, имеющего важнейшее значение в промышлености:
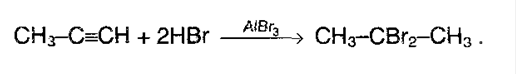
Если же галогенводород в избытке, то реакция (особенно у несимметричных алкинов) идет по правилу Марковникова:
3. Гидратация (присоединение воды). Реакция протекает только в присутствии солей ртути (II) в качестве катализатора:
На 1ой стадии образуется непредельный спирт, в котором гидроксигруппа находится у атома углерода, образующего двойную связь. Такие спирты называются виниловыми или фенолами. Отличительная черта таких спиртов – неустойчивость. Они изомеризуются в более стабильные карбонильные соединения (альдегиды и кетоны) вследствие переноса протона от ОН -группы к углероду при двойной связи. При этом π -связь рвется (между атомами углерода), и образуется новая π -связь между атомомами углерода и атомом кислорода. Такая изомеризация происходит из-за большей плотности двойной связи С=О по сравнению с С=С. Только ацетилен превращается в альдегид, его гомологи - в кетоны. Реакция протекает по правила Марковникова:
Эта реакция носит названия – реакции Кучерова. 4. Те алкины, которые имеют концевую тройную связь, могут отщеплять протон под действием сильных кислотных реагентов. Такой процесс обусловлен сильной поляризацией связи
Причиной поляризации служит сильная электроотрицательность атома углерода в sp -гибридизации, поэтому алкины могут образовывать соли – ацетилениды:
Ацетилениды меди и серебра легко образуются и выпадают в осадок (при пропускании ацетилена через аммиачный раствор оксидасеребра или хлорида меди). Эти реакции являются качественными на концевую тройную связь:
Полученные соли легко разлагаются под действием HCl, в результате выделяется исходный алкин:
Поэтому алкины легко выделить из смеси других углеводородоров. 5. Полимеризация. При участии катализаторов алкины могут реагировать друг с другом, причем в зависимости от условий, могут образовываться различные продукты. Например, под воздействием хлорида меди (I) и хлорида аммония:
Винилацетилен (полученное соединение) присоединяет хлороводород, образуя хлорпрен, который служит сырьем для получения синтетического каучука:
6. Если ацетилен пропускать через уголь при 600 ºС, получают ароматическое соединение – бензол. Из гомологов ацетилена, получают гомологи бензола:
7. Реакция окисления и восстановления. Алкины легко окисляются перманганатом калия. Раствор обесцвечивается, т.к. в исходном соединении есть тройная связь. При окислении происходит расщепление тройной связи с образованием карбоновой кислоты: В присутствие металлических катализаторов происходит восстановление водородом:
Вопрос 8 Химические свойства Химические свойства альдегидов и кетонов в значительной степени обусловлены наличием в их молекулах сильно полярной карбонильной группы (связь 1. Горение: 2CH3CHO + 5O2 2. Присоединение (по двойной связи карбонильной группы). Из альдегидов при этом получаются первичные спирты, а из кетонов - вторичные. 3. Окисление: CH3CHO + Ag2O
4. Замещение атомов водорода в углеводородном радикале (замещение происходит в
Примеры реакций, характеризующие химические свойства спиртов. Это очень разнообразный и обширный класс химических соединений. В зависимости от количества групп –OH в молекуле, он подразделяется на одно-, двух- трехатомные и так далее — многоатомные соединения. Химические свойства спиртов зависят также от содержания оксигрупп групп в молекуле. Эти вещества являются нейтральными и не диссоциируют на ионы в воде, как, например, сильные кислоты или сильные основания. Однако могут слабо проявлять как кислотные (снижаются с увеличением в ряду спиртов молекулярной массы и разветвленности углеводородной цепи), так и основные (растут с увеличением молекулярной массы и разветвленности молекулы) свойства. Несколько основных реакций, которые характеризуют химические свойства спиртов: 1) При взаимодействии со щелочными металлами или их гидроокисями (реакция депротонирования) образуются алкоголяты (атом водорода замещается на атом металла), в зависимости от углеводородного радикала получаются метилаты, этилаты, пропилаты и так далее, например, пропилат натрия: 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑. 2. При взаимодействии с концентрированными галогенводородными кислотами образуются галогенпроизводные углеводородов: HBr + CH3CH2OH ↔ CH3CH2Br + H2O. Эта реакция является обратимой. В результате происходит нуклеофильное замещение ионом галогена гидроксильной группы. 3. Спирты могут окисляться до диоксида углерода, до альдегидов или до кетонов. Спирты горят в присутствии кислорода: 3O2 + C2H5OH →2CO2 + 3H2O.Под действием сильного окислителя (хромовая кислота, перманганат калия и так далее) первичные спирты преобразуются в альдегиды: C2H5OH → CH3COH + H2O, а вторичные — в кетоны: CH3—(CHOH)—CH3 → CH3—(CHO)—CH3 + H2O. 4. Реакция дегидратации протекае т при нагревании в присутствии водоотнимающих веществ (хлорид цинка, серная кислота и так далее). В результате образуются алкены: C2H5OH → CH2=CH2 + H2O. 5. Реакция этерификации протекает также при нагревании в присутствии водоотнимающих соединений, но, в отличие от предыдущей реакции, при более низкой температуре и с образованием простых эфиров: 2C2H5OH → C2H5—O—C2H5O. С серной кислотой реакция происходит в две стадии. Сначала образуется эфир кислоты серной: C2H5OH + H2SO4 → C2H5O—SO2OH + H2O, затем при нагревании до 140 °С и в избытке спирта образуется диэтиловый (его часто называют серный) эфир: C2H5OH + C2H5O—SO2OH → C2H5—O—C2H5O + H2SO4 Химические свойства спиртов зависят от вида и пространственного расположения атомов: молекулы бывают с изомерией цепи и изомерией положения. В зависимости от максимального количества одинарных связей углеродного атома (связанного с оксигруппой) с другими атомами углерода (с 1-м, 2-мя или 3-мя) различают первичные (нормальные), вторичные или третичные спирты. У первичных спиртов гидроксильная группа присоединена к первичному углеродному атому. У вторичных и третичных — ко вторичному и третичному соответственно. Начиная с пропанола, появляются изомеры, которые отличаются положением гидроксильной группы: пропиловый спирт C3H7—OH и изопропиловый спирт CH3—(CHOH)—CH3.
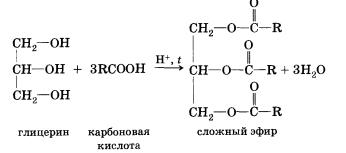
Химические свойства многоатомных спиртов, по аналогии с их физическими свойствами, зависят от типа углеводородного радикала, образующего молекулу, и, конечно, количества гидроксильных групп в ней. Например, этиленгликоль CH3OH—CH3OH (температура кипения 197 °С), являющийся 2-х атомным спиртом, представляет собой жидкость бесцветную (имеет сладковатый вкус), которая смешивается с H2O, а также низшими спиртами в любых соотношениях. Этиленгликоль, как и его высшие гомологи, вступают во все реакции, характерные для одноатомных спиртов. Глицерин CH2OH—CHOH—CH2OH (температура кипения 290 °С) является простейшим представителем 3-х атомных спиртов. Это густая сладкая на вкус жидкость, которая тяжелее воды, но смешивается с ней в любых соотношениях. Растворяется в спирте. Для глицерина и его гомологов также характерны все реакции одноатомных спиртов. Химические свойства 1. Диссоциация с образованием катионов водорода и анионов кислотного остатка. Более точно этот процесс описывает уравнение, учитывающее участие в нем молекул воды. Равновесие диссоциации карбоновых кислот смещено влево, подавляющее большинство их — слабые электролиты. Очевидно, что присутствием в молекулах карбоновых кислот «кислого» водорода, т. е. водорода карбоксильной группы, обусловлены и другие характерные свойства. 2. Взаимодействие с металлами, стоящими в электрохимическом ряду напряжений до водорода. Так, железо восстанавливает водород из уксусной кислоты: 2СН3—СООН + Fe —> (CHgCOO)2Fe + Н2 3. Взаимодействие с основными оксидами с образованием соли и воды: 2R—СООН + СаО —> (R—СОО)2Са + Н20 4. Взаимодействие с гидроксидами металлов с образованием соли и воды (реакция нейтрализации): R—СООН + NaOH —> R—COONa + Н20 3R—СООН + Са(ОН)2 —> (R—СОО)2Са + 2Н20 5. Взаимодействие с солями более слабых кислот, с образованием последних. Так, уксусная кислота вытесняет стеариновую из стеарата натрия и угольную из карбоната калия. 6. Взаимодействие карбоновых кислот со спиртами с образованием сложных эфиров — уже известная вам реакция эте-рификации (одна из наиболее важных реакций, характерных для карбоновых кислот). Взаимодействие карбоновых кислот со спиртами катализируется катионами водорода. Реакция этерификации обратима. Равновесие смещается в сторону образования сложного эфира в присутствии водоотни-мающих средств и удалении эфира из реакционной смеси.
В реакции, обратной этерификации, которая называется гидролизом сложного эфира (взаимодействие сложного эфира с водой), образуются кислота и спирт. Очевидно, что реагировать с карбоновыми кислотами, т. е. вступать в реакцию этерификации, могут и многоатомные спирты, например глицерин: Dсе карбоновые кислоты (кроме муравьиной) наряду с карбоксильной группой содержат в молекулах углеводородный остаток. Безусловно, это не может не сказаться на свойствах кислот, которые определяются характером углеводородного остатка. 7. Реакции присоединения по кратной связи — в них вступают непредельные карбоновые кислоты; например, реакция присоединения водорода —гидрирование. При гидрировании олеиновой кислоты образуется предельная стеариновая кислота. Непредельные карбоновые кислоты, как и другие ненасыщенные соединения, присоединяют галогены по двойной связи. Так, например, акриловая кислота обесцвечивает бромную воду. 8. Реакции замещения (с галогенами) — в нее способны вступать предельные карбоновые кислоты; например, при взаимодействии уксусной кислоты с хлором могут быть получены различные хлорпроизводные кислоты:
При галогенировании карбоновых кислот, содержащих более одного атома углерода в углеводородном остатке, возможно образование продуктов с различным положением галогена в молекуле. При протекании реакции по свободнорадикальному механизму могут замещаться любые атомы водорода в углеводородном остатке. Если же реакцию проводить в присутствии небольших количеств красного фосфора, то она идет селективно — водород замещается лишь в а -положении (у ближайшего к функциональной группе атома углерода) в молекуле кислоты. Причины такой селективности вы узнаете при изучении химии в высшем учебном заведении. Карбоновые кислоты образуют различные функциональные производные при замещении гидроксильной группы. При гидролизе этих производных из них вновь образуется карбоновая кислота. Хлорангидрид карбоновой кислоты можно получить действием на кислоту хлорида фосфора(ІІІ) или тионилхлорида (SОСl2). Ангидриды карбоновых кислот получают взаимодействием хлор-ангидридов с солями карбоновых кислот. Сложные эфиры образуются в результате этерификации карбоновых кислот спиртами. Этерификация катализируется неорганическими кислотами. Эту реакцию инициирует протонирование карбоксильной группы — взаимодействие катиона водорода (протона) с неподеленной электронной парой атома кислорода. Протонирование карбоксильной группы влечет за собой увеличение положительного заряда на атоме углерода в ней:
Физические свойства Если число атомов углерода в цепи не превышает пяти, то это резко пахнущие, подвижные и летучие жидкости. Выше пяти - тяжелые маслянистые вещества, еще больше - твердые, парафинообразные. Плотность первых двух представителей превышает единицу. Все остальные легче воды. Температура кипения: чем больше цепь, тем выше показатель. Чем более разветвленная структура, тем ниже. Температура плавления: зависит от четности количества атомов углерода в цепи. У четных она выше, у нечетных ниже.
В воде растворяются очень хорошо. Способны образовывать прочные водородные связи Типы гибридизации
26.Напишите реакции подтверждающие кислотные и основные свойства спирта. 1. Спирты реагируют с щелочными и щелочноземельными металлами, при этом образуется алкоксид металла и водород. Например, реакция этанола с натрием идет значительно медленнее, чем реакция натрия с водой:
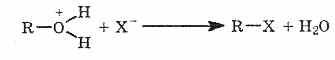
С сильными кислотами Льюиса спирты ведут себя подобно основаниям, образуя донорно-акцепторные комплексы
3. Ангидриды и хлорангидриды карбоновых кислот со спиртами образуют сложные эфиры.
Основные свойства спиртов. 1. Спирты — слабые основания. При взаимодействии с кислотами спирты могут протонироваться за счет образования донорно-акцепторной связи.
С галогеноводородами Первичные и вторичные спирты реагируют с галогенводородами по механизму SN2:
Для третичных спиртов характерен механизм SN1:
Химические свойства алкинов.
Химические свойства алкинов объясняет наличие тройной связи в молекуле алкина. Типичная реакция для алкинов – реакция присоединения, которая протекает в 2 стадии. На первой происходит присоединение и образование двойной связи, а на второй – присоединение к двойной связи. Реакция у алкинов протекает медленнее, чем и алкенов, т.к. электронная плотность тройной связи «размазана» более компактно, чем у алкенов, и поэтому менее доступна для реагентов. 1. Галогенирование. Галогены присоединяются к алкинам в 2 стадии. Например,
А суммарно:
Алкины также как алкены обесцвечивают бромную воду, поэтому эта реакция является качественной и для алкинов. 2. Гидрогалогенирование. Галогенводороды присоединяются к тройной связи несколько тружднее, чем к двойной. Для ускорения (активации) процесса используют сильную кислоту Льюиса – AlCl3. Из ацетилена при таких условиях модно получить винилхлорид, который идет на производства полимера – поливинилхлорида, имеющего важнейшее значение в промышлености:
Если же галогенводород в избытке, то реакция (особенно у несимметричных алкинов) идет по правилу Марковникова:
3. Гидратация (присоединение воды). Реакция протекает только в присутствии солей ртути (II) в качестве катализатора:
На 1ой стадии образуется непредельный спирт, в котором гидроксигруппа находится у атома углерода, образующего двойную связь. Такие спирты называются виниловыми или фенолами. Отличительная черта таких спиртов – неустойчивость. Они изомеризуются в более стабильные карбонильные соединения (альдегиды и кетоны) вследствие переноса протона от ОН -группы к углероду при двойной связи. При этом π -связь рвется (между атомами углерода), и образуется новая π -связь между атомомами углерода и атомом кислорода. Такая изомеризация происходит из-за большей плотности двойной связи С=О по сравнению с С=С. Только ацетилен превращается в альдегид, его гомологи - в кетоны. Реакция протекает по правила Марковникова:
Эта реакция носит названия – реакции Кучерова. 4. Те алкины, которые имеют концевую тройную связь, могут отщеплять протон под действием сильных кислотных реагентов. Такой процесс обусловлен сильной поляризацией связи Причиной поляризации служит сильная электроотрицательность атома углерода в sp -гибридизации, поэтому алкины могут образовывать соли – ацетилениды:
Ацетилениды меди и серебра легко образуются и выпадают в осадок (при пропускании ацетилена через аммиачный раствор оксидасеребра или хлорида меди). Эти реакции являются качественными на концевую тройную связь:
Полученные соли легко разлагаются под действием HCl, в результате выделяется исходный алкин:
Поэтому алкины легко выделить из смеси других углеводородоров. 5. Полимеризация. При участии катализаторов алкины могут реагировать друг с другом, причем в зависимости от условий, могут образовываться различные продукты. Например, под воздействием хлорида меди (I) и хлорида аммония:
Винилацетилен (полученное соединение) присоединяет хлороводород, образуя хлорпрен, который служит сырьем для получения синтетического каучука:
6. Если ацетилен пропускать через уголь при 600 ºС, получают ароматическое соединение – бензол. Из гомологов ацетилена, получают гомологи бензола:
7. Реакция окисления и восстановления. Алкины легко окисляются перманганатом калия. Раствор обесцвечивается, т.к. в исходном соединении есть тройная связь. При окислении происходит расщепление тройной связи с образованием карбоновой кислоты: В присутствие металлических катализаторов происходит восстановление водородом:
Вопрос 8
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 478; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.253.21 (0.015 с.) |



 .
.


 .
.








 поляризована в сторону атома кислорода). Чем больше частичный заряд (
поляризована в сторону атома кислорода). Чем больше частичный заряд ( +) на атоме углерода этой группы, тем выше активность соединения.
+) на атоме углерода этой группы, тем выше активность соединения. 4CO2 + 4H2O
4CO2 + 4H2O CH3OH
CH3OH 2Ag
2Ag  + CH3COOH (реакция "серебряного зеркала" - качественная реакция)
+ CH3COOH (реакция "серебряного зеркала" - качественная реакция) -положение, т. е. замещается атом водорода у 2-го атома углерода):
-положение, т. е. замещается атом водорода у 2-го атома углерода):