
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Реакции присоединения и окисленияСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Реакции присоединения бензола протекают в жестких условиях, так как сопровождаются нарушением ароматических свойств молекулы. Гидрирование бензола протекает в присутствии катализатора (Ni, Pd или Pt), температуре более 200оС и давлении с образованием циклогексана. Хлорирование бензола проводят при интенсивном ультрафиолетовом облучении с образованием гексахлорциклогексана (гексахлоран).
Гомологи бензола вступают в реакцию галогенирования по типу радикального замещения в боковой цепи, которое характеризуется предпочтительным замещением водорода у менее гидрогенизированного атома углерода:
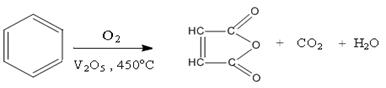
Окисления бензола и его гомологов. Бензол устойчив в обычных условиях к действию таких окислителе как азотная кислота, раствора перманганата калия, хромовой смеси, пероксида водорода. В жестких условиях окисления кислородом в присутствии катализатора оксида ванадия (V2O5, 450оС) бензол окисляется до малеинового ангидрида:
малеиновый ангидрид
Гомологи бензола, независимо от длины и разветвленности радикала боковой цепи, всегда окисляются по a - углеродному атому боковой цепи с разрывом С - С связи. Окисление возможно при действии раствора перманганата калия в кислой или щелочной среде при нагревании, что всегда приводит к образованию бензолкарбоновой кислоты и алкилкарбоновых кислот, в зависимости от числа и размера радикала. Ниже приведены примеры окисления гомологов бензола: а)
толуол бензойная кислота
б)
пропилбензол бензойная этановая кислота кислота в)
1,4-дипропил- бензол-1,4- бензол дикарбоновая кислота
Реакции окисления боковых цепей гомологов бензола используют с целью их идентификации. Число и относительное положение боковых цепей можно определить, окисляя соединения в соответствующие кислоты, которые затем можно идентифицировать различными физико-химическими методами. Реакции электрофильного замещения Конденсированных аренов Реакции электрофильного замещения в нафталине протекают в более мягких условиях, предпочтительно по 1 – положению (или α-), повышение температуры реакции приводит к образованию продукта замещения водорода во 2 – положение (или b-). Галогенирование нафталина осуществляется в присутствии галогенидов металлов при температуре 20-40оС.
1-бромнафталин 2-бромнафталин (99%) (1%)
б) Нафталин нитруется азотной кислотой в уксусном ангидриде при слабом нагревании или нитрующей смесью при комнатной температуре, повышение температуре способствует образованию более устойчивого b - продукта.
1-нитронафталин 2-нитронафталин
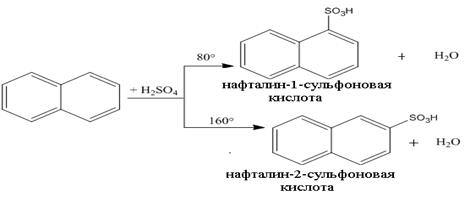
в) Сульфирование нафталина является примером термодинамически контролируемой реакции. Действие безводной концентрированной серной кислоты при 80оС приводит к образованию нафталин-1-сульфоновой кислоты, а повышение температуры до 160оС – нафталин-2-сульфоновая кислота:
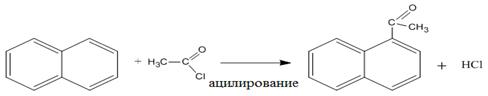
г) Ацилирование нафталина хлористым ацетилом при 0оС приводит к образованию предпочтительно 1- ацетилнафталина, выше 30оС – 2- ацетилнафталина:
Реакции присоединения для нафталина протекают в более мягких условиях в сравнении с бензолом. Например, гидрирование по одному бензольному кольцу возможно при действии водорода в момент выделения, в условиях каталитического гидрирования нафталин превращается в насыщенный декагидронафталин (тетралин).
тетралин декалин
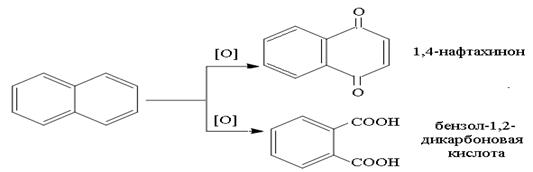
Окисление нафталина протекает легче, чем бензола. В более мягких условиях окисления образуется нафтахинон-1,4, при действии сильного окислителя – происходит разрушение одного из колец с образованием дикарбоновой кислоты по схеме:
Отдельные представители Бензол ( С6Н6) - жидкость с характерным запахом, почти нерастворимая в воде. Получают бензол при сухой перегонке каменного угля и переработки нефти. Широко используется в промышленности в качестве растворителя и сырья для синтеза красителей, полимеров, взрывчатых веществ, поверхностно - активных веществ. Бензол токсичен, вдыхание паров вызывает острое отравление, приступы головокружения, судороги. В организме углеводороды подвергаются С - гидроксилированию (окисление с ообразованием гидроксисоединений) и выводятся из клетки. Однако бензол окисляется очень медленно, поэтому накапливается в организме и относится к кумулятивным ядам. Толуол (метилбензол) - бесцветная жидкость, нерастворимая в воде. Применяют для получения бензола, бензойной кислоты, сахарина, взрывчатых веществ, лаков. Толуол добавляют к моторному топливу как высокооктановый компонент бензинов. Толуол примерно на два порядка мене токсичен, чем бензол, так как окисляется в организме до бензойной кислоты и быстрее выводится из клетки.
Кумол (изопропилбензол) - жидкость, является важным продуктом для синтеза фенола и ацетона кумольным способом. Цимол (пара -метилизопропилбензол) - является основой многих эфирных масел. Стирол (винилбензол) - приятно пахнущая жидкость, исходный мономер для получения полимеров, например, полистирола, который применяют в качестве электроизоляционного материала. При сополимеризации с бутадиеном получают некоторые виды синтетических каучуков. Полистирольные полимеры, содержащие функциональные группы кислого или основного характера, используют в качестве ионообменных смол. Ксилолы (диметилбензолы) используют в качестве компонента высокооктановых бензинов и растворителей в лакокрасочной промышленности, а так же применяют для получения полиэфиров. Нафталин - бесцветные пластинки, обладающие высокой летучестью (возгонка) и характерным запахом. Используется для получения фталевого ангидрида, фталевой кислоты, растворителей (тетралин и декалин) и разнообразных других производных. Антрацен - твердое вещество, в виде антрахинона используется в синтезе антрахиноновых красителей. Фенантрен в частично или полностью гидрированном состоянии входит в состав стероидных гормонов, алкалоидов как основной структурный компонент.
Сернистые соединения нефти
Сера является наиболее распространенным гетероэлементом в нефти и нефтепродуктах. Содержание ее в нефтях месторождений России изменяется от 0,05% до 3%. Таблица 26 Содержание серы в нефтях некоторых месторождений
В соответствии с технологической классификацией в зависимости от содержания серы нефти подразделяются на три класса: I- малосернистые, содержание до 0,5% серы; II- сернистые, содержание до 0,51 -2,0% серы; III- высокосернистые, содержащие более 2,0% серы. С повышением температуры кипения нефтяных фракций содержание в них серы увеличивается. До 60% всей серы нефти содержится во фракциях топлив и масел (выкипающих до 4500С), 40% и более в мазуте. Распределение серы по фракциям иллюстрируется данными таблицы 27. Таблица 27
Распределение серы (в масс. %) по фракциям различных сернистых и высокосернистых нефтей
Распределение серы по фракциям зависти от природы сернистых соединений.
Характеристика сернистых соединений нефти Сера в нефти и нефтепродуктах может содержаться в виде неорганических соединений серы: элементная сера и сероводород и органических: меркаптаны, сульфиды, дисульфиды, тиофены, тиофаны. Значительная часть серы нефти входит в состав смолисто-асфальтеновых веществ, это не идентифицированная сера.
Элементная сера и сероводород в сырых нефтях содержатся в незначительных количествах или не содержатся совсем. Они появляются в нефтях или в нефтяных фракциях в результате вторичных реакций. Сера может получаться при окислении сероводорода кислородом воздуха.
Или при термическом разложении дисульфидов
В свою очередь, дисульфиды образуются при окислении меркаптанов
Сероводород обычно образуется в процессах переработки нефти в результате термического разложения меркаптанов и сульфидов или при реакции углеводородов с серой.
Б.Н.Айвазовым как критерий термической стабильности сернистых соединений было предложении сероводородное число – количество Н2S(в мг), выделяющегося при нагревании 100 г нефти при 3000С в течение часа. Сероводородное число не связано с общим содержанием серы, так как, оно изменялось от 4,2 до 300,6 при изменении содержания серы от 0,7 до 30,3%. Оно связано с термической стабильностью сернистых соединений, что важно в процессах переработки нефти. Качественно сера и сероводород обнаруживаются по реакции
Меркаптаны RSH, или тиоспирты,или тиолы. Называюся про радикалу с добавлением слова меркаптан или тиол. Радикалы могут быть любые: алифатические, нафтеновые, ароматические:
изопропилмеркаптан
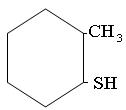
2-метил-циклогексилмеркаптан
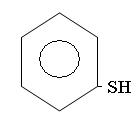
фенилмеркаптан или тиофен
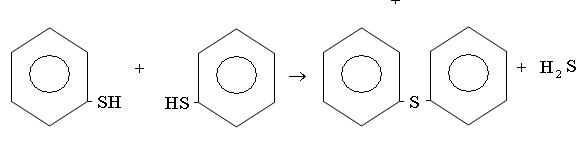
В виде меркаптанов сравнительно немного серы нефти – от 1 до 15% от всей серы нефти.Однако известны исключения из этой закономерности. Так нефть Марковского месторождения (Иркутская область) при общем содержании серы 0,96% содержит 0,77% меркаптановой серы; фракция 40-2000С газоконденсата Оренбургского месторождения содержит 1,24% общей серы, в том числе 0,297% меркаптановой. В наибольшем количестве меркаптаны содержатся в бензиновой фракции, с повышением температуры кипения их содержание быстро уменьшается; это связано с их низкой термической стабильностью. До 3000С меркаптаны разлагаются с образованием сульфидов.
При более высоких температурах - до олефинов
Сероводород может вновь присоединиться к олефину
Интересной особенностью алкилтиолов бензиновых фракций является то, что SH- группа чаще находится при вторичном или третичном атоме углерода, чем при первичном, что свидетельствует об их вторичном происхождении. По увеличении термической стабильности меркаптаны располагаются в ряд: первичные, вторичные, третичные, ароматические.
Слабыми окислителями (кислород воздуха, иод)меркаптаны окисляются до дисульфидов.
Сильными окислителями (азотная кислота, гидроперекиси(образующиеся при окислении углеводородов)) - до сульфокислот и даже до серной кислоты.
Образованием кислот, более агрессивных, чем меркаптаны, объясняется высокая коррозионная активность меркаптанов. С другой стороны, разрушая гидроперекиси, меркаптаны тормозят окисление углеводородов. Будучи, и обладая кислотными свойствами, меркаптаны взаимодействуют со щелочами, оксидами и солями металлов.
Промывка бензинов водно-щелочным раствором едкого натра (спирт добавляется для снижения гидролиза меркаптида натрия) используется для демеркаптанизации бензинов. Реакция с PbO является качественной реакцией на меркаптаны(докторская проба), после удаления Н2S.
Образование черного осадка PbS свидетельствует о наличии меркаптанов. Реакция с AgNO3 используется для количественного определения меркаптанов (титрованием) после удаления сероводорода. Соли образованные меркаптанами, называютмя меркаптидами с добавлением названия радикала (метилмеркаптид калия, бутилмеркаптид свинца) и т.д. В настоящее время выделено более 50 различных меркаптанов с числом углеродных атомов от 1 до9; из них более 40 алкилтиолов, 6 циклоалкилтиолов и тиофенол. Все меркаптаны имеют неприятный запах,низшие используются для одорации природного газа. Сульфиды или тиоэфиры подразделяются на алифатические (диалкилсульфиды) и алициклические (тиацикланы), содержащие атом серы в цикле. Алифатические называются по названию радикалов:
Метилфенилсульфид
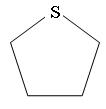
Циклические сульфиды называются как углеводороды с тем же числом углеродных атомов, включая серу, с добавлением приставки тиа:
Тиациклопентан
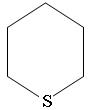
Тиациклогексан Или по количеству метиленовых групп –СН2, связанных через атом серы: тетраметиленсульфид, пентаметиленсульфид Сульфида содержатся в бензиновых и в основном в средних фракциях нефти, где они могут составлять более половины всех сернистых соединений. В бензиновых фракциях содержатся в основном диалкилсульфиды, в керосино-газойлевых и масляных фракциях – в основном циклические сульфиды. Таблица 28 Групповой состав сульфидов различных нефтей
Количество диалкилсульфидов (тиацикланов) снижается с повышением температуры кипения фракции; выше 3000С они практически отсутствуют. Углеводородные радикалы, содержащие три и более атомов углерода, обычно связаны с серой по вторичному углеродному атому.
Выделено более 50 тиаалканов, в т.ч. все изомеры С2-С6.Алкилциклоакилсульфиды и алкиларилсульфиды изучены в меньшей степени. В тиацикланах цикл, содержащий атом серы, может входить в полициклическую систему,содержащую до семи колец. Атом серы чаще входит в пятичленный цикл (тиациклопентан) –на 60-70% и в 30-40% случаев –в шестичленный(тиациклогексан). В полициклических системах атом серы всегда находится в
В нефтях были также обнаружены сернистые соединения мостикового строения: -Бициклические
Трициклические
Среднюю молекулу тиацикланов средних фракций можно изобразить следующим образом:
Где R1 и R2 – СН3 или С2Н5; n = 2÷6. С повышением температуры кипения фракции увеличивается количество циклов в молекуле, реже- растет длина алкильных цепей. Ароматические серусодержащие соединения представлены производными
тиаиндана
Тиатетралина с алкильными цепями. Основные реакции сульфидов Обусловлены в основном наличием двух неподеленных пар электронов у атома серы. С протоном кислоты сульфиды дают сульфониевые соединения: Эта реакция используется в промышленности для извлечения сульфидов из нефтяных фракций. Процесс идет в две ступени: на первой ступени используется 86%-ная серная кислота, при этом извлекаются сульфиды алифатического и нафтенового строения; на второй ступени используется 91%-ная серная кислота, при этом извлекаются сульфиды ароматического строения. После отделения сульфониевые соединения разлагаются при разбавлении водой. Сульфиды дают комплексные соединенияс солями тяжелых металловза счет передачи неподеленной пары электронов атома серы на свободную электронную орбиталь акцептора. Важнейшие комплексообразователи: хлорид алюминия, тетрахлорид титана, ацетат серебра, хлорид ртути (I I), карбонилы железа.
Комплексы разлагаются водным раствором аммиака или горячей водой. Реакция эта используется для извлечения сульфидов из нефтяных фракций(часто ацетатом ртути) или для извлечения редких и драгоценных металлов (Pt,Pd,Ag,Au, Ir и др.) из растворов. Сульфиды окисляются различными окислителями(Н2О2, НNO3, кислород воздуха, гидроперекиси) с образованием сульфоксидов и сульфонов
Сульфоксид Сульфон
При окислении нефтепродуктов сульфиды взаимодействуют с образующимися гидроперекисями, разрушая их
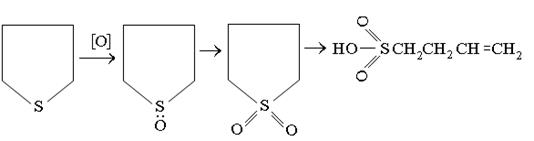
И тем самым тормозя процесс окисления. Этим объясняется антиокислительное действие сульфидов и сульфоксидов. Оно в большей степени проявляется при действии сульфоксидов, чем сульфидов. Некоторые сульфоксиды (диметилсульфоксид) и сульфоны (тетраметиленсульфон, сульфолан) используют как экстрагенты для извлечения ароматических углеводородов из нефтяных фракций. Среди продуктов глубокого окисления сульфидов присутствуют, наряду с сульфоксидами и сульфонами, сульфокислоты, непредельные соединения, альдегиды и кетоны. В термическом отношении сульфиды устойчивее меркаптанов, чем объясняется присутствие их в средних и высших фракциях нефти. Циклические сульфиды устойчивее алифатических. Разлагаются сульфиды вначале до меркаптанов и олефинов, затем до сероводорода и олефинов:
Количественно сульфиды определяются по реакции:
Дисульфиды содержатся в небольших количествах, составляя 7-15% всей серы нефти. Присутствуют во фракциях до 3000 по свойствам подобны сульфидам. Восстановление (водородом в момент выделения) приводит к меркаптанам:
Реакция используется в аналитической практике, они определяются в виде меркаптанов. Тиофены отличаются высокой термической стабильностью и присутствуют в средних и высших фракциях нефти. В средних фракциях содержатся алкилпроизводные тиофена:2;3-метил,2;3-этил, реже пропилпроизводные; 2,3; 2,4; 2,5; 3,4-диметилтиофены.
Реже встречаются циклоалкилтиофены, они содержат одно или два конденсированных с тиофеном нафтеновых кольца. Гораздо более распространены арилтиофены:
Дибензтиофен
Бензтиофен
Нафтотиофен и их алкилированные гомологи. В виде тиофенового кольца сера входит в состав САВ нефти. В химическом и термическом отношении тиофены устойчивы к окислению; проявляют ароматический характер. В присутствии катализатора все сернистые соединения гидрируются с потерей серы в виде сероводорода, на этом основано обессеривание нефтепродуктов.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-06-28; просмотров: 2653; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.43.27 (0.011 с.) |










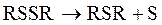
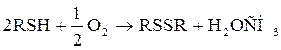
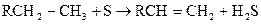





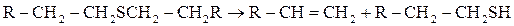







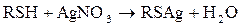

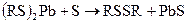
 диметилсульфид
диметилсульфид

 -положении к соседнему кольцу. В американских нефтях было обнаружено следующее соотношение бициклических систем:
-положении к соседнему кольцу. В американских нефтях было обнаружено следующее соотношение бициклических систем: ≈ 35:50:15
≈ 35:50:15
 тиаадамантан
тиаадамантан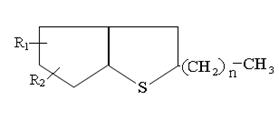







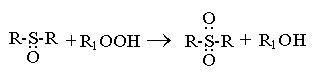

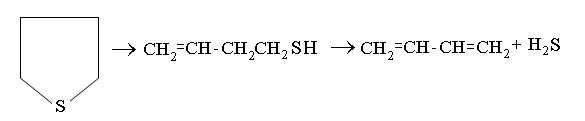
 2RSR+2HCl+KIO3 2RSOR+ICl+RCl+H2O
2RSR+2HCl+KIO3 2RSOR+ICl+RCl+H2O R-S-S-R+2H 2RSH
R-S-S-R+2H 2RSH






