Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Показания и противопоказанияСодержание книги
Поиск на нашем сайте К ПЕРЕСАДКЕ ЛЕГКОГО С начала 80-х годов прошлого века, когда трансплантация легкого (LTr) была предложена для лечения пациента с сосудистым заболеванием легких, спектр патологии, при которой пересаживают легкие, значительно расширился. В настоящее время LTr наиболее часто выполняют при терминальных стадиях хронической обструктивной болезни; эмфиземе; идиопатическом фиброзирующем альвеолите; муковисцидозе; первичной легочной гипертензии (ПЛГ), синдроме Эйзенменгера (рис. 4).
Рисунок 4 - Частота патологии легких, при которой выполняют LTr (%)
К абсолютным противопоказаниям относятся: •хроническая недостаточность других органов, включая почечную; печеночную с коагулопатией или портальной гипертонией; левожелудочковую недостаточность; обширное поражение коронарных артерий; •злокачественное новообразование; •активный внелегочный инфекционный процесс; •курение (отказ от курения менее чем 3 мес. назад); • ожирение - масса более 130% должного, • низкий реабилитационный потенциал; •неадекватное поведение и плохое сотрудничество с медицинским персоналом. Оптимальный возраст для трансплантации комплекса «сердце-легкие» - 50 лет, двусторонней LTr - 55, односторонней LTr - 65. Наряду с отторжением не менее остро стоит проблема инфекции в посттрансплантационном периоде. Исходная колонизация микроорганизмами, их чувствительность к антибактериальным препаратам часто имеют решающее значение в исходе лечения. Актуальность проблемы возрастает в группах реципиентов с муковисцидозом и бронхоэктазами, которых на протяжении жизни лечили многими противомикробными средствами, в связи с чем сформировались резистентные штаммы микроорганизмов. В некоторых трансплантационных центрах подобные инфекции служат поводом для отказа от пересадки легкого. Абсолютным же противопоказанием остается активный туберкулез, гепатит, СПИД.
ЛЕГОЧНОЕ ДОНОРСТВО Ситуация с донорскими легкими отличается от донорских проблем с другими органами. Во-первых, ожидание легочного трансплантата более длительное и с более высокой смертностью в «листе ожидания», чем при пересадке сердца и печени. Во-вторых, легкие наиболее повреждаемый орган у доноров со смертью головного мозга. Они чувствительны к гипергидратации, при черепно-мозговой травме имеется возможность аспирации желудочного содержимого с развитием воспаления при проведении реанимации, ИВЛ. В-третьих, легкие исходно инфицированы, поскольку они постоянно контактируют с внешней средой. Даже не очень длительная ИВЛ может приводить к развитию трахеобронхита и пневмонии, что делает орган непригодным. В-четвертых, легкие плохо переносят ишемию и консервацию. Допустимое время консервации 6-8 ч. Эти и некоторые другие аспекты обусловливают то, что легкие могут быть использованы лишь от 20% доноров со смертью головного мозга, у которых забирают другие органы для трансплантации. Формально требования к донору следующие: возраст менее 65 лет, отсутствие данных о легочных заболеваниях, нормальная рентгенограмма грудной клетки, хорошее расправление легкого, адекватная оксигенация, удовлетворительная бронхоскопическая картина, соответствие размера трансплантата объему грудной клетки реципиента. Этапы забора легкого: • срединная стернотомия, вскрытие обеих плевральных полостей; • разделение аорты и легочного ствола; • системное введение гепарина в дозе 3 мг/кг, что составляет приблизительно 20-25 тыс.ед.; • подготовка системы перфузии, растворов, ледяной крошки (ice-slush); • катетеризация восходящей аорты и легочного ствола; • системно вводится простагландин Е (Alprostadil или Eproprostendol, PGE1) -1 ампула; • перевязка и пересечение верхней полой вены; • перевязка нижней полой вены; • отсечение ушка левого предсердия; • зажим на восходящую аорту; • синхронная перфузия через все катетеры консервирующего раствора; • местное охлаждение; • удаление легкого после отсечения элементов его корня (легочная артерия отсекается по ее бифуркации, легочные вены - с оставлением вокруг них небольшого участка предсердия, бронх ушивают сшивающим аппаратом и отсекают) и удаление сердца. Во избежание развития гидростатического отека трансплантата давление раствора при перфузии консервирующего раствора не должно превышать 10-15 мм рт.ст., температура, при которой выполняется перфузия +4 - С°. Перфузия через легочную артерию позволяет достаточно хорошо промыть легочную паренхиму. Важным моментом в трансплантации легкого является реперфузия трансплантата. В течение 10 мин давление в легочной артерии должно быть минимальным, что обеспечивает защиту эндотелия, поврежденного при консервации. При заборе долей легкого от живых доноров перфузию и консервацию выполняют in vitro во избежание попадания консервирующего раствора в системное кровеносное русло донора. Клинически ишемическо-реперфузионное повреждение проявляется отеком легкого. Существует несколько возможностей воздействовать на этот процесс, используя простагландины, кортикостероиды и вентиляцию газовыми смесями, содержащими NO. Лекарственные препараты можно вводить донору перед перфузией, либо их использовать как составную часть консервирующего раствора или назначать реципиенту непосредственно перед реперфузией. Применяют высокие дозы метилпреднизолона (500-1000 мг), их вводят непосредственно перед реперфузией.
ВЫБОР ВАРИАНТА ТРАНСПЛАНТАЦИИ Существует четыре варианта трансплантации легких: односторонняя, двусторонняя, комплекс «сердце-легкие», пересадка долей легких от живых доноров. ХИРУРГИЧЕСКАЯ ТЕХНИКА Односторонняя трансплантация легкого. Стандартным доступом для SLTr является заднебоковая торакотомия. Легкое выделяют, мобилизуют его корень, проводят пробы с отключением оперируемого легкого от ИВЛ. После удаления собственного легкого в условиях сохраняющейся гипотермии выполняют три анастомоза реципиента с донорским легким. Последовательность выбирается спереди-назад и соответствует - бронх, артерия, венозное соустье реципиента с манжеткой предсердия трансплантата (рис. 5).
Рисунок 5 - Этапы (а-г) телескопического межбронхиального анастомоза Венозный анастомоз выполняют соединением венозного соустья реципиента с участком предсердия вокруг вен трансплантата.

Артериальный анастомоз накладывают по типу «конец в конец» нитями (рис. 6).
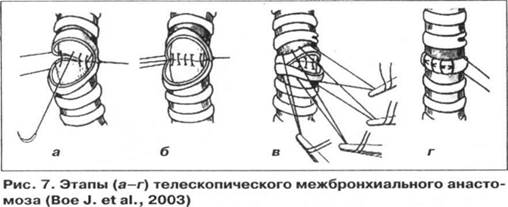
Трансплантация доли легкого от живых доноров При лобэктомии у доноров обеспечивают максимальную длину сосудов и бронха. Для этого их отсекают по бифуркации вышележащего долевого бронха или артерии. Нижнюю легочную вену отсекают тотчас по левому предсердию. Имплантацию доли в позицию удаленного легкого выполняют на той же стороне. Анастомозы накладывают с учетом различного диаметра структур корня легкого реципиента и трансплантата. (рис. 7). Искусственное кровообращение требуется от момента выполнения пневмонэктомий до реперфузии долей и восстановления ИВЛ.

ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД В послеоперационном периоде приходится решать ряд задач: обеспечение вентиляционной поддержки, коррекции электролитных и гемодинамических нарушений, диагностики раннего отторжения, профилактики и лечения инфекционных осложнений. Новое трансплантированное легкое имеет склонность к развитию отека, что связано с повышенной проницаемостью легочных сосудов и нарушением лимфатического дренажа. В основе этих нарушений лежат ишемическо-реперфузионное повреждение трансплантата, инфицирование органа на донорском этапе, а также травма его при операции. Иммуносупрессивная терапия после трансплантации легкого Иммуносупрессивная терапия включает в себя вводную (индукционную) терапию, поддерживающую, лечение острого и хронического отторжения. Применяется многокомпонентная иммунносупресивная терапия.
ТРАНСПЛАНТАЦИЯ ПЕЧЕНИ История трансплантации печени охватывает период около 50 лет. Впервые в эксперименте трансплантация дополнительной печени в гетеротопическую позицию была выполнена в 1955 г. C.S.Welch. Идея такого способа операции подкупала технической простотой, не удаляя пораженную печень, C.S.Welch помещал печеночный трансплантат в подвздошную ямку и накладывал анастомоз между печеночной артерией и аортой, воротную вену анастомозировал с нижней полой веной, а холедох имплантировал в тонкую кишку. Вскоре, однако, выяснилось, что у выживших животных быстро наступала атрофия донорской печени, что вначале объясняли реакцией отторжения. Позднее, в 60-е годы, Т.Starzl установил, что основной причиной атрофии печени при гетеротопической трансплантации является отсутствие в органе портального кровотока. Последующими работами T.Starzl был доказан гепатотрофический эффект глюкагона и инсулина, содержащихся в крови воротной вены. Именно поэтому в дальнейшем основным способом трансплантации печени в клинике стала методика ортотопической трансплантации. В 60-e годы ХХ века наиболее подготовленной к трансплантации печени была группа американских хирургов во главе с T.Starzl.
Томас Старзл Первые положительные результаты были получены T.Starzl в 1967 году. Во многом этому способствовало использование новых протоколов иммуносупрессивной терапии. Максимальная продолжительность жизни многих реципиентов превысила 20 лет. С 80-х годов текущего столетия трансплантация печени становится стандартной операцией в лечении необратимых хронических заболеваний печени. В настоящее время в Институте Трансплантации Томаса Старзла (Питтсбург, США) ежегодно выполняется 500–600 подобных операций. В Европе первая успешная трансплантация печени была выполнена в Кембриджском университете Sir Roy Calne 23 мая 1967 года. После внедрения в клинику техники трансплантации доли печени от живого родственного донора, существенно расширились возможности трансплантации в педиатрии. Технические аспекты трансплантации левой доли печени разработаны B.Smith в 1969 году, в клинике такой вариант операции впервые был выполнен R.S.Raia (1988). Первая же успешная трансплантация доли печени произведена R.W.Strong в Австралии. В настоящее время трансплантация печени во многих развитых странах стала клиническим методом лечения хронических заболеваний печени в терминальной стадии. Трансплантация печени является также безальтернативным методом лечения при фульминантном печеночном повреждении, сопровождающимся массивным гепатоцеллюлярным некрозом. Основоположник метода – T.Starzl – считает, что “ни один крупный гепатологический центр не может считать себя таковым, если он не владеет методом печеночной трансплантации” (T Starzl, 1994). По данным статистических отчетов Евротранспланта, количество трансплантаций печени колеблется в разных странах от 7 до 18 операций на 1 млн. населения и составляет более 10000 в год. Наибольшее число операций выполняется в США – 4500 в год. К концу ХХ века в мире произведено более 70000 трансплантаций печени, максимальная продолжительность жизни реципиентов превысила 26 лет. История трансплантации печени
Показания и противопоказания к трансплантации печени Показания к трансплантации печени могут быть разделены на абсолютные (фульминантная и быстропрогрессирующая хроническая печеночная недостаточность с неблагоприятным ближайшим прогнозом) и относительные (последние охватывают более 50 нозологий). Во всех случаях решающими клиническими факторами, которые свидетельствуют в пользу выполнения трансплантации, есть прогрессирующая печеночная недостаточность, которая обнаруживает себя стойкой гипербилирубинемией, снижением протромбинового индекса, гипоальбуминемией, асцитом, кровотечением из пищеводных флебэктазий, портосистемной энцефалопатией, гепаторенальным синдромом. Показания к трансплантации печени ● Вирусный цирроз (В, С) ● Алкогольный цирроз ● Первичный билиарный цирроз ● Первичный склерозирующий холангит ● Аутоиммунный гепатит ● Фульминантный гепатит ● Метаболические заболевания печени ● Злокачественные новообразования печени ● Билиарные атрезии Абсолютными противопоказаниями к трансплантации печени являются наличие ВИЧ-инфекции, экстрагепатические злокачественные опухоли, неконтролируемая инфекция, прогрессирующая кардиопульмонарная недостаточность, тяжелая легочная гипертензия, наркотическая и алкогольная зависимость, отказ от соблюдения правил иммуносупрессии. После установления показаний к трансплантации необходимо оценить тяжесть состояния реципиента и его способность перенести операцию. У пациентов, не требующих проведения интенсивной предоперационной подготовки, 1-летняя выживаемость трансплантата составляет 90%, если же такая подготовка необходимая - только 50%. Пациенты с портальной гипертензией, осложненной кровотечением с пищеводных флебэктазий, составляют особенно трудную группу больных. Перед трансплантацией им целесообразно выполнить эндоскопическое склерозирование вен пищевода. Критерии селекции донора Первичная оценка потенциального донора печени, совместимого с реципиентом по системе АВО, включает анализ антропометрических характеристик, анамнестических данных, данных клинических и инструментальных методов обследования. Возраст донора не должен превышать 45-50 лет. Вес донора должна составлять 0,70-1,10 от веса. Абсолютными противопоказаниями к забору донорской печени являются заболевания гепатобилиарной зоны, злоупотребление алкоголем, наркотическая зависимость, травма брюшной полости, отравление гепатотропными ядами, наличие экстрацеребральных злокачественных опухолей, ВИЧ-инфекция, HbsAg и антитела к гепатиту С, остановка кровообращения более 10 минут, продолжительная (свыше 7 суток) ИВЛ. Обязательными клиническими обследованиями донора являются определение печеночных ферментов (АСТ, АЛТ), щелочной фосфатазы, общего и прямого билирубина, протромбинового индекса, белковых фракций, HbsAg, УЗИ печени.
Несмотря на тщательное обследование донора, во время проведения процедуры эксплантации, иногда имеющиеся заболевания печени бывают нераспознанными. Это может вызвать очень серьезные последствия, в том числе и отсутствие начальной функции трансплантата. Для предотвращения подобной ситуации обязательным правилом являются выполнения превентивной биопсии и проведение срочной морфологической оценки состояния донорской печени.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 458; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.216 (0.011 с.) |