
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Zinci oxydum – окись цинка – ZnOСодержание книги
Поиск на нашем сайте Описание: белый или белый с желтоватым оттенком аморфный порошок без запаха. Поглощает СО2 воздуха. ZnO + CO2 à ZnCO3 Растворимость: практически нерастворим в воде и спирте, растворим в растворах щелочей, разв. минеральных кислотах, уксусной кислоте. Подлинность: при прокаливании окрашивается в желтый цвет., при охлаждении снова белеет. Допустимые примеси: мышьяк. Недопустимые примеси: карбонаты и нер-мые примеси железа, меди, алюминия, свинца. Количественное определение: Прямая комплексонометрия после растворения в соляной кислоте и нейтрализации раствором аммиака. Титрант: трилон Б, pH=9,5-10. Инд – кислотный хром черный специальный. Хранение: в хорошо упакованной таре Применение: вяжущее, подсушивающее, дезинфицирующее, при кожных заболеваниях.
Bismuthi subnitras – висмута нитрат основной. Описание: белый аморфный или микрокристаллический прошок. Смоченный водой окрашивает синюю лакмусовую бумагу в красный цвет. Растворимость: практически нерастворим в воде и спирте, легко растворим в азотной и соляной кислоте. Подлинность: С сульфидом натрия выпадет коричнево-черный осадок, растворимый в концентрированной азотной кислоте. 2Bi3+ + 3Na2S à Bi2S3¯ + 3K+ Bi2S3 + 6HNO3 à 2Bi(NO3)3 + 3H2S С KI выпадет черный осадок, растворимый в избытке KI (образуется желто-оранжевый комплекс). Bi3+ + 3KI à BiI3¯ + 3K+ При прокаливании выделяются желто-бурые пары и остаток ярко-желтого цвета. Висмута нитрат основной Допустимые примеси: хлориды щелочных и щелочно-земельных металлов, серебро. Недопустимые примеси: CO3, NH4, Cu, Pb, SO4, As, Te Количественное определение: прямая комплексонометрия. Индикатор: пирокатехиновый фиолетовый. рН=2-3 (HNO3). Титрант – трилон Б.
Вторая и третья стадии см. Магния сульфат. Расчет ведут по Bi2O3. Расчетная формула для прямого титрования без контрольного опыта. Хранение: в хорошо упак. таре, предохр. от д-я света. Применение: Вяжущее антисептическое при заболеваниях ЖКТ. Соединения меди, серебра. Cuprisulfas – сульфат меди – CuSO4•5H2O Описание: синие кристаллы или синий кристаллический порошок без запаха. Медленно выветривается на воздухе. Водный растворы имеют слабокислую реакцию. Растворимость: легко растворим в воде. Очень легко в кипящей. Пр. нер-рим в 95%спирте. Подлинность: 1) Металлическая скрепка покрывается медным налетом. Сu2+ + Fe à Fe2+ + Cu 2) Ионы меди образуют синий комплекс с раствором аммиака. CuSO4 + 2NH4OH à Cu2(OH)2SO4¯ + (NH4)2SO4 Cu2(OH)2SO4 + (NH4)2SO4 + 6NH4OH à 2[Cu(NH3)4]SO4 синий + 8H2O 3) Сульфаты с солями бария дают белый осадок, нерастворимый в минеральных кислотах. SO42- + Ba2+ àBaSO4 Допустимые примеси: хлориды, железо, соли металлов, не осаждающихся H2S Количественное определение: косвенная йодометрия (нефармакопейно – прямая комплексонометрия с индикатором мурексидом) CuSO4 + 2KI à CuI2 + K2SO4 2CuI2 à 2CuI¯ + I2 осадок цвета слоновой кости I2 + 2Na2S2O3 à 2NaI + Na2S4O6 f(CuSO4) = 1/2 Хранение: список Б. В хорошо упакованной таре. Применение: Антисептик, вяжущее, прижигающее, наружно, иногда внутрь (рвотное). Argenti nitras – нитрат серебра – AgNO3 Описание: бесцв. прозрачн. кристаллы в виде пластинок или белых цилиндрич. палочек, без запаха. Под действием света темнеет. Растворимость: очень легко растворим в воде, труднорастворим в спирте. Подлинность: 1) С хлоридами выпадает белый творожистый осадок, нер-мый в HNO3, р-мый в NH4OH. Ag+ + Cl- à AgCl¯ 2) Реакция серебряного зеркала. 2[Ag(MH3)2]OH + H-COH 3) Реакция с дифениламином. реакцию см. примесь нитратов в воде Недопустимые примеси: Висмут, медь, свинец Количественное определение: Тиоцианатметрия. Индикатор: FeNH4(SO4)2•12H2O, среда – HNO3. Титрант – роданид амония NH3SCN. AgNO3 + NH4CNS Fe3+ + 6CNS- à [Fe(CNS)6]3- красный f(AgNO3) = 1; Хранение: список А. В банках с притертой пробкой в защищенном от света месте. Применение: Антисептическое и прижигающее. Применяется наружно, иногда внутренне Органические лекарственные вещества Классификация v По происхождению: природные - алкалоиды, гормоны и т.д. синтетические. v По строению: алифатические циклические гетероциклические карбоциклические алициклические ароматические
|
||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 709; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.113 (0.009 с.) |

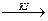 K[BiI4]
K[BiI4] 2Bi2O3 + H2O + 2NO2 + O2
2Bi2O3 + H2O + 2NO2 + O2

 2Ag¯ + HCOONH4 + 3NH3 + H2O
2Ag¯ + HCOONH4 + 3NH3 + H2O AgCNS¯ + NH4NO3
AgCNS¯ + NH4NO3



