
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Расчет навески вещества для приготовления титрованного раствораСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
К исходным веществам для приготовления титрованных растворов предъявляются определенные требования: чистота, постоянство состава, устойчивость, большая величина молярной массы эквивалента. Если вещество удовлетворяет этим требованиям, раствор титранта готовят по точной навеске, взятой на аналитических весах с точностью до четвертого знака, точная концентрация такого раствора устанавливается в процессе приготовления.
Если вещество не удовлетворяет указанным требованиям, то отвешивают на технических весах приблизительную навеску вещества, на 5-10% больше теоретической. Точную концентрацию такого раствора устанавливают по навеске или раствору стандартного вещества
При приготовлении растворов некоторых кислот (серной, хлороводородной) необходимо учитывать, что концентрированные растворы кислот не являются 100%-ными, а содержат воду, объемы таких растворов, используемых для приготовления титрованных растворов, отмеривают мерными цилиндрами (приблизительный объем). Алгоритм решения 1. Для расчета навески вещества необходимо знать фактор эквивалентности, молярную массу эквивалента вещества, концентрацию и заданный объем титрованного раствора. 2. Вычислить титр раствора по заданной концентрации:
Если требуемая концентрация раствора неизвестна, то ее рассчитывают из других данных условия задачи: из величины титра данного раствора по какому-либо веществу
3. Титр раствора показывает массу исходного вещества в 1 см3 раствора, поэтому для вычисления навески этого вещества нужно вычислить массу вещества в заданном объеме раствора а = ТТР × VТР Пример. 6. Какую навеску КОН, содержащего 10% индифферентных примесей, следует взять для приготовления 800 см3 0,2000 моль/дм3 раствора? Решение. 1. fЭ(КОН) = 1, следовательно, MЭ(КОН) = МКОН = 56,11 г/моль 2. 3. Рассчитывают навеску чистого КОН аКОН = 0,01122 × 800 = 8,9722 г 4. Вычисляют навеску КОН, необходимую для приготовления титрованного раствора, с учетом содержащихся в веществе примесей: 100 – 10 = 90% чистого КОН содержится в исходном веществе, тогда: а = 8,9722 × 100 / 90 = 9,9777 г Расчет концентраций и объемов при приготовлении титрованных растворов Пример 7. Рассчитать объем, в котором надо растворить навеску Ba(OH)2 массой 0,8567, чтобы получить раствор с молярной концентрацией эквивалента 0,1000 моль/дм3. Решение. 1. fЭ Ва(ОН)2= ½, Э Вa(ОН)2= ½ Вa(ОН)2, МЭ = ½М=½171,35 г/моль=85,67 г/моль 2. Расчет концентраций и объемов стандартизованных (установленных) титрованных растворов по результатам титрования В основе решения задач такого типа лежит закон эквивалентов, из которого вытекает основное уравнение титриметрии:
Зная значения трех величин из этих уравнений из результатов титрования, всегда можно рассчитать четвертую.
Способ пипетирования – способ установления точной концентрации раствора, приготовленного по приблизительной навеске вещества. Аликвотную часть стандартного раствора известной концентрации титруют устанавливаемым рабочим раствором (или наоборот). Алгоритм решения 1. Записать уравнение реакции, лежащей в основе определения. 2. Записать основное уравнение титриметрии, применительно к реагирующим веществам, проставляя в него известные величины. При необходимости проводят дополнительные вычисления некоторых значений. 3. Рассчитать искомую величину по данному уравнению. 4. Вычислить далее другие необходимые по условию задачи величины по соответствующим формулам. Пример 8. Вычислить СЭ, Т и КП раствора КОН по 0,1000 моль/дм3 раствору Н2SO4, если на 10,00 см3 раствора КОН расходуется 12,00 см3 этого раствора H2SO4. Решение. 1. H2SO4 + 2KOH = K2SO4 + 2H2O 1 моль 2 моль 2. 3. 4. МЭКОН = fЭ × МКОН = 1 × 56,11 = 56,11 г/моль
Расчет массового содержания определяемого вещества в анализируемом образце Алгоритм решения 1. Записать уравнение реакции, лежащей в основе определения. 2. Установить вариант и способ титрования, фактор эквивалентности и молярную массу эквивалента определяемого вещества. 3. Вычислить титр раствора по определяемому веществу. 4. Рассчитать массовое содержание определяемого вещества путем умножения вычисленного титра на объем израсходованного титранта. 5. При необходимости перед расчетом массового содержания провести дополнительные вычисления определенных величин, исходя из условия задачи.
Пример 9. Вычислить массу КОН, содержащегося в навеске, если на ее титрование было израсходовано 19,44 см3 раствора H2SO4 с молярной концентрацией эквивалента 0,1410 моль/дм3. Решение. 1. 2KOH + H2SO4 = K2SO4 + 2H2O 2 моль 1 моль 2. Прямое титрование, способ отдельных навесок, fЭ (КОН) = 1, 3. 4. Расчет массовой доли (w%) определяемого вещества в анализируемом образце Алгоритм решения Действия 1-5 таких типовых задач провести аналогично приведенному выше алгоритму. 6. Далее, принимая исходную навеску за 100%, составить пропорцию: а – 100% Q – (w%) (w%) = Q × 100 / а
Основные формулы, используемые в физической и коллоидной химии Раздел II. Физическая химия Тема. Основные понятия и законы термодинамики и термохимии Зная основные законы термодинамики и термохимии, студенты должны уметь производить термодинамические расчеты. Задача 1 При хранении муки моносахариды медленно окисляются кислородом воздуха с выделением тепла. Найдите тепловой эффект реакции, если теплоты образования равны: DНобр.СО2 = –393,6 кДж/моль, DНобр.Н2О = –285,9 кДж/моль, DНобр.С6Н12О6 = –1272,45 кДж/моль Дано:
DН =? Ответ: тепловой эффект реакции окисления муки равен – 2794,56 кДж.
|
||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 967; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.218.134 (0.006 с.) |


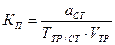

 или
или 
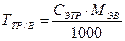 Þ
Þ 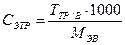
 г/см3
г/см3 =
=  × V Þ
× V Þ 
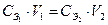 или
или 
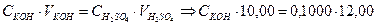
 моль/дм3
моль/дм3
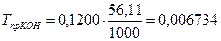 г/см3
г/см3 г/см3
г/см3 или
или 
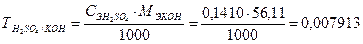 г/см3
г/см3
 = –285,9 кДж/моль
= –285,9 кДж/моль
 = –1272,45 кДж/моль
= –1272,45 кДж/моль
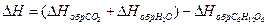
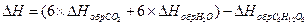 DН = [(6´(–393,6)+6´(–285,9)] – – (–1272,45)=2794,56 кДж
DН = [(6´(–393,6)+6´(–285,9)] – – (–1272,45)=2794,56 кДж



