Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Распространение и локализацияСодержание книги
Поиск на нашем сайте
Флавоноиды широко распространены в растительном мире. Особенно богаты флавоноидами цветковые растения, относящиеся к семействам розоцветных (различные виды боярышника, арония (рябина) черноплодная), бобовых (софора японская, стальник полевой, виды солодки), гречишных (горцы перечный и почечуйный, спорыш птичий, гречиха посевная), сложноцветных (бессмертник песчаный, сушеница топяная, пижма обыкновенная), губоцветных (пустырники сердечный и пятилопастный) и др. Наиболее высокое содержание флавоноидов отмечено у тропических и альпийских растений. Обнаружены флавоноиды и у споровых растений (мхи, папоротники, хвощи), реже встречаются в водорослях, грибах, а также в микроорганизмах и насекомых. Локализуются флавоноиды в различных органах, но чаще в надземных: цветках, листьях, плодах; значительно меньше их в стеблях и подземных органах (солодка, шлемник байкальский, стальник полевой). Наиболее богаты флавоноидными соединениями молодые цветки, незрелые плоды. Содержание флавоноидов в растениях различно - в среднем 0,5-5 %, иногда достигает 20 % (в бутонах софоры японской). В растениях флавоноиды присутствуют в растворенном виде в клеточном соке, в основном в виде гликозидов, которые лучше растворяются в воде. Под влиянием ферментов гликозиды расщепляются на сахара и агликоны. В качестве cахарных остатков чаще встречаются: из гексоз - D-глюкоза, D-галактоза; из пентоз - D-ксилоза, L-арабиноза; из метилированных пентоз – L-рамноза; из уроновых кислот - D-глюкуроновая кислота. Основную группу составляют O-гликозиды; в меньшей степени распространены С-гликозиды. О-гликозиды, в зависимости от числа остатков сахара, положения и порядка их присоединения, делятся на монозиды, биозиды, триозиды и дигликозиды. В дигликозидах моносахара присоединяются в двух разных положениях флавоноидного ядра.
Факторы, влияющие на накопление флавоноидов Основными являются возраст и фаза развития растений. Наибольшее количество флавоноидов накапливается у многих растений в фазе цветения, а в фазе плодоношения уменьшается. Факторы окружающей среды (свет, почва, влага, высота над уровнем моря и др.) оказывают также значительное влияние на накопление флавоноидов. В южных и высокогорных районах, под влиянием света, и на почвах, богатых микроэлементами, содержание флавоноидов увеличивается. Биологическая роль флавоноидов
1. Флавоноиды играют роль фильтров в растениях, защищая ткани от вредного воздействия УФ-лучей. 2. Согласно гипотезе русского биохимика В.И. Палладина именно флавоноиды являются переносчиками водорода в дыхательной цепи митохондрий растительной клетки. 3. Флавоноиды участвуют в процессе фотосинтеза и окислительного фосфорилирования. Совместно с аскорбиновой кислотой участвуют в ферментативных процессах окисления и восстановления, способствуют выработке иммунитета. 4. Являясь растительными пигментами, флавоноиды (в частности, антоцианы) придают яркую окраску цветкам и плодам, чем привлекают насекомых-опылителей, птиц и животных, и тем самым способствуют опылению и распространению растений. Классификация флавоноидов Современная классификация флавоноидов основана на: · положении бокового фенильного радикала; · степени окисленности пропанового фрагмента; · величине, наличии или отсутствии гетероцикла.
I. В зависимости от места присоединения бокового фенильного радикала флавоноиды делят на 4 группы: 1. Собственно флавоноиды (эуфлавоноиды). Боковой фенильный радикал присоединяется в положении 2. Наиболее многочисленная группа (известно около 400 агликонов). Выделяют 10 основных классов эуфлавоноидов. 2. Изофлавоноиды. Боковой фенильный радикал присоединяется в положении 3. Известно около 60 соединений, характерных главным образом для представителей семейства бобовых. 3. Неофлавоноиды. Боковой фенильный радикал присоединяется в положении 4. Малоизученная группа флавоноидов, обнаружены только в семействах зверобойных, мареновых и бобовых. 4. Другие классы флавоноидов: ксантоны, флаволигнаны, кумарофлавоноиды, бифлавоноиды. Данные соединения широко изучаются и обладают высокой биологической активностью. II. По степени окисленности пропанового фрагмента собственно флавоноиды (эуфлавоноиды) делят на: окисленные и восстановленные. Восстановленные (производные флавана) делятся на 5 групп.
1. Катехины (флаван-3-олы). Наиболее восстановленные флавоноидные соединения.
Молекула флаван-3-олов содержит два асимметрических атома углерода в пирановом кольце (С2 и С3) и, следовательно, для каждой молекулы возможны четыре изомера и два рацемата. Например, известные изомерные соединения (+)-катехин и (–)-эпикатехин отличаются конфигурацией гидроксильной группы третьего углеродного атома, они отличаются также по физическим свойствам (температура плавления, удельное вращение и др.). Эпикатехин обладает большей биологической активностью. Накапливаются в листьях чая китайского. 2. Лейкоантоцианидины (флаван-3,4-диолы).
Известно 12 соединений. Лейкоантоцианидины в виде мономеров сопутствуют катехинам в листьях чая китайского. Димеры и полимеры катехинов и лейкоантоцианидинов – структурные единицы конденсированных дубильных веществ. В отличие от других флавоноидов катехины и лейкоантоцианидины, как правило, не образуют гликозилированных форм. Лейкоантоцианидины представляют собой лабильные соединения, легко окисляющиеся до соответствующих антоцианидинов при нагревании с кислотами. 3. Антоцианидины (производные катиона флавилия).
Обнаружено 6 агликонов. В кислой среде образуют соли от розовой до малиновой окраски, в щелочной, выступая как анионы, дают соли оливково-зеленого цвета. Способны образовывать соли с металлами. Соли Ca, Mg – синей окраски, K – от пурпуровой до черно-фиолетовой. Содержатся в плодах черники, цветках василька синего, траве фиалки трехцветной. Гликозиды антоцианидинов называют антоцианами, например, цианин – 3,5-диглюкозид цианидина - содержится в цветках василька синего.
4. Флаваноны (флаван- 4-оны). Выделено около 30 агликонов. Небольшая группа флавоноидов, в основе структуры которых лежит нестойкое дигидро- гамма -пироновое кольцо. В присутствии щелочей кольцо раскрывается, и образуются халконы. Обнаружены в семействах розоцветных, бобовых и сложноцветных. а) Ликвиритигенин – 7,4´-дигидроксифлаванон и его 4´-глюкозид – ликвиритин содержатся в корнях солодки.
б) Нарингенин – 5,7,4´-тригидроксифлаванон и его 5-моногликозиды – салипурпозид и гелихризин содержатся в цветках бессмертника песчаного.
в) Эриодиктиол – 5,7,3´,4´-тетрагидроксифлаванон и его 7-биозид – 7-рамноглюкозид эриоцитрин; гесперитин – 5,7,3´-тригидрокси-4´-метоксифлаванон и его 7-биозид – рамноглюкозид гесперидин (экзокарпий плодов цитрусовых).
5. Флаванонолы (флаванон-3-олы). Отличаются от флаванонов наличием гидроксильной группы при С3 и, подобно катехинам, содержат два асимметрических атома углерода в молекуле. Они очень лабильны и поэтому в растениях не накапливаются в значительных количествах.
Таксифолин (дигидрокверцетин) и аромадендрин (дигидрокемпферол) встречаются редко и очень быстро окисляются. Содержатся в древесине хвойных (ель, сосна, лиственница) и лиственных (эвкалипт, бук, вишня) деревьев, а также в хвощах (трава хвоща полевого).
Окисленные (производные флавона) делятся на 2 группы.
6. Флавоны. Выделено около 20 агликонов. а) Апигенин – 5,7,4´-тригидроксифлавон и его 5-гликозиды.
7-глюкозид-4´-кислота пара -кумаровая апигенина – квинквелозид содержится в траве пустырника. 8-С-глюкозид апигенина – витексин содержится в плодах боярышника и траве фиалки. б) Лютеолин – 5,7,3´,4´-тетрагидроксифлавон и его 5-гликозиды.
Апигенин и лютеолин в виде 5-гликозидов содержатся в траве хвоща полевого, сушеницы топяной, череды трехраздельной, в цветках пижмы обыкновенной и бессмертника песчаного. в) Байкалеин – 5,6,7-тригидроксифлавон и его гликозид – 7-кислота глюкуроновая – байкалин содержатся в корнях шлемника байкальского.
г) Скутелляреин - 5,6,7,4´-тетрагидроксифлавон и его 7-гликозид – 7-кислота глюкуроновая - скутеллярин содержатся в корнях шлемника байкальского.
7. Флавонолы (флавон-3-олы). Наиболее многочисленная и широко распространенная группа. Выделено около 210 агликонов, из них самые распространенные – кемпферол и кверцетин. а) Кемпферол – 3,5,7,4´-тетрагидроксифлавон, или 5,7,4´ тригидроксифлавонол-3.
Эквизетрин – 7-фруктозо-арабинозид кемпферола содержится в траве хвоща полевого. б) Кверцетин – 3,5,7,3´,4´-пентагидроксифлавон, или 5,7,3´,4´-тетрагидроксифлавонол-3. В виде агликона содержится в траве астрагала шерстистоцветкового.
Гликозиды кверцетина: · рутин – 3-рутинозид (глюкорамнозид) кверцетина содержится в траве фиалки, пустырника, горца перечного, зверобоя, плодах и бутонах софоры японской, плодах аронии (рябины) черноплодной; · авикулярин – 3-арабинозид кверцетина содержится в траве спорыша (горца) птичьего; · гиперозид – 3-галактозид кверцетина содержится в траве зверобоя, горца почечуйного, цветках и плодах боярышника; · кверцитрин – 3-рамнозид кверцетина содержится в траве спорыша (горца) птичьего, цветках боярышника.
III. Также выделяют группы флавоноидов:
а) с разорванным гетероциклом:
8,9. Халконы и дигидрохалконы. Встречаются совместно с флаванонами. а) Бутеин – 5,7,3´,4´-тетрагидроксихалкон содержится в траве череды в свободном виде и в виде гликозидов.
б) Изоликвиритигенин – 7,4´-дигидроксихалкон и его 4´-глюкозид – изоликвиритин содержатся в корнях солодки.
б) с пятичленным гетероциклом:
10. Ауроны. Распространены в основном у представителей семейств сложноцветных, бобовых и норичниковых. Сульфуретин и его 7-глюкозид содержатся в траве череды.
IV. Изофлавоноиды в растениях встречаются, в основном, как производные изофлавона. Гинестеин – 5,7,4´-тригидроксиизофлавон и даидзеин – 7,4´-дигидроксиизофлавон содержатся в створках плодов фасоли, корнях стальника полевого и других растениях семейства Fabaceae. Формононетин – 7-гидрокси-4´-метоксиизофлавон и его 7-глюкозид ононин содержатся в корнях стальника полевого.
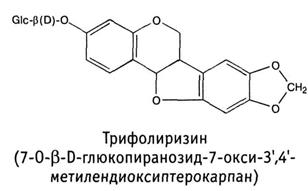
К изофлавоноидам также относится достаточно специфическая группа соединений – птерокарпаны, образованные замыканием связи между орто -положением кольца В и карбонильным кислородом, при этом возникает дополнительный пятичленный цикл. Примером может служить трифолиризин, найденный в стальнике полевом.
V. Другиеклассы флавоноидов: 1. Ксантоны – класс природных соединений, имеющих структуру дибензо- гамма -пирона. Название происходит от греч. «xanthos» - желтый, так как природные производные ксантона имеют желтую или кремовую окраску. Первый представитель этого ряда – генцизин – выделен из горечавки желтой в 1921 г. В настоящее время насчитывается до 300 выделенных из растений ксантоновых производных. Встречаются в свободном виде и в виде О- и С-гликозидов преимущественно в семействах горечавковых, зверобойных и некоторых других.
Ксантон
Наиболее широко распространен в растительном мире С-гликозид мангиферин (плоды манго, трава золототысячника, трава копеечника альпийского).
2. Флаволигнаны – силибин, силидианин, силихристин содержатся в плодах расторопши пятнистой (см. раздел «Лигнаны»).
Физико-химические свойства
Физические свойства. Катехины, лейкоантоцианидины, флаванонолы, изофлавоны - бесцветные; флаваноны, флавоны, флавонолы - желтые; халконы и ауроны - оранжевые; антоцианидины в зависимости от реакции среды красные, синие или фиолетовые аморфные или кристаллические вещества, без запаха, горького вкуса, с определенной температурой плавления (гликозиды - 100-180 ºС, агликоны - до 300 ºС). Гликозилированные формы флавоноидов, катехины и лейкоантоцианидины хорошо растворимы в воде, этаноле и метаноле различной концентрации, нерастворимы в органических растворителях (диэтиловом эфире, хлороформе, ацетоне). Свободные агликоны, за исключением катехинов и лейкоантоцианидинов, нерастворимы в воде, но хорошо растворимы в этаноле, метаноле и других органических растворителях (диэтиловом эфире, хлороформе, ацетоне). Все флавоноиды хорошо растворимы в пиридине, диметилформамиде и щелочах. Все флавониды оптически активны, способны флуоресцировать в УФ-свете, имеют характерные УФ-спектры, характеризующиеся наличием двух максимумов поглощения, и ИК-спектры. Химические свойства. Химические свойства обусловлены особенностью строения флавоноидов: наличием ароматических, пиранового или пиронового колец, функциональных групп. 1. Гликозиды подвергаются ферментативному и кислотному гидролизу до агликонов и сахаров. O-гликозиды гидролизуются более или менее легко при действии разбавленных минеральных кислот и ферментов. С-гликозиды с трудом расщепляются только в жестких условиях при действии крепких кислот (кислоты концентрированные хлористоводородная или уксусная) или их смесей (смесь Килиани) при длительном нагревании. 2. Благодаря кольцам А и В флавоноиды способны: · образовывать комплексные соединения с солями металлов (железа, алюминия, циркония). С солями железа - в зависимости от количества гидроксильных групп от зеленой и синей до коричневой окраски; с солями алюминия – желтой окраски, с желто-зеленой флуоресценцией; · вступать в реакцию азосочетания с солями диазония с образованием азокрасителей. 3. Флавоноиды, содержащие пироновый цикл (флавоны и флавонолы), способны: · восстанавливаться в кислой среде атомарным (свободным) водородом, полученным в результате реакции взаимодействия кислоты с металлическим магнием или цинком, до антоцианидинов (проба Шинода, или цианидиновая проба); · растворяться в щелочах с образованием растворимых в воде фенолятов. 4. Флавоноиды, содержащие пирановый цикл (катехины, лейкоантоцианидины), способны легко окисляться до производных флавона и флавонола. 5. Флавоноиды при сплавлении в жестких условиях со щелочью распадаются на составные части, что используется для установления их структуры. Физические и химические свойства используются в анализе сырья на подлинность и доброкачественность. Способы получения
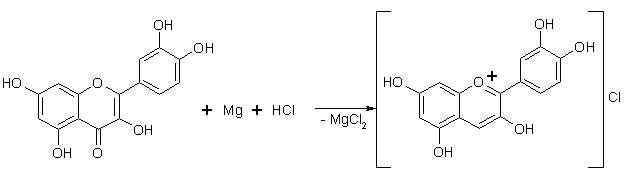
Для выделения флавоноидов проводят экстракцию растительного материала этанолом. Спиртовое извлечение упаривают, к остатку добавляют горячую воду и после охлаждения удаляют неполярные соединения (хлорофилл, жирные и эфирные масла и др.) из водной базы хлороформом или четыреххлористым углеродом. Для выделения отдельных флавоноидов существуют специфические методы. Качественные реакции Специфических реакций для всех групп флавоноидов не существует. Наиболее часто используют следующие реакции. 1. Цианидиновая проба (проба Шинода). Флавоноиды при восстановлении атомарным водородом в присутствии магния (или цинка) и кислоты концентрированной хлористоводородной образуют характерное окрашивание. Реакция очень чувствительна, основана на восстановлении карбонильной группы и образовании антоцианидинов. Для проведения реакции 1 г порошка сырья заливают 10 мл 95 % этанола, нагревают на водяной бане до кипения и настаивают 3-4 часа. Спиртовое извлечение фильтруют, упаривают до объема 2 мл, делят пополам и разливают в 2 пробирки; в каждую пробирку прибавляют по 3 капли кислоты концентрированной хлористоводородной. В первую пробирку добавляют 0,03-0,05 г магниевой или цинковой пыли и нагревают на водяной бане до кипения. Жидкость окрашивается в красный или ярко-розовый цвет. Во второй пробирке окрашивание отсутствует. Флавоны дают оранжево-красные, флавонолы от розовой до малиновой окраски соли.
Кверцетин Цианидина хлорид
Антоцианидины, халконы и ауроны в кислой среде сразу дают окрашенные оксониевые соли. Цианидиновая реакция приводится в ГФ ХI для установления подлинности цветков бессмертника песчаного. 2. Проба Брианта. Проводится при положительной цианидиновой реакции и является ее модификацией. Эта проба дает возможность сделать заключение о присутствии в сырье гликозидов и (или) агликонов. В пробирку, где проводилась проба Шинода, добавляют октанол и встряхивают. Если: · окраска перешла в органический слой - в сырье содержатся только агликоны, которые растворимы в октаноле; · окраска осталась в водной фазе - в сырье присутствуют только гликозиды; · окрасились оба слоя - в сырье присутствуют флавоноиды как в виде гликозидов, так и в виде агликонов. 3. Реакция с солями железа (III). С железа окисного хлоридом образуются комплексные соединения, окрашенные в черно-синий цвет, если флавоноиды – тригидроксипроизводные, и в зеленый - если дигидроксипроизводные. 4. Реакция с 2-5 % спиртовым раствором алюминия хлорида. Флавоноиды, имеющие две гидроксигруппы у С3 и С5, образуют хелатные комплексы за счет водородных связей, возникающих между карбонильной и гидроксильными группами и ионом алюминия, имеющие желтый цвет с желто-зеленой флуоресценцией. Эта реакция приведена в ГФ XI для подтверждения подлинности сырья зверобоя, горца перечного и спорыша птичьего. Аналогично образуются комплексы с солями циркония. 5. Реакция с 1 % раствором основного свинца ацетата. Антоцианидины дают синий аморфный осадок. Флавоны, халконы и ауроны - осадки ярко-желтого цвета. 6. Реакция с 10 % спиртовым раствором щелочи. Флавоны, флавонолы, флаваноны и флаванонолы растворяются в щелочах с образованием фенолятов желтого цвета, при нагревании окраска изменяется до оранжевой или коричневой. Халконы и ауроны при взаимодействии со щелочами обычно дают красное или ярко-желтое окрашивание. Антоцианидины образуют со щелочами соли от синего до оливково-зеленого цвета. 7. Реакция азосочетания с диазосоединениями (кислота сульфаниловая или пара -нитроанилин).Образуетсяазокраситель оранжевого, красного или вишнево-красного цвета. 8. Борно-лимонная реакция с реактивом Вильсона (по 0,5 г кислот борной и лимонной в метаноле). Реакция отличия флавоноидов от фуранохромонов. Флавоноиды дают с кислотой борной комплексы желтой окраски с ярко-желтой флуоресценцией, которые не разрушаются кислотой лимонной. Фуранохромоны со смесью кислот борной и лимонной не реагируют.
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 797; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.54.190 (0.009 с.) |


 Лейкоцианидин
Лейкоцианидин
 Цианидин
Цианидин
 Цианин
Цианин
 Ликвиритигенин
Ликвиритигенин
 Ликвиритин
Ликвиритин
 Нарингенин
Нарингенин
 Эриодиктиол
Эриодиктиол
 Гесперитин
Гесперитин
 Таксифолин
Таксифолин
 Апигенин
Апигенин
 Лютеолин
Лютеолин
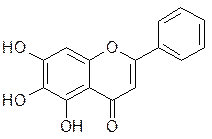 Байкалеин
Байкалеин
 Скутелляреин
Скутелляреин
 Кемпферол
Кемпферол
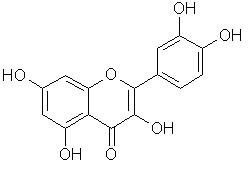 Кверцетин
Кверцетин
 Бутеин
Бутеин
 Изоликвиритигенин
Изоликвиритигенин
 Сульфуретин
Сульфуретин
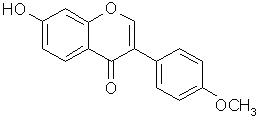 Формононетин
Формононетин

 Мангиферин
Мангиферин
 Силибин
Силибин