Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Обработка результатов эксперимента. Диаметр частиц, мм -Содержание книги
Поиск на нашем сайте
Адсорбент - Диаметр частиц, мм - Навеска адсорбента (m), г - Свободный объём системы по гелию (V св), см3 - Температура ампулы с адсорбентом в термостате, °С - Температура нитрометра, °С - Барометрическое давление, мм рт. ст - Газ - Исходный объём газа в нитрометре V исх, см3 - Объём газа в нитрометре за вычетом свободного объёма системы: V = V исх- V св Объём адсорбированного газа при 298 К и 760 мм рт. ст. (Δ V, см3)вычисляют по формуле: Результаты измерений заносят в табл. 3.1. Таблица 3.1 Экспериментальные результаты
Аналогичные измерения и обработку результатов проводят с использованием в качестве рабочего газа кислорода. По результатам измерений строятся кинетические кривые адсорбции Вопросы для самоконтроля 1. В чём суть волюмометрического метода измерении адсорбции газов? 2. В чём заключается предварительная подготовка адсорбента перед адсорбционными измерениями? 3. Как определяются кинетическая кривая, степень отработки адсорбционной ёмкости, величина равновесной емкости адсорбента, значение коэффициента внутренней диффузии?
ТЕРМИЧЕСКИЙ АНАЛИЗ Теоретическая часть Термический анализ является одним из важнейших методов физико-химического исследования веществ [22-26]. При воздействии высоких температур протекают химические реакции (дегидратация, разложение и т.д.) и физические превращения (плавление, полиморфные переходы и т.д.). Термический анализ широко используется при исследовании твёрдофазных процессов, реакций термического разложения и фазовых превращений веществ. В основе метода лежит зависимость физических или химических свойств материалов от температуры. В зависимости от измеряемого параметра различают основные методы исследований: – дилатометрия – измерение линейных и объемных размеров материалов; – дифференциально-термический анализ (ДТА) – определение разности температур между образцом и эталоном; – дифференциально-сканирующая калориметрия (ДСК) основана на непрерывной регистрации разности теплового потока от образца и эталона как функции температуры; – термогравиметрический анализ (ТГА) – определение величины и характера изменения массы образца в условиях программируемого подъема температуры; – синхронный термический анализ предполагает одновременное использование термогравиметрии и дифференциальной сканирующей калориметрии (ТГА/ДСК) или термогравиметрии и дифференциально-термического анализа (ТГА/ДТА). Наиболее широко применяются термогравиметрический и дифференциально-термический анализы. Термогравиметрический метод анализа основан на регистрации изменения массы образца при повышении температуры. Изменение массы твёрдых тел обусловлено протекающими физико-химическими процессами. Для процессов разложения и диссоциации характерно уменьшение массы образца, для реакции окисления, напротив − увеличение массы. Установка для термогравиметрических исследований состоит из термовесов, предназначенных для непрерывной регистрации изменений массы, печи, в которую помещен образец, термопары и программного регулятора температуры. Термогравиметрический анализ (ТГА) заключается в измерении зависимости массы твердого образца от температуры среды, в которую он помещен. Кривая зависимости потери массы от температуры (кривая ТГ, рис. 4.1) имеет вид плато, горизонтальный участок которой говорит об устойчивости химического соединения в данном интервале температур и отсутствии химических превращений (при этом физические превращения не исключаются), вертикальный участок на кривой свидетельствует о химическом разложении материала.
Рис. 4.1. Термогравиметрическая кривая (ТГ) разложения кристаллогидрата оксалата кальция
На основании кривой ТГ можно определить потерю массы при нагревании (Δ m), что позволяет оценить содержание примесей в анализируемом материале. Для этого необходимо знать состав химического соединения, относящегося к данному температурному плато, и состав продукта разложения. К сожалению, кривая ТГ не позволяет точно определить температуру разложения (истинную температуру химической реакции). Температуру химической реакции можно с высокой точностью определить, если воспользоваться дифференциальной формой записи, показывающей скорость изменения массы образца Возможны следующие варианты методов исследований: изотермический, когда масса образца изменяется на протяжении некоторого времени при выбранной температуре, квазистатический, когда образец нагревается при каждой из ряда возрастающих температур до достижения постоянного значения массы, и динамический, когда температура среды, окружаемой нагреваемый образец, изменяется по заданному закону. Из большого числа различных типов химических реакций наиболее хорошо изучены реакции разложения, на протекание которых в статических условиях в значительной степени влияют давление и состав газовой фазы, а в проточных системах – гидродинамические условия. Для определения состава газовой фазы используют химические и инструментальные методы анализа. Для этого должен быть предусмотрен непосредственный контакт ячейки с измерительным прибором (манометром или газовой бюреткой). Для определения количественного состава газовой фазы часто прибегают к вымораживанию, поглощению или превращению продуктов в легко анализируемую форму. Метод дифференциального термического анализа (ДТА) основан на сравнении термических свойств образца исследуемого вещества и термически инертного эталона, в качестве которого применяются вещества, не претерпевающие никаких изменений при нагревании до требуемой температуры. В качестве эталонов применяются прокаленные оксиды алюминия или магния. В данном случае регистрируемым параметром служит разность температур, измеряемая при нагревании или охлаждении образца и эталона с постоянной скоростью. ДТА-кривая получается с помощью дифференциальной термопары (рис. 4.2).
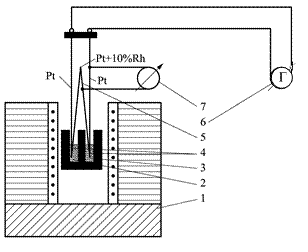
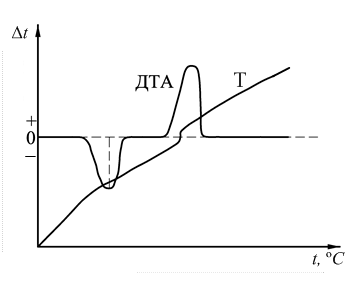
Рис. 4.2. Схема дифференциальной и простой термопар: 1– электропечь; 2 – исследуемое вещество; 3 – эталонное вещество; 4 – горячие концы дифференциальной термопары; 5– холодный спай дифференциальной термопары; 6 – гальванометр записи кривой ДТА; 7 – гальванометр записи температурной кривой. Дифференциальная термопара представляет собой две обычные термопары, соединенные между собой одноименными концами, образующими холодный спай. Два других конца подключены к прибору, позволяющему фиксировать изменения в цепи электродвижущей силы (ЭДС), возникающей при нагревании горячих спаев термопары. Один горячий спай помещён в исследуемое вещество, а другой в эталонное. Схематическое изображение простой (Т) и дифференциальной (ДТА) кривых нагревания приведено на рис. 4.3. Нулевой линией называется параллельная оси абсцисс линия, проведенная через начало хода кривой ДТА. Часто после завершения процесса разложения кривая ДТА не возвращается к нулевой линии, а идет параллельно ей или под некоторым углом. Эта линия хода термической кривой носит название базисной линии. Расхождение базисной и нулевой линий обусловлено различными теплофизическими свойствами исследуемого и эталонного веществ.
Рис. 4.3. Схематическое изображение простой (Т) и дифференциальной (ДТА) кривых нагревания
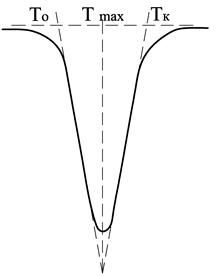
Экстремумы (пики) на кривой ДТА на базисной линии соответствуют термическим эффектам. Так, эндотермические превращения отображаются отклонением кривой ДТА ниже нулевой линии, экзотермические – выше нулевой линии. Первые обычно обозначаются знаком минус, вторые – плюс. Положение термических эффектов на термограмме кривой ДТА характеризуется температурными границами протекания реакции. Значение температур определяют графически, снося соответствующие точки с кривой ДТА на простую температурную кривую, а затем на ось температур. Устанавливают температуры начала Т 0, максимума Т max и окончания термического эффекта Тк (рис. 4.4). За начало процесса принимается температура Т 0, при которой кривая ДТА отклоняется от нулевой линии, фиксируя эндо- или экзотермический пик. При расшифровке результатов анализа часто указывают не начало и конец реакции, а интервал температур, в котором она протекает, т.е. Т 0 – Тк, или температуру максимума термического эффекта Т mах. Последнюю устанавливают как точку пересечения касательных к правой и левой ветвям пика.
Рис. 4.4. Определение температур начала, конца и максимума термического эффекта
Вследствие трудностей, связанных с графическим определением температуры начала реакции, наиболее надёжной характеристикой является температура Т mах. Изменения температуры образца вызываются физическими переходами или химическими реакциями, связанными с изменением энтальпии. К ним относятся фазовые переходы, плавление, перестройка кристаллической структуры, реакции дегидратации и разложения, разрушение кристаллической решётки и др. В общем случае фазовые переходы, дегидратация, восстановление и некоторые реакции разложения сопровождаются эндотермическими эффектами, а кристаллизация, окисление и отдельные процессы термолиза – экзотермическими эффектами.
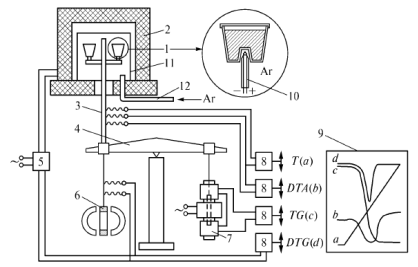
Дериватография Дериватография (от лат. derivatus – отведённый, отклонённый и греч. grapho – пишу) –комплексный метод исследования химических и физико-химических процессов, происходящих в твёрдом теле в условиях программного подъема температуры, получивший в настоящее время широкое распространение. Дериватография основана на сочетании дифференциального термического анализа с другими физико-химическими методами: термогравиметрией, масс-спектрометрией и т.д. Дериватографом называется прибор, совмещающий термогравиметрический и дифференциальный термический анализы. При проведении дериватографических исследований регистрируются четыре кривые (рис. 4.5): – зависимость температуры от времени носит линейный характер и показывает скорость нагрева образца (Т); – термогравиметрическая кривая показывает зависимость изменения массы от температуры нагрева образца (ТГ); – кривая дифференциально-термического анализа отражает тепловые эффекты процессов, происходящих при нагревании вещества (ДТА); – дифференциально-термогравиметрическая кривая отражает скорость изменения массы образца (ДТГ). Основным отличием дериватографа от других термических установок является тождественность условий опыта, что достигается путем одновременной регистрации всех кривых на одном листе для одной и той же навески при соответствующих одинаковых температурах нагрева. Совместное получение простой и дифференциальной кривых даёт возможность обнаружить и количественно оценить даже очень слабые эффекты потери массы в изучаемом веществе. Дериватограф Q-1500D позволяет проводить термогравиметрические исследования при нагревании образца до 1500 оС, а также квазитермические и квазиизобарные измерения при температурах до 100 оС. Такие измерения обеспечивают значительно большую селективность по сравнению с традиционными измерениями, при которых нагрев печи производится по линейному закону. При этом происходит удлинение температурного интервала разложения, вызываемое прежде всего перепадом температуры внутри пробы, что несомненно является следствием динамического нагревания печи. Такое явление особенно ярко проявляется при нагреве с высокой скоростью. Однако при медленном нагреве или при изотермическом исследовании значительно реже проявляются погрешности. Желаемый нагрев со скоростью 0,1-0,2 град/мин в практических условиях неосуществим вследствие высокой продолжительности опыта. Решение этой проблемы даёт Q - дериватография. Квазитермический режим предусматривает нагрев образца с большой скоростью (2-5 град/мин) до момента разложения, затем нагрев прекращается. Регулирование температуры производится таким образом, чтобы изменение массы образца происходило с очень малой скоростью, величина которой задается путем изменения порога чувствительности усилителя. Схема устройства дериватографа Q-1500D приведена на рис. 4.5.
Рис. 4.5. Принципиальная схема дериватографа Q-1500D: 1 − тигель с исследуемым образцом; 2 − печь; 3 − керамическая трубка с термопарами; 4 − весы; 5 − программатор нагрева; 6 − датчик скорости изменения массы; 7 − датчик изменения массы; 8 − усилители выходного сигнала; 9 − дериватограммма; 10 − термопара; 11 − защитный кварцевый стакан; 12 − подвод инертного газа; a – изменение температуры эталона (Т); b – запись дифференциального термического анализа (ДTA); с – изменение массы образца (TГ); d – скорость изменения массы образца (ДТГ) Важнейшей частью дериватографа является термовесовой блок, в котором располагаются равноплечные аналитические весы 4, снабженные пневмозатухающим устройством. На одном плече весов находятся на керамическом стержне с термоэлементом 1 два тигля, в одном из которых находится исследуемый образец, а в другом − инертное вещество. Устройство тигля изображено на поз. 10. Внутри тигля имеется термопарный чехол для регистрации температуры внутри образца. Керамическая трубка с тиглем в процессе работы помещается в печь 2, подъём и опускание которой производятся автоматически. Режим работы дериватографа, а именно, скорость нагрева, задаётся с помощью программатора нагрева 5. Изменение массы регистрируется с помощью датчика изменения массы 7. Определение скорости изменения массы производится с помощью дифференциального трансформатора – датчика скорости изменения массы 6, который преобразует движение плеча весов в соответствующий электрический сигнал. Затем с помощью усилителей выходного сигнала 8 информация преобразовывается в дериватограмму 9, на которой представлено одновременно четыре кривых (Т, ДТА, ТГ, ДТГ). В зависимости от условий опыта возможно проведение термического анализа в инертной среде, например в аргоне, для чего в приборе предусмотрен ввод инертного газа 12. Иногда для температурной стабилизации и уменьшения градиента температур используют защитный кварцевый стакан 11. Особое внимание необходимо уделить рассмотрению влияния скорости нагревания на наблюдаемую температуру разложения образца. В результате многочисленных исследований показано, что наблюдаемые значения температуры разложения различаются при медленном и быстром нагреве. В последнем случае имеет место повышение наблюдаемой температуры разложения. При протекании нескольких последовательных реакций при медленном нагреве их удается разделить.
|
||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 251; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.105.46 (0.008 с.) |

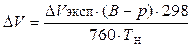 (3.12)
(3.12)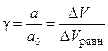
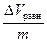 (см3/г) и коэффициенты разделения смеси азота и кислорода (m - масса адсорбента). На кинетических кривых для γ = 0,5 находят значения времени отработки ёмкости адсорбента на 50 % (t 0,5) и вычисляют эффективные коэффициенты диффузии De (см2/с):
(см3/г) и коэффициенты разделения смеси азота и кислорода (m - масса адсорбента). На кинетических кривых для γ = 0,5 находят значения времени отработки ёмкости адсорбента на 50 % (t 0,5) и вычисляют эффективные коэффициенты диффузии De (см2/с): (3.12)
(3.12)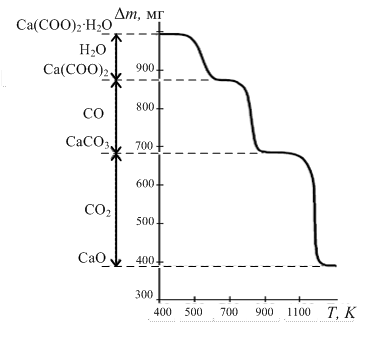
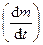 от времени нагрева t. Каждый пик на дифференциальной кривой ДТГ соответствует максимальной скорости изменения массы, т.е. истинной температуре химической реакции.
от времени нагрева t. Каждый пик на дифференциальной кривой ДТГ соответствует максимальной скорости изменения массы, т.е. истинной температуре химической реакции.