Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение изотермы адсорбции азота при высоком давленииСодержание книги
Поиск на нашем сайте
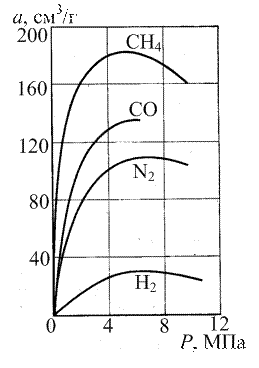
Приборы и реактивы: − объемная установка для измерения величины адсорбции под давлением; − адсорбент – цеолит NaX; − адсорбтив – азот технический из баллона; − калибровочный газ – гелий марки А из баллона. Цель работы. Измерение равновесной адсорбции азота на цеолите NaX под давлением. Сущность работы. Адсорбция слабо сорбирующихся газов (таких как азот, кислород, водород, метан, СО и др.) имеет определенную специфику. Чтобы повысить адсорбционную способность адсорбента по этим веществам, их адсорбцию часто проводят при высоком давлении. Изотермы адсорбции этих веществ имеют линейный начальный участок, который описывается уравнением Генри. Далее изотермы проходят через максимум и имеют ниспадающую ветвь. Такие изотермы называются изотермами избыточной адсорбции. Пример изотерм избыточной адсорбции газов на микропористом активном угле при 20 оС приведен на рис. 2.13 [1].
Рис. 2.13. Изотермы избыточной адсорбции газов на микропористом активном угле при 20 оС Ниспадающая ветвь изотермы отражает тот факт, что при расчёте из экспериментальных данных, полученных объемным методом, определяется так называемая избыточная величина адсорбции, соответствующая разности между общим объёмом адсорбированного газа и объёмом газа, сжатого в свободном пространстве (свободном объёме). Рост плотности газа в свободном пространстве по мере увеличения давления и приводит к снижению избыточной величины адсорбции. Таким образом, избыточная адсорбция совпадает с Гиббсовым определением адсорбции и Гиббсовым избытком Г [1,19]. Полная и избыточная адсорбции связаны как где ρ а – плотность газа в адсорбированном состоянии; ρг – плотность газа в газовой фазе при заданном давлении. Значения ρг приводятся в справочной литературе; величину ρ а можно определить по методу Дубинина–Николаева [1].
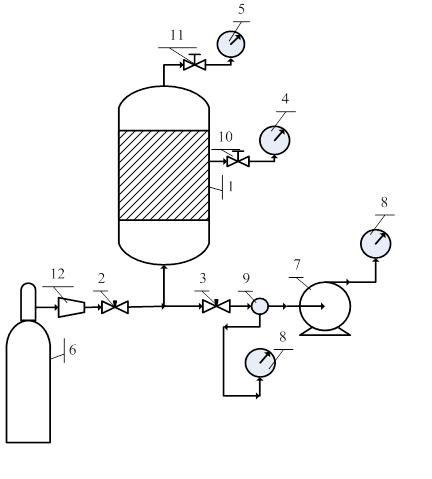
Методика проведения эксперимента Схема экспериментальной установки для исследования равновесной адсорбции газов под давлением приведена на рис. 2.14. Основным аппаратом установки является металлический адсорбер 1 с крышками, снабженный манометром 4 и вакууметром 5.
Перед загрузкой исследуемый адсорбент дегидратируют при 350-400 оС в токе азота и горячим засыпают в адсорбер 1. Установку проверяют на герметичность. Затем определяют свободный объём системы, который включает в себя объём пустот между гранулами адсорбента и объём пор адсорбента. Его определяют с помощью гелия, практически не адсорбирующегося при комнатной температуре. Измерение свободного объёма системы по гелию При закрытых кранах 2 и 10 и открытых кранах 3 и 11 с помощью вакуум-насоса 7 из адсорбера откачивают воздух до остаточного давления
Рис. 2.14. Схема экспериментальной установки: 1 – адсорбер; 2,3,10,11 – краны; 4 – манометр; 5 – вакуумметр; 6 – баллон с азотом (гелием); 7 – вакуумный насос; 8 – газосчётчик; 9 – переходник; 12 – редуктор краны 2, 10 закрывают, и открывают кран 3, откачивают гелий из адсорбера 1 при помощи вакуум-насоса 7. После остановки стрелки газосчётчика 8 открывают кран 11 и регистрируют показания вакуумметра 5 и газосчётчика 8. Аналогичные действия проводят при других значениях давления. После определения величины свободного объёма системы, его значение приводят к нормальным условиям. Результаты оформляют следующим образом: Адсорбент - Объём адсорбента, л - Температура, °С - Барометрическое давление, мм рт.ст. - Газ – гелий Таблица 2.6 Результаты измерений
По результатам измерений строят калибровочную кривую зависимости свободного объёма системы от давления V св = f(P). Измерение изотермы адсорбции азота При закрытых кранах 2 и 10 и открытых кранах 3 и 11 с помощью вакуум-насоса 7 из адсорбера 1 откачивают воздух до остаточного давления
Замерив объём десорбированного газа при давлении в адсорбере, равном 1 ата, подсоединяют газосчётчик 8 к выхлопу вакуум-насоса, открывают кран 3 при закрытых кранах 2 и 10 и откачивают газ из адсорбера при помощи вакуум-насоса 7, замеряя объём десорбата (кран 12 открыт). Все значения давления в адсорбере и соответствующие им показания газосчётчика (величины объёма десорбата) регистрируют. При обработке результатов эксперимента вводят поправку на свободный объём системы. Результаты записывают в табл. 2.7.
Адсорбент - Объем адсорбента, л - Температура, °С - Барометрическое давление, мм рт.ст. - Газ - азот Таблица 2.7 Результаты измерений
По результатам измерений строят изотерму адсорбции a= f(P).
Вопросы для самоконтроля 1. Каким уравнением описываются изотермы адсорбции компонентов воздуха при комнатной температуре? 2. Какова методика волюмометрического определения изотерм адсорбции при повышенных давлениях? 3. Каковы особенности волюмометрического метода при измерениях при повышенном давлении?
Лабораторная работа 6 Определение изотермы адсорбции фенола из водных растворов на активном угле методом переменных концентраций Приборы и реактивы: − адсорбент – активный уголь; − адсорбтив – фенол; − бюксы стеклянные; − пробирки с пришлифованными пробками – 10 шт; − шейкер; − центрифуга; − спектрофотометр. Цель работы. Освоение метода переменных концентраций и определение изотермы адсорбции фенола из водных растворов на активном угле. Сущность работы. Метод измерения величины адсорбции в зависимости от относительной концентрации вещества в растворе заключается в определении разности концентраций адсорбтива в исходном и равновесном растворах. При использовании метода переменных концентрацийнесколько пробирок или колб (7-10 шт.) с навесками подготовленного адсорбента заливают растворами с различной концентрацией адсорбтива при соотношении Известно, что адсорбция на углеродных адсорбентах в значительной мере зависит от ряда факторов: концентрации адсорбтива, рН раствора, электронодонорных или электроноакцепторных свойств адсорбтива, пористости и поверхностных свойств адсорбента, которые связаны с присутствием окисленных функциональных групп и их поверхностного заряда. Для того чтобы получить надёжные данные по адсорбции фенола, необходимо фиксировать все параметры, которые могут оказывать влияние на процесс адсорбции.
Порядок проведения работы Предварительные эксперименты: − определение времени установления равновесия в системе фенол − активный уголь; − калибровка спектрофотометра (методика проведения калибровки приведена ниже). Подготовка адсорбента Подготовка адсорбента заключается в очистке его поверхности от различных адсорбированных им паров и газов, а также от паров воды, которые могли быть поглощены из воздуха. Для этого образец активного угля в виде порошка прогревают в сушильном шкафу при температуре 100 оС. По достижении постоянной массы (примерно через 2 ч) бюкс с образцом вынимают из сушильного шкафа. После охлаждения бюкса в эксикаторе с цеолитом, бюкс с образцом взвешивают и определяют навеску угля. Навески адсорбента (10 шт.) взвешивают на аналитических весах (~ 0,1 г). Каждая навеска (m, г) загружается в заранее приготовленные колбы или пробирки, куда заливают растворы адсорбтива. Приготовление растворов Рассчитывают количество фенола, необходимое для приготовления раствора исходя из предельной растворимости. Предельную растворимость находят по справочным данным [17]. Растворимость фенола в воде при 18 оС составляет 0,88 моль/л. Рассчитанное количество фенола взвешивают на аналитических весах и в мерной колбе растворяют в дистиллированной воде, после чего доводят до метки и перемешивают до полного растворения вещества. Последующие растворы готовят методом разбавления исходного раствора. Начальные концентрации приготовленных растворов с 0 составляют от 5 до 30 ммоль/л.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 223; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.19.218.250 (0.009 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 , (2.17)
, (2.17)