Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Часть 2. Молекулярная Физика.Содержание книги
Поиск на нашем сайте
Лабораторная работа №100 Оптические методы измерения размеров молекул различных жидкостей и определения различных характеристик их теплового движения Оптические характеристики прозрачных сред тесно связаны с внутренним строением вещества среды. Взаимодействие световой волны с веществом (явления дисперсии и молекулярной рефракции) позволяют связать макроскопические характеристики вещества с размерами его молекул. Из курса оптики известна формула Лоренца:
где
Опытные данные свидетельствуют о том, что молекулярная рефракция
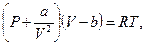
где P – давление газа;
При фазовом переходе от жидкой фазы к газообразной изменяется среднее расстояние между молекулами, но не размеры самих молекул. Если считать молекулы шариками с некоторым эффективным средним радиусом
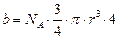
где Таким образом:
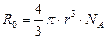
Для оценки эффективного радиуса молекул справедлива формула:
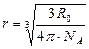
Порядок выполнения работы
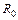 , а затем по формуле (2.5) — эффективный радиус молекул , а затем по формуле (2.5) — эффективный радиус молекул 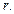 Экспериментальные данные и результаты расчетов заносятся в табл. 2.1. Экспериментальные данные и результаты расчетов заносятся в табл. 2.1.
2. При фазовом переходе от жидкой фазы к газообразной изменяется среднее расстояние между молекулами, но не размеры самих молекул. Этот факт позволяет по измеренным значениям радиусов молекул рассчитать среднюю длину свободного пробега Расчет выполняется по формулам:
где
Вычисление производится для значений давления и температуры, соответствующих условиям проведенного опыта. 3. Расчет погрешностей в данной работе не производится, поскольку определение величин производится по оценочным (приблизительным) формулам. Контрольные вопросы 1. На чём основан используемый способ измерения размеров молекул? 2. С какой точностью определяются размеры молекул? 3. Каков физический смысл величин 4. Как распределены молекулы по скоростям? 5. Можно ли до опыта предсказать, у какой молекулы воды или спирта эффективный радиус будет больше?
Лабораторная работа № 107
|
|||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 317; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.83.38 (0.009 с.) |

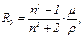
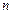 — показатель преломления;
— показатель преломления;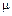 — молярная масса;
— молярная масса;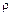 — плотность вещества;
— плотность вещества;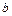 в уравнении Ван-дер-Ваальса для другого фазового состояния вещества — газообразного. Уравнение состояния реального газа имеет вид:
в уравнении Ван-дер-Ваальса для другого фазового состояния вещества — газообразного. Уравнение состояния реального газа имеет вид: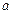 — поправка на межмолекулярное взаимодействие;
— поправка на межмолекулярное взаимодействие;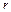 , то оказывается, что
, то оказывается, что 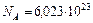
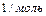 — число Авогадро.
— число Авогадро.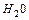
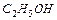
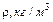
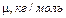
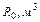
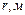
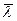 , среднюю скорость хаотического движения молекул
, среднюю скорость хаотического движения молекул 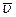 и коэффициент диффузии D молекул водяного пара и спирта.
и коэффициент диффузии D молекул водяного пара и спирта.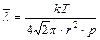

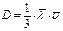
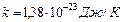 — постоянная Больцмана;
— постоянная Больцмана;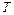 — термодинамическая температура, взять 293К;
— термодинамическая температура, взять 293К;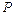 — атмосферное давление, взять 103075Па;
— атмосферное давление, взять 103075Па;