Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Спектры излучения и поглощенияСодержание книги
Поиск на нашем сайте
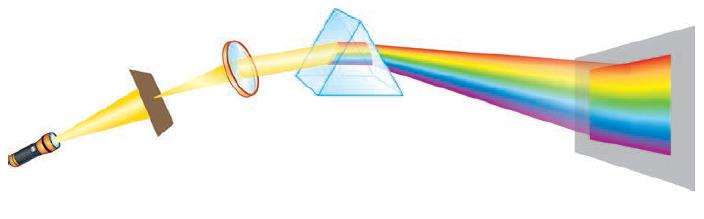
В § 29 мы говорили о том, что электромагнитное излучение представляет собой широкий спектр колебаний, которые различаются частотой и, следовательно, длиной волны. Напомним, что для того, чтобы вычислить частоту, зная длину волны, надо разделить скорость распространения волны на эту длину. Так что чем больше частота излучения, тем короче его длина волны. Теперь мы также знаем, что энергия электромагнитного излучения прямо пропорциональна его частоте, т. е. обратно пропорциональна длине его волны. Излучение, длина волны которого лежит на участке от 380 до 780 нм, воспринимается человеческим глазом и называется видимой частью излучения или просто видимым светом. От длины волны видимого света зависит его цвет. Излучение, в котором все части спектра представлены в равном соотношении, воспринимается как белый свет. Таким, например, является солнечное излучение[10]. Впервые на то, что солнечный свет можно разложить на составляющие его различно окрашенные лучи, обратил внимание Ньютон. Разумеется, и до него люди наблюдали на небе радугу, которая почему– то появлялась обычно после дождя, любовались игрой света в драгоценных камнях и т. д., но причину этого явления никто объяснить не мог. Решающее открытие было сделано Ньютоном следующим образом. Свет от Солнца или от фонаря пропускают через узкую щель, а затем с помощью линзы фокусируют на белом экране, где образуется короткий белый прямоугольник. Если на пути луча света поместить стеклянную призму, то этот прямоугольник сместится и превратится в окрашенную полоску, где постепенные переходы цветов от красного до фиолетового совпадают с теми, которые можно наблюдать в радуге (рис. 109). Ньютон знал, что, проходя через призму, лучи света испытывают преломление, т. е. меняют угол направления своего движения. Теперь оказалось, что лучи разного цвета меняют этот угол по– разному. На основании этого наблюдения Ньютон сделал вывод, что лучи разного цвета преломляются призмой неодинаково.
Рис. 109. Дисперсия света на призме
Обнаруженное им радужное изображение он назвал спектром (от лат. spektrum – видение), а само явление разложения света на различные цветовые составляющие – дисперсией. Таким образом, оказалось, что белый свет представляет собой смесь различных цветов. Эксперименты и выводы Ньютона опровергли распространённое до этого времени мнение о том, что цвет является свойством окрашенных предметов, т. е. цвет приобретает окраску при столкновении с цветными поверхностями. Но если это так, то от чего зависит цвет всех предметов, которые находятся вокруг нас и окраска которых является их естественным свойством? Возьмём какой-нибудь прозрачный окрашенный предмет, например цветное стекло или пластик. Положим его на стол и посмотрим на него в падающем сверху свете. Допустим, что его цвет будет синим. Это значит, что те лучи, которые он от себя отражает и которые после этого попадают в наш глаз, будут синими, т. е. в глаза попадает излучение, имеющее такую длину волны, которая воспринимается человеком как синий цвет. Теперь посмотрим через этот прозрачный предмет на свет. Мы убедимся, что всё, что мы видим, станет тоже синим. А это означает, что наше стекло пропускает через себя только синее излучение. Можно проделать наблюдения с прозрачными предметами любого цвета и убедиться в том, что во всех случаях они будут отражать и пропускать одно и то же излучение. Это значит, что предмет данного цвета выбирает для отражения и пропускания только небольшую часть из всего спектра белого света. Что происходит с остальной частью спектра? Она поглощается окрашенным предметом.
Если мы имеем дело с непрозрачным предметом, то он не пропускает никакого света, а может только отражать и поглощать. Белый предмет отражает весь видимый спектр, потому он и выглядит как белый. Чёрный же не отражает никакого света – все падающие на него лучи он поглощает. Поэтому от него в наш глаз не попадает никакого излучения, что воспринимается как чернота. Именно по этой причине люди в жару стараются носить белую или светлую одежду, в наибольшей степени отражающую солнечные лучи, тогда как одежда чёрного цвета большинство лучей поглощает и от этого нагревается. Всё же цветные предметы поглощают свет избирательно, в определённых областях видимого спектра, а все остальные падающие на них волны, отражают. Этот отражённый свет и попадает нам в глаза, вызывая ощущение определённого цвета. Соответственно, сочетание всех волн, которые поглощаются веществом, образует его спектр поглощения, а тех, которые им отражаются, – спектр отражения. Таким же образом для прозрачных тел можно определить спектр пропускания , который, как мы уже сказали, в основном совпадает со спектром отражения. Но для того чтобы что-то могло поглотить или отразить свет, этот свет должен откуда-то прийти. Другими словами, всякий свет должен иметь источник. Таким источником может быть Солнце, Луна, звёзды, электрическая лампа, свеча и многое другое.
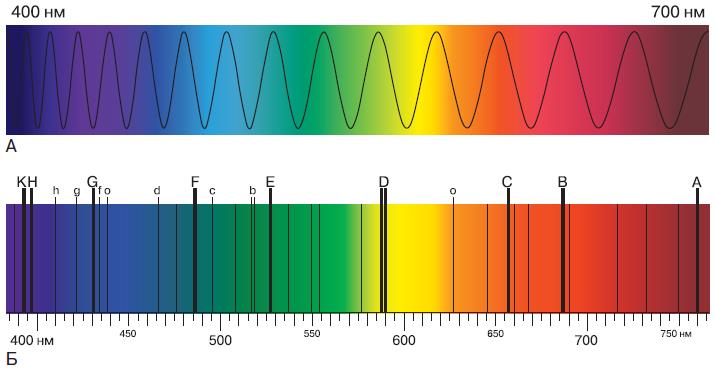
Рис. 110. Непрерывный (А) и линейчатый (Б) спектры
Свет, испускаемый этим источником, иногда может быть белым, как свет Солнца, а иногда в нём будут преобладать волны с какой-то определённой длиной. Так, свет лампочки накаливания является почти белым, но с некоторым преимуществом жёлтой части спектра, а цвет огня в печи или костре имеет хорошо выраженную красную составляющую. В то время, когда не было цветных телевизоров, изображение на экранах называлось чёрно-белым, однако «белый» фон был не совсем таким, в нём явно просматривался голубой оттенок. Отсюда и названия передач старого телевидения, например «Голубой огонёк». Совокупность волн всех частот, испускаемых данным источником света, называют его спектром испускания. Для изучения спектров, испускаемых различными источниками, применяют приборы, называемые спектрометрами. Если направить спектрометр на Солнце или электрическую лампу накаливания, можно увидеть полосу, в которой представлены все цвета спектра, плавно переходящие друг в друга. Такой спектр называют сплошным или непрерывным (рис. 110, А). Другой вид имеют спектры, испускаемые светящимися газами. Они состоят из чётко разграниченных линий. Каждая линия чётко отграничена от соседних линий чёрными полосами и представляет собой узкий интервал, в котором содержится излучение, которое соответствует определённой длине волны. Такой спектр принято называть линейчатым или прерывистым (рис. 110, Б). С помощью спектрометра можно исследовать как спектры испускания, так и спектры поглощения. Первым исследователем, обратившим внимание на спектральные линии, был Йозеф Фраунгофер (1787–1826). В его честь эти линии были названы фраунгоферовыми линиями. В 1850 г. Густав Кирхгоф (1824–1887) и Роберт Бунзен (1811–1899) пришли к выводу, что каждый химический элемент имеет свой уникальный линейчатый спектр и, в частности, по спектру небесных светил можно определить их химический состав. В результате их исследований в науке появился новый метод, называемый спектральным анализом, с помощью которого можно определять состав веществ даже на больших расстояниях. С помощью этого метода инертный газ гелий был открыт на Солнце почти на тридцать лет раньше, чем на Земле, и именно в честь Солнца получил своё название.
Проверьте свои знания
1. Как называется разложение спектра на различные цветовые составляющие? 2. Какие виды спектров могут быть характерными для физического тела? 3. От чего зависит воспринимаемый глазом цвет предмета? 4. Для каких целей используют спектральный анализ?
Задания
1. Подберите эпиграф к данному параграфу. 2. Зажгите газовую горелку и бросьте в её пламя щепотку поваренной соли. Вы увидите, как пламя окрасится в жёлтый цвет. Как вы думаете, почему? В дальнейшем можно поочерёдно бросать в пламя различные порошки или брызгать различными негорючими жидкостями. Пронаблюдайте, как в каждом случае будет изменяться цвет пламени.
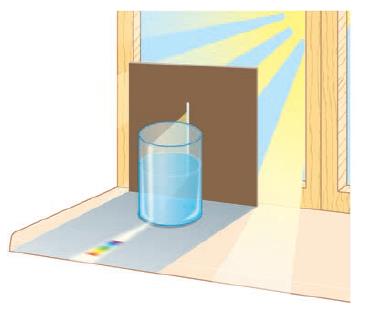
Рис. 111. Иллюстрация к заданию 3
3. Выполните практическую работу «Разложение света». Для этого вам понадобится кусок картона, обычный стакан с водой и белая бумага (рис. 111). Прорежьте в картоне длинную узкую щель. На солнечном месте поставьте на белую бумагу стакан, а между ним и солнцем – картон с щелью. Вы увидите, что солнечные лучи, проходя через щель, а затем через воду в стакане, разлагаются на разные цвета. На бумаге появится последовательность цветных полосок.
Атомная модель Бора
О, Ты, непостижимый Атом, Шедевр творения Творца! Где тот Материи анатом, Который смог бы до конца, Чрез формулу иль созерцаньем, Иль опытом, когда-нибудь Постичь Божественную Суть Тебя – основы Мирозданья?
В каких начертано скрижалях То Слово, что в Тебе звучит? То Слово, что в Тебе искали Первопроходец Демокрит, Отец Системы Менделеев, Твою Модель создавший Бор, И сонмы прочих галилеев Найти мечтали с давних пор?
Джанто
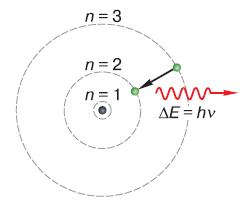
Спектральный анализ в сочетании с квантовой теорией позволили датскому физику Нильсу Бору (1885–1962) предложить в 1913 г. новую модель атома. Мы уже говорили о том, что главный недостаток модели атома, предложенной Резерфордом, заключался в том, что электрон, двигаясь по орбите вокруг атомного ядра, должен постоянно излучать энергию и, потеряв её, через самое непродолжительное время упасть на ядро. Бор предположил, что электроны в атомах могут находиться в некоторых стабильных состояниях, т. е., согласно термину Резерфорда, на определённых орбитах. Эти орбиты не могут находиться на любом расстоянии от ядра, для них существует набор определённых фиксированных положений, которые называют квантовыми уровнями. Энергия электрона зависит от расстояния его орбиты до атомного ядра. Электроны, находящиеся на таких орбитах, не излучают электромагнитных волн, поскольку, теряя энергию, он должен перейти на более низкую орбиту. Однако переход электронов с более высокой орбиты на более низкую возможен. Это явление называется квантовым скачком, который, как и всё в квантовой физике, трудно представить наглядно. Электрон мгновенно исчезает с одной орбиты и возникает на другой. Если эта новая орбита имеет более низкий уровень, то электрон теряет энергию, которая испускается атомом в виде кванта излучения, т. е. фотона (рис. 112). Частота этого излучения равна, как мы знаем, энергии кванта, делённой на постоянную Планка. Если разность энергий между орбитами мала, то происходит излучение в красной области спектра, а если велика, то в синей или даже ультрафиолетовой его области.
Рис. 112. Схема испускания и поглощения фотона при переходе электрона на другую орбиту
Соответственно, для того чтобы совершить квантовый скачок на более высокую орбиту, электрон должен поглотить квант энергии. Величина этой энергии определяет орбиту, на которой этот электрон окажется. Электроны, следовательно, могут двигаться в атоме вверх и вниз скачками с одного квантового уровня на другой, не занимая промежуточных положений. Это подобно тому, как постоялец в гостинице может переехать в другой номер, находящийся на несколько этажей выше или ниже прежнего, но никогда не согласится ночевать на лестнице. Аналогию можно продолжить, если предположить, что в данном отеле комфортность, а следовательно, и цена номеров увеличивается с повышением этажа проживания. Тогда при переезде на более низкий этаж постоялец получит разницу в стоимости, а при переселении наверх должен будет эту разницу доплатить. Такое представление об атоме позволяет понять, почему испускание и поглощение света происходит не непрерывно, а отдельными участками, которые образуют линии спектра. Переходя с орбиты на орбиту, электрон испускает или поглощает не любое количество энергии, а только такое, которое соответствует разности квантовых уровней этих орбит. Допустим, энергия электрона, находящегося на самой высокой либо ~ орбите n, равна E n, на орбите m – E m, а на орбите k – Ek. С орбиты E n электрон может перейти либо на орбиту Em, либо на орбиту E k. При этом он может испустить фотоны с энергией либо (En – Em), либо (En – Ek), либо (E m – E k) без всяких промежуточных значений. Точно так же, поднимаясь с более низкой орбиты на более высокую, он может поглотить только те фотоны, энергия которых равна либо (E n – E m), либо (En – Ek). Фотоны, обладающие другими значениями энергии, он оставит без внимания. Если номер на первом этаже отеля стоит 1000 рублей, на втором – 2000, а на третьем – 5000 рублей, то при переезде постоялец должен будет заплатить (или получить) 1000, 3000 или 4000 рублей. Никакие другие суммы при таком расчёте не могут быть использованы. Всем известно, что многие вещества начинают светиться, т. е. испускать свет, в процессе их нагревания. Это происходит потому, что, приобретая энергию, атомы начинают совершать колебательные движения с большой амплитудой и чаще сталкиваются друг с другом. Потребляя тепловую энергию, их электроны переходят на более высокие орбиты. Долго удержаться на этих орбитах они не могут и возвращаются на освободившиеся низкие орбиты, испуская полученную энергию в виде фотонов света. Чем больше полученная энергия, тем больше будет и энергия испущенного фотона, а следовательно, тем больше будет и частота испускаемого излучения. Эта закономерность закрепилась в народном выражении: «раскалиться не докрасна, а добела». Она объясняется тем, что при небольшой степени нагрева предмет (например, металл) содержит мало энергии и её хватает только на низкочастотное красное излучение. По мере увеличения температуры в испускаемом спектре появляются волны, обладающие всё большей частотой, и в результате в нём начинают присутствовать все области спектра. Поэтому излучение становится белым. При ещё большем нагреве можно сдвинуть спектр в область ещё больших частот и получить голубое излучение. В астрономии известно, что цвет наблюдаемых звёзд зависит от их температуры. Самые холодные представляются нам красными, те, что погорячее, – белыми, а самые раскалённые – голубыми.
Проверьте свои знания
1. От чего зависит энергия электрона в атоме? 2. Что происходит во время квантового скачка? 3. Что требуется для того, чтобы электрон переместился на более высокую орбиту? 4. Как зависит цвет испускаемого нагретым телом излучения от температуры этого тела?
Основные понятия квантовой физики
Я смело могу сказать, что квантовой физики никто не понимает…И если вы просто согласитесь, что, возможно, природа ведёт себя именно таким образом, то вы увидите, что это очаровательная и восхитительная особа. Если сможете, не мучайте себя вопросом «Но как же так может быть?», ибо в противном случае вы зайдёте в тупик, из которого ещё никто не выбирался. Никто не знает, как же так может быть. Р. Фейнман, лауреат Нобелевской премии, один из крупнейших специалистов в области квантовой физики
Противоречивость квантового и волнового поведения света вызывала полное недоумение у физиков в начале XX в. В середине 20-х гг. противоречия удалось разрешить, создав новую науку – квантовую физику (квантовую механику). Новая наука позволила согласовать волновые и корпускулярные представления о природе света, а также объяснить строение атома, свойства элементарных частиц и другие при родные явления. Правда, для этого ей пришлось пожертвовать привычными и кажущимися очевидными представлениями об окружающем нас мире. Положения новой науки оказались настолько непривычными, что не только дилетанты, но и многие серьёзные учёные долгое время отказывались в них верить. При знакомстве с основами квантовой физики лучше всего не задавать вопроса: «А как же это происходит на самом деле?» Ответ на этот вопрос всегда будет один: на самом деле именно так всё и происходит. Причина недоумения заключается в том, что многие явления и законы микромира резко отличаются от тех явлений, которые происходят в обычном для нас макромире.
Рис. 113. Луи де Бройль
Обычно всякое объяснение строится на аналогии: «это похоже на то, как…» или «это явление напоминает нам…». Для описания же того, что происходит в микромире, у нас нет никаких аналогий, потому что в макромире ничего подобного не происходит. Однако приходится поверить в эти законы просто потому, что они доказаны экспериментально и теоретически. В 1924 г. молодой французский физик Луи де Бройль (1892–1987) (рис. 113), занимавшийся исследованием рентгеновского излучения, выдвинул необычайно смелую гипотезу. Он предположил, что если волны света обладают свойствами частиц, то и такие частицы, как атомы, протоны и электроны, должны обладать свойствами волны, т. е. свойство быть одновременно и волной, и частицей, называемое корпускулярно-волновым дуализмом (слово «дуализм» означает двойственность, двойную природу), присуще всем объектам микромира. Не следует думать, что между микро– и макромиром существует резкая граница, где перестают действовать квантовые законы и начинаются привычные для нас законы физики. Как это ни удивительно, любой предмет можно рассматривать как волну. Допустим, что частица массой в 1 г движется со скоростью 1 м/с. Тогда её можно представить как волну, длина которой составляет 10-19 мкм. Эта величина настолько мала, что лежит за пределами любого измерения, поэтому говорить о волновых свойствах таких больших частиц не имеет никакого смысла. Для малых же объектов, таких как атомы и элементарные частицы, волновые свойства имеют очень большое значение. Гипотеза де Бройля впервые была экспериментально подтверждена в 1927 г., когда для электронов было обнаружено явление дифракции, которая, как вы знаете, является непременным свойством волны. В дальнейшем были доказаны волновые свойства протонов и других элементарных частиц, а также атомов и молекул. В настоящее время эти волновые свойства широко используются в технических установках.
Рис. 114. Вернер Гейзенберг
Почти в одно время с де Бройлем молодой немецкий физик Вернер Гейзенберг (1901–1976) (рис. 114) предположил: к квантовым процессам вообще неприменимы многие положения классической механики хотя бы по той причине, что при исследовании микромира невозможно само понятие «измерение» в том смысле, в каком оно понимается в макромире. Одним из основных понятий физики является скорость, т. е. расстояние, на которое тело переместилось за единицу времени. Но как мы можем узнать, что оно переместилось и тем более насколько оно переместилось? Очень просто: мы видим или каким-то образом определяем его месторасположение в один момент времени, а затем – через определённый промежуток времени. Но для того чтобы что-то увидеть, надо, чтобы от этого «чего-то» отразился фотон или электрон, который попадёт в наш глаз или в любой другой регистрирующий прибор. Но если отражение таких частиц практически не повлияет на обычный, пусть и очень маленький предмет, такой как бактерия или даже молекула, то на движении электрона он скажется весьма значительно, и тот изменит свою скорость. Получается, что мы не можем определить местонахождение электрона, не изменив при этом его скорости. В результате Гейзенберг сформулировал принцип неопределённости, согласно которому, невозможно одновременно точно измерить положение частицы и её скорость. Чем точнее мы измеряем координату частицы, тем большую ошибку допускаем в определении её скорости, и наоборот. В отличие от классической физики, где требуется максимально абстрагироваться от самого факта измерения или наблюдения и предполагается, что само проведение эксперимента никак не сказывается на свойствах изучаемого объекта, в квантовой механике дело обстоит совершенно иначе. Сам факт измерения изменяет свойства объекта, и избавиться от этого невозможно. В квантовых исследованиях мы всегда наблюдаем не сам объект, а результат его взаимодействия с измеряющим прибором. Соответственно, разные приборы дают разные результаты. Это происходит не потому, что эти приборы неисправны или недостаточно точны, а потому, что они измеряют различные свойства объекта. Если мы хотим исследовать свойства электрона как частицы, то он ведёт себя как частица. Если же мы хотим изучать его волновые свойства, то он будет вести себя как волна. В этом и заключается предложенный Бором принцип дополнительности:
объекты микромира ведут себя и как волны, и как частицы, причём одно описание не исключает, а дополняет другое.
На самом деле электроны и фотоны не являются ни волнами, ни частицами, а представляют собой нечто иное, не имеющее аналогов в макромире. Это «иное» иногда похоже на знакомые нам морские волны, а иногда – на обычные физические тела. Теперь вы убедились в том, что квантовая физика действительно в какой-то степени странная наука. Многие серьёзные учёные в течение долгого времени отказывались верить в квантово-волновой дуализм. Множество экспериментов, проводимых с целью «установить истинную природу» квантовых частиц и доказать, что они являются «на самом деле» частицами или, наоборот, волной, потерпели полную неудачу. Как ни удивительны законы микромира, они являются объективными законами Природы, и их приходится признавать.
Проверьте свои знания
1. Что такое корпускулярно-волновой дуализм? 2. Почему в макромире не учитывают квантовых законов? 3. В чём заключается принцип неопределённости Гейзенберга?
Задания
Чему равна энергия кванта электромагнитного излучения с длиной волны, составляющей 300 нм, если учесть, что излучение распространяется со скоростью света, а постоянную Планка принять равной 10-34 Дж с?
|
||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 372; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.15 (0.012 с.) |