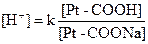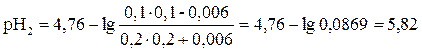Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Буферные системы. Кислотно-основное состояниеСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Буферными называют растворы, способные сохранять значение рН при разбавлении или добавлении небольших количеств кислоты или щелочи.К таким растворам относят: 1) Растворы, содержащие слабую кислоту и соль этой кислоты и сильного основания (СН3СООН + СН3СООNa); 2) Растворы, содержащие слабое основание и соль этого основания и сильной кислоты (NH4OH + NH4Cl); 3) Растворы, содержащие соли многоосновных кислот (Na2HPO4 + NaH2PO4). Расчет рН буферного раствора Расчета рН буферных растворов осуществляется по уравнению Гендерсона – Гассельбаха: – для кислотного буфера уравнение имеет вид
– для основного буфера
Уравнения показывают, что рН буферного раствора данного состава определяется отношением концентраций кислоты и соли или основания и соли, поэтому не зависит от разбавления. При изменении объема раствора концентрация каждого компонента изменяется в одинаковое число раз.
Буферная емкость Способность буферных растворов сохранять постоянство рН ограничена. Т.е. прибавлять кислоту или щелочь, существенно не меняя рН буферного раствора, можно лишь в ограниченных количествах. Величину, характеризующую способность буферного раствора противодействовать смещению реакции среды при добавлении кислот и щелочи, называют буферной ёмкостью раствора (В). Буферная ёмкость измеряется количеством молей эквивалентов сильной кислоты или щелочи, добавление которой к 1 л буферного раствора изменяет рН на единицу. Математически буферная ёмкость определяется следующим образом: В по кислоте (моль/л ил ммоль/л):
где n(1/z HA) – количество моль эквивалентов кислоты, рН0 и рН – рН буферного раствора до и после добавления кислоты, VБ – объем буферного раствора. В по щелочи (моль/л или ммоль/л):
где n (1/z ВОН) – количество моль эквивалентов щелочи, остальные обозначения те же. Буферная ёмкость зависит от ряда факторов: 1. От природы добавляемых веществ и компонентов буферного раствора. Т.к. некоторые вещества могут образовывать нерастворимые соединения или комплексы или давать другие нежелательные реакции с компонентами буферной системы, тогда понятие буферной ёмкости теряет смысл. 2. От исходной концентрации компонентов буферной системы. Чем больше количества компонентов кислотно-основной пары в растворе, тем больше буферная ёмкость этого раствора.
Предел соотношения концентраций компонентов буферного раствора, при котором система все еще сохраняет свои свойства. Интервал рН = рК ± 1, называется зоной буферного действия системы. Это соответствует интервалу соотношения Ссоли/Ск-ты от 1/10 до 10/1. Вк (крови) = 0,05моль/л; Вк (плазмы) = 0,03 моль/л; Вк (сыв.крови) = 0,025 моль/л Буферные системы крови Особенно большое значение буферные системы имеют в поддержании кислотно-основного равновесия организмов. Значение рН большей части внутриклеточных жидкостей находится в интервале от 6,8 до 7,8. Кислотно – основное равновесие в крови человека обеспечивается гидрокарбонатной, фосфатной, белковой и гемоглобиновой буферными системами. Нормальное значение рН плазмы крови 7,40 ± 0,05. Гемоглобиновая буфернаясистемана 35% обеспечивает буферную емкость крови: Карбонатная буферная система: Фосфатная буферная система Белковая буферная системаосуществляет роль нейтрализации кислот и щелочей благодаря амфотерным свойствам: в кислой среде белки плазмы ведут себя как основания, в основной – как кислоты: Буферные системы имеются и в тканях, что способствует поддержанию рН тканей на относительно постоянном уровне. Главными буферами тканей являются белки и фосфаты. Поддержание рН осуществляется также с помощью легких и почек. Через легкие удаляется избыток углекислоты. Почки при ацидозе выделяют больше кислого одноосновного фосфата натрия, а при алкалозе – больше щелочных солей: двухосновного фосфата натрия и бикарбоната натрия.
Примеры решения задач Пример 1. Рассчитать рН буферного раствора, приготовленного смешением 10 мл 0,1М раствора уксусной кислоты и 100 мл 0,1М раствора ацетата натрия (рК(сн3 соон) =4,76). Решение: Рассчитываем рН кислотного буферного раствора по формуле Ответ: 5,76
Пример 2. Рассчитать буферную емкость по кислоте, если на титрование 10 мл сыворотки крови пошло 5 мл 0,1 моль/л соляной кислоты, если при титровании рН изменился от 7,36 до 5,0. Решение: Рассчитываем буферную емкость по формуле:
Ответ: 0,021 моль/л
Пример 3. Буферный раствор состоит из 100 мл 0,1моль/л уксусной кислоты и 200 мл 0,2моль/л ацетата натрия. Как изменится рН этого раствора, если к ней добавить 30 мл 0,2моль/л раствора гидроксида натрия. Решение: Рассчитываем рН буферного раствора по формуле:
При добавлении к буферному раствору NaOH увеличивается количество соли и уменьшается количество кислоты в буферном растворе: 0,006 0,006 0,006 СH3COOH + NaOH = CH3COONa + H2O Рассчитываем n(NaOH) = 0,03 л · 0,2 моль/л = 0,006 моль, следовательно в буферном растворе количество кислоты уменьшается на 0,006 моль, а количество соли увеличится на 0,006 моль. Рассчитываем рН раствора по формуле:
Отсюда: рН2 – рН1 = 5,82 – 5,3 = 0,52 Ответ: изменение рН буферного раствора = 0,52.
Задачи для самостоятельного решения 1. Рассчитать рН буферного раствора, приготовленного смешением 100 мл 0,1М раствора дигидрофосфата натрия и 10 мл 0,1М раствора гидрофосфата натрия (рК(Н2РО4 -) = 7,21). 2. Рассчитать молярную концентрацию уксусной кислоты, если на приготовление ацетатного буфера с рН= 5,76 к 100 мл 0,1М раствора ацетата натрия прилили 10 мл уксусной кислоты (рК(сн3 соон) =4,76). 3. Рассчитать Рн желудочного сока, если концентрация НС1 0,365%, плотность 1г/мл. 4. На титрование 2 мл крови для изменения рН от начального значения (7,36) до конечного значения (7,0) потребовалось добавить 1,6 мл 0,01 М раствора HCl. Рассчитайте буферную емкость по кислоте. 5. Сколько моль ацетата натрия необходимо добавить к 300 мл уксусной кислоты, чтобы понизить концентрацию ионов водорода в 300 раз (Кдис (сн3 соон) = 1,85.10 -5 ). 6. При биохимических исследованиях используют фосфатный буфер с рН= 7,4. В каком соотношении надо смешать растворы гидрофосфата натрия и дигидрофосфата натрия с концентрацией по 0,1 моль/л каждый, чтобы получить такой буферный раствор (рК(Н2РО4 -) = 7,4). 7. Какие нарушения КОС наблюдаются при следующих показателях: рН крови = 7,20, Рсо2 = 38 мм рт. ст., БО = 30 ммоль/л, СБО = -4 ммоль/л. Как устранить данное нарушение КОС? 8. Рассчитать Рн ацетатного буферного раствора, состоящего из 60 мл 0,2М раствора уксусной кислоты и 120 мл 0,01М раствора ацетата натрия при рК(сн3соон) = 4,76. 9. Рассчитать рН 0,01М раствора уксусной кислоты, если степень диссоциации кислоты равна 0,1. 10. Рассчитать объем 5% раствора гидрокарбоната натрия, необходимого для коррекции метаболического ацидоза, если сдвиг буферных оснований (ВЕ) составляет - 10 ммоль/л при массе больного 68 кг. Тестовые задания
|
||||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 969; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.134.83 (0.008 с.) |

 .
.
 ,
, ,
,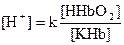 . Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли.
. Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли. по своей мощности занимает первое место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма.
по своей мощности занимает первое место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма. . Дигидрофосфатобладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Гидрофосфат имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.
. Дигидрофосфатобладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Гидрофосфат имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.