
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
II. Кривая титрования слабой кислоты сильным основанием.
При расчете кривой титрования слабой кислоты щелочью следует учитывать тот факт, что до точки эквивалентности в растворе присутствует буферная смесь, состоящая из неоттитрованной слабой кислоты и ее соли, образованной за счет взаимодействия слабой кислоты со щелочью. В точке эквивалентности в растворе присутствует соль, образованная слабой кислотой и сильным основанием, она подвергается гидролизу и среда становится щелочной, в отличие от точки эквивалентности в случае титрования сильной кислоты щелочью. За точкой эквивалентности в растворе, как и в случае титрования сильной кислоты, будет находиться в избытке щелочь, и ее содержание в растворе будет определять рН.
Пример. Построить кривую титрования 10,0 мл 0,1 М CH3COOH раствором 0,1 М NaOH. Расчетные данные приведены в табл.4. Решение:
Во всех последующих точках на кривой титрования до точки эквивалентности (в том числе в начале скачка на кривой титрования) расчет рН ведут для буферной системы (смесь CH3COOH и ее соли CH3COONa) по формуле
Концентрация оставшейся уксусной кислоты в растворе вычисляется по формуле
а концентрация ацетата натрия – по формуле
Например, при добавлении 9,0 мл 0,1 М NaOH
Значение рН в начале скачка на кривой титрования (добавлено 9,99 мл 0,1 М NaOH) рассчитывается по формуле
Таблица 4. Расчет кривой титрования 10,0 мл 0,1 М СH3COOH раствором 0,1 М NaOH
В общем случае рН в начале скачка на кривой титрования слабой одноосновной кислоты можно вычислить по формуле pH = pK + 3 (17) Эта формула получается с учетом того факта, что логарифм отношения количества неоттитрованной кислоты (0,1 %) к количеству полученной соли (99,9 %) в данном случае
В точке эквивалентности (по закону эквивалентов должно быть добавлено 10,0 мл 0,1 М NaOH) рН рассчитывается для гидролизующейся соли CH3COONa по формуле
За точкой эквивалентности расчет рН ведется аналогичным образом, как и в случае титрования сильной кислоты щелочью. Внешний вид кривой титрования приведен на рис.2. Анализ кривой титрования Характерной особенностью кривых титрования слабых одноосновных кислот является несовпадение точки эквивалентности с точкой нейтральности и расположение точки эквивалентности в щелочной области. Величина скачка на кривой титрования значительно меньше, чем в случае титрования сильной кислоты щелочью. Так, в данном случае рН = рН конца скачка - рН начала скачка = 9,7 - 7,76 = 1,94 вместо 5,4 единиц при титровании 0,1 М HCl раствором 0,1 М NaOH. В данном случае в качестве индикатора можно использовать только фенолфталеин, интервал перехода окраски которого лежит в щелочной среде и попадает в область скачка на кривой титрования. Метиловый оранжевый применять нельзя, так как он изменит свою окраску раньше достижения точки эквивалентности. Величина скачка уменьшается с уменьшением концентрации кислоты, с возрастанием температуры, с уменьшением константы диссоциации слабой кислоты. При Kкисл < 10- 6 скачок исчезает вообще.
Рис.2. Кривая титрования 10 мл 0,1 М CH3COOH раствором 0,1 М NaOH
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 254; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.154.41 (0.007 с.) |
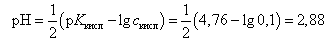 (13)
(13) (14)
(14)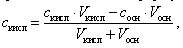 (15)
(15) (16)
(16)




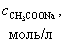


 (18)
(18)



