
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа 8. Влияние разбавления на рН буферного раствораСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Задача работы: выяснить, как зависит рН буферного раствора от разбавления его водой. Оборудование, реактивы: пробирки, 0,1М растворы уксусной кислоты и ацетата натрия, пипетки на 1, 5, 10 мл, универсальный индикатор, цветная шкала рН. Выполнение работы: 1. 2. 3. Сравнить между собой цвета в пробирках №1 и 4; №2 и 5; №3 и 6. Сделать вывод: зависит ли рН буферного раствора от разбавления? 4. Для обоснования полученных результатов, рассчитать рН для шести приготовленных растворов (все расчеты привести). Для расчета используют уравнение Гендерсона- Гассельбаха:
рК(СН3СООН) = 4,76 – табличная величина.
5. Оформляют работу. Формулируют выводы.
Работа 9. Влияние кислоты и щелочи на рН буферного раствора Задача работы: выяснить, как добавление небольшого количества сильной кислоты или основания влияет на рН буферного раствора. Оборудование, реактивы: пробирки, 0,1М растворы уксусной кислоты и ацетата натрия, пипетки, универсальный индикатор, цветная шкала рН. Выполнение работы: В трех пробирках готовят буферный раствор из 5 мл 0,1М раствора уксусной кислоты и 5 мл 0,1М раствора ацетата натрия. 1. Затем прибавляют в одну пробирку 5 капель 0,1М раствора HCl, в другую – 5 капель 0,1М раствора NaOH, в третью – 5 капель дистиллированной воды и в каждую – по 2 капли индикатора метилрота. 2. Сравнить между собой цвета в пробирках. 3. Сделать вывод: зависит ли рН буферного раствора от соотношения компонентов? 4. Оформляют работу.
ТЕМА 5. ЭЛЕКТРОХИМИЯ В этом разделе представлена работа, в которой используется электрохимический метод анализа растворов электролитов – потенциометрия. Одной из ее разновидностей является рН – метрия, в которой определяют рН растворов – одной из самых важных характеристик сред организма и жидких лекарственных средств.
Работа 10. Потенциометрический метод определения рН растворов при помощи стеклянного электрода Задача работы: изучение степени обратимости ионных реакций, определяющих потенциал мембранного стеклянного электрода, нахождение кислотности контрольного раствора. Оборудование, материалы, реактивы: стеклянный электрод с Н+ - функцией, хлорсеребряный электрод сравнения, термометр на 50 ˚С, набор стандартных растворов для рН-метрии (или 0,05 М раствор HCl), раствор Вейбеля (или другой контрольный раствор с рНх), хромовая смесь, мерная посуда. Выполнение работы: 1. 2. Составляют гальваническую цепь для измерения потенциала стеклянного электрода. В стаканчик емкостью 50 – 100 мл вводят стеклянный электрод и внешний хлоридсеребряный электрод сравнения. Выводы от электродов подключают к вольтметру (рН – метру, который работает в режиме измерения напряжения). 3. Таблица 4
При отсутствии стандартных растворов для рН – метрии готовят из 0,05 М (или 0,1М) раствора HCl последовательным разбавлением серию растворов с концентрацией 0,02; 0,01; 0,005; 0,002 и 0,001 М. Растворы готовят в мерных колбах на 100 или 50 мл. Расчет объема исходного раствора Vисх с концентрацией Сисх (0,05М или 0,1 М раствор HCl), который необходим для приготовления растворов с заданной концентрацией Снеоб (необходимой) ведут по формуле: Таблица 5
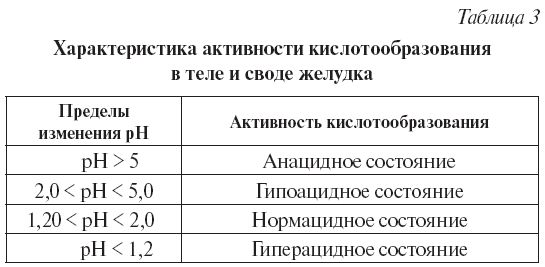
Растворы соляной кислоты обратно в посуду не сливают. 4. Строят зависимость Ест от рНа. Проверяют ее линейность, находят наклон линейного участка dЕст / d(рНа) = ∆Ест / ∆ (рНа). Сопоставляют полученное значение с теоретическим, равным 2,3RT/F или 0,059 В при 298 К. 5. Заливают в стаканчик желудочный сок (или другой раствор с неизвестным рНх). Измеряют потенциал стеклянного электрода, определяют по графику кислотность данного раствора, сравнивают с нормой. 6. Анализируют результаты, формулируют выводы, оформляют работу.
|
|||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 788; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.22.130.228 (0.006 с.) |

 В трех пробирках (№1, 2, 3) готовят буферные растворы с тем же соотношением сопряженных компонентов, как и в работе 5. В другие три пробирки (№4, 5, 6) переносят по 2 мл каждой смеси и разбавляют их 6 мл дистиллированной воды. В шесть полученных пробирок прибавляют по 2 капли индикатора метилрота и перемешивают легким постукиванием.
В трех пробирках (№1, 2, 3) готовят буферные растворы с тем же соотношением сопряженных компонентов, как и в работе 5. В другие три пробирки (№4, 5, 6) переносят по 2 мл каждой смеси и разбавляют их 6 мл дистиллированной воды. В шесть полученных пробирок прибавляют по 2 капли индикатора метилрота и перемешивают легким постукиванием. Сравнить между собой цвета в пробирках №1,2,3 и №4,5,6. Сделать вывод: зависит ли рН буферного раствора от соотношения компонентов?
Сравнить между собой цвета в пробирках №1,2,3 и №4,5,6. Сделать вывод: зависит ли рН буферного раствора от соотношения компонентов?


 Подготавливают к работе стеклянный электрод. Для этого выдерживают его несколько минут в хромовой смеси, промывают дистиллированной водой и высушивают фильтровальной бумагой.
Подготавливают к работе стеклянный электрод. Для этого выдерживают его несколько минут в хромовой смеси, промывают дистиллированной водой и высушивают фильтровальной бумагой. Заполняют стакан раствором (20 – 30 мл) с известным значением рН (обычно это буферный раствор для рН – метрии). Измеряют температуру. Производят измерение потенциала стеклянного электрода (дожидаясь стационарного значения). По окончании измерения, отставляют стаканчик с измеряемым раствором и подставляют стаканчик с дистиллированной водой. Это делается для того, чтобы промыть электрод от предыдущего раствора, а также, чтобы стеклянный электрод не пересыхал. Сливают буферный раствор в ту посуду, где он хранится в лаборатории. Перед тем как подставить стаканчик с новым раствором, электрод высушивают фильтровальной бумагой, чтобы не произошло разбавления, а следовательно изменения концентрации ионов водорода. Проделывают то же самое с серией растворов с известными значениями кислотности. Пока меняют буферный раствор, стеклянный электрод постоянно должен находиться в дистиллированной воде. Результаты измерений заносят в таблицу 4.
Заполняют стакан раствором (20 – 30 мл) с известным значением рН (обычно это буферный раствор для рН – метрии). Измеряют температуру. Производят измерение потенциала стеклянного электрода (дожидаясь стационарного значения). По окончании измерения, отставляют стаканчик с измеряемым раствором и подставляют стаканчик с дистиллированной водой. Это делается для того, чтобы промыть электрод от предыдущего раствора, а также, чтобы стеклянный электрод не пересыхал. Сливают буферный раствор в ту посуду, где он хранится в лаборатории. Перед тем как подставить стаканчик с новым раствором, электрод высушивают фильтровальной бумагой, чтобы не произошло разбавления, а следовательно изменения концентрации ионов водорода. Проделывают то же самое с серией растворов с известными значениями кислотности. Пока меняют буферный раствор, стеклянный электрод постоянно должен находиться в дистиллированной воде. Результаты измерений заносят в таблицу 4. , где Vколбы – объем мерной колбы, в которой готовят раствор. Кислотность этих растворов рассчитывают по формуле: рНа = - lg (g±(HCl) · CHCl), где СHCl – молярная концентрация, а g±(HCl) – молярный средний коэффициент активности соляной кислоты, приведенный в таблице 5.
, где Vколбы – объем мерной колбы, в которой готовят раствор. Кислотность этих растворов рассчитывают по формуле: рНа = - lg (g±(HCl) · CHCl), где СHCl – молярная концентрация, а g±(HCl) – молярный средний коэффициент активности соляной кислоты, приведенный в таблице 5.


