Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Метод спектрометрии ионной подвижностиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Спектрометрия ионной подвижности (СИП, Ion Mobility Spectrometry, IMS), как высокочувствительный метод детектирования химических веществ, возникла в начале 70-х гг. С тех пор она подверглась значительным усовершенствованиям, что сделало ее пригодной для реализации в приборах, предназначенных для решения различных задач. На принципе СИП разработаны компактные, портативные и надежные приборы для детектирования в воздухе паров химических веществ. Газосигнализаторы, основанные на СИП, являются популярными техническими средствами второго поколения, используемыми в различных странах для индикации ТХ и АХОВ. Среди других применений приборов на методе СИП можно назвать обнаружение взрывчатых веществ и наркотиков. Многосторонность применения вместе с низким пределом детектирования являются главными преимуществами СИП. Метод СИП основан на регистрации спектров ионной подвижности анализируемых веществ. Для этого используются приборы, называемые спектрометрами ионной подвижности. Основной частью такого спектрометра является ионно-дрейфовая труба (ИДТ), схема которой представлена на рисунке 1.10.
Рисунок 1.10 – Схема ионно-дрейфовой трубы
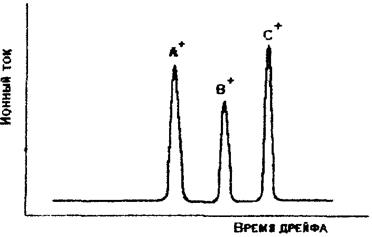
ИДТ включает в себя источник ионизации (обычно радиоактивный) 1, коллекторный электрод 4 и электрические затворы 2 и 3, управляющие движением ионов в приложенном вдоль оси трубы постоянном электрическом поле напряженностью Е. В ИДТ различают две области – область ионизации I и область дрейфа II. Анализируемые вещества вводятся в ИДТ с потоком контролируемого на содержание примесей окружающего воздуха или с потоком газа-носителя, в качестве которого используется очищенный и осушенный воздух или азот. В области I происходит ионизация молекул газа-носителя (воздуха) и анализируемых веществ. Образовавшиеся в области ионизации ионы (на рисунке 1.10 они не показаны) под действием электрического поля движутся к области дрейфа II. В спектрометрах ионной подвижности используется импульсный ввод ионов в область дрейфа. Для этого область дрейфа отделяется от области ионизации инжектирующим электрическим затвором (в виде сет-ки) 2. Когда к затвору приложено запирающее напряжение, прибывающие к нему ионы разряжаются. Периодически на затвор подаются короткие импульсы открывающего напряжения. Во время открытия затвора небольшая часть ионов в виде пространственно ограниченной группы 6, называемой «пакетом» ионов, беспрепятственно проходит сквозь сетку в область дрейфа, где под влиянием приложенного электрического поля движется (дрейфует) по направлению к коллекторному электроду 4. Скорость движения Vi ионов в электрическом поле напряженностью Е равна: Vi = КЕ. Ионы, обладающие разной подвижностью, движутся в области дрейфа ИДТ с различными скоростями, в результате чего происходит разделение общего «пакета» инжектированных ионов 6 на пространственно разделенные «пакеты» разного вида ионов 7. «Пакеты» ионов с большей подвижностью уходят вперед, а «пакеты» ионов с меньшей подвижностью отстают. Эти «пакеты» ионов в разное время достигают коллекторного электрода и последовательно разряжаются на нем. Возникающий при этом ток усиливается усилителем 5 и регистрируется как функция времени, прошедшего с момента поступления ионов в область дрейфа (т.е. с момента открытия инжектирующего затвора). Эта запись представляет собой спектрограмму (спектр) подвижности инжектированных в область дрейфа ионов и состоит из последовательности пиков, каждый из которых соответствует определенному виду ионов. Положение пика в спектре зависит от подвижности данного вида ионов, а площадь (или высота) – от их количества. На рисунке 1.11 в качестве примера представлен спектр подвижности трех видов ионов А +, В + и С +. Время от момента ввода ионов в область дрейфа до момента прихода данного вида ионов к коллекторному электроду называется временем дрейфа τd этих ионов. Оно определяется по положению максимума соответствующего пика в спектре ионной подвижности.
Рисунок 1.11 – Спектр подвижности трех видов ионов
Как можно видеть из вышеизложенного, разделение ионов разной подвижности при их движении в электрическом поле имеет сходство с разделением веществ разной сорбируемости при их движении вдоль слоя сорбента в хроматографической колонке. Одинаков и принцип регистрации сигнала детектора как функции времени с момента ввода ионов в область дрейфа или пробы в хроматографическую колонку. Именно поэтому спектрограмма ионной подвижности очень похожа на хроматограмму. Не удивительно, что спектрометрия ионной подвижности после своего возникновения долгое время называлась плазменной хроматографией (под плазмой в данном случае понимался слабо ионизированный газ. Качественный анализ в спектрометрии ионной подвижности проводится на основе регистрации времени дрейфа – аналога времени удерживания в хроматографии, количественный анализ в обоих методах основан на измерении площади или высоты пиков. Существенной особенностью метода СИП является необходимость удаления из области дрейфа нейтральных молекул анализируемых веществ для предотвращения нежелательных реакций между ними и ионами, приводящих к искажению результатов анализа. Для этого область дрейфа непрерывно продувается дрейф-газом (название газа связано с тем, что именно в среде этого газа происходит дрейф ионов). В качестве дрейф-газа обычно используется очищенный азот или воздух. В последнее время получили распространение спектрометры ионной подвижности, в которых помимо инжектирующего затвора используется второй затвор, называемый сканирующим. Он помещается перед коллекторным электродом 3 (рисунок 1.10). Открывающий импульс подается на сканирующий затвор через некоторое время после открытия инжектирующего затвора. Регистрация спектров ионной подвижности в случае применения двух затворов осуществляется следующим образом. Проводится цикл последовательных инжектирований ионов в область дрейфа (цикл сканирования). При каждом очередном инжектировании время задержки открытия сканирующего затвора изменяется на определенную величину. Обычно интервал изменения времени задержки в одном цикле сканирования составляет от 0 до 20 мс. Если время открытия сканирующего затвора совпадает с моментом прибытия к затвору данного вида ионов, то эти ионы будут пропущены к коллекторному электроду и зарегистрированы. Таким образом, за время одного цикла регистрируется (сканируется) один спектр подвижности инжектируемых ионов. Управление затворами осуществляется электронным блоком синхронизации и сканирования, выполняющим также функцию усреднителя сигналов. В результате регистрируется кривая, представляющая собой усредненный спектр за большое число циклов сканирования. Увеличение длительности инжектирующего импульса приводит к росту амплитуды ионного тока, что увеличивает чувствительность определения, а также одновременно вызывает увеличение ширины пиков, что снижает специфичность. Поэтому в каждом конкретном случае (конструкция спектрометра, напряженность электрического поля, температура, подвижность анализируемых ионов и др.) выбирают разумный компромисс между требованиями по чувствительности и специфичности определения. Длительность сканирующего импульса обычно принимается равной длительности инжектирующего. Варьированием длительностью обоих импульсов в зависимости от времени задержки можно обеспечить хорошее разрешение пиков по всему спектру и повысить чувствительность. Идентификация веществ с помощью приборов, работающих на методе СИП, проводится путем сравнения экспериментально определенной подвижности ионов детектируемого вещества с хранящимися в памяти микропроцессора подвижностями ионов эталонных веществ. При этом необходимо иметь в виду, что в зависимости от влажности и температуры газа в ИДТ детектируемое вещество может давать гидратированные кластерные ионы с разным числом молекул воды, т.е. разной массы, а так как подвижность ионов зависит от их массы, эти кластерные ионы будут иметь различную подвижность, что затруднит идентификацию. Поэтому необходимо контролировать влажность и температуру газа в ИДТ. А поскольку ионная подвижность зависит еще и от давления, оно также подлежит контролю. Ионно-дрейфовая труба спектрометра ионной подвижности изготавливается из непористой металлокерамики, покрытой изнутри резистивным слоем для формирования однородного электрического поля при приложении к торцам слоя разности потенциалов или из металлических (латунных или из нержавеющей стали) колец, разделенных диэлектриком (например, тефло-ном). В последнем случае к каждому кольцу прикладывается электрический потенциал, изменяющийся при помощи делителя напряжения на определенную величину при переходе от одного кольца к следующему. Осевой градиент электрического поля составляет 150 – 200 В см-1 в области ионизации и 250 – 280 В · см-1 в области дрейфа. Система термостабилизации поддерживает температуру ИДТ и пневматической системы в заданном диапазоне. Спектрометры ионной подвижности могут быть с открытым или закрытым контуром циркуляции. В спектрометрах с открытым контуром анализируемый воздух поступает непосредственно в ИДТ. Эти приборы имеют более высокую чувствительность, но их недостатком является влияние на результаты анализа влажности воздуха. Изменение влажности, как отмечалось выше, приводит к образованию кластерных ионов с различными массами, что ухудшает идентификации веществ, в частности мономерных кластеров ТХ. В спектрометрах с закрытым контуром используется мембранный интерфейс, который отделяет наружный воздух от дрейфового газа внутри ИДТ. Мембрана делается из диметилсиликонового полимера толщиной от 5 до 251 мкм. Такие мембраны проницаемы для молекул органических соединений, но задерживают большую часть паров воды. Процент ТХ, проникающих через мембрану, составляет примерно от 10 до 20 %, что обуславливает несколько более высокий предел детектирования по сравнению с приборами открытого типа. Относительная влажность паров воды позади мембраны составляет от 0,5 до 2,5 % при 25 °С, и поддерживается на этом уровне с помощью осушителя во внутреннем потоке газа. Таким образом, относительно паров воды прибор с закрытым контуром циркуляции является герметичной системой. Мембрана обычно помещается в насадку с входным отверстием. Для лучшей проницаемости мембрана может подогреваться микронагревателем до температуры от 75 до 120 °С. На рисунке 1.12 представлена пневматическая схема спектрометра ионной подвижности с закрытым контуром циркуляции.
Рисунок 1.12 – Пневматическая схема спектрометра ионной подвижности с закрытым контуром циркуляции Анализируемый воздух микрокомпрессором 4 просасывается через мембранный интерфейс 2. На входе газа расположены аэрозольный и пылевой фильтры 3. Диффундирующие через мембрану интерфейса 2 молекулы детектируемых веществ потоком газа-носителя переносятся в ионно-дрейфовую трубу 5. Внутренний поток газа обеспечивается микрокомпрессором 7, а его очистка – фильтром 8 на основе активированного угля и молекулярного сита. Скорость потока газа контролируется расходомером 6. После расходомера происходит разделение внутреннего потока – одна его часть выполняет функцию газа-носителя и поступает в мембранный интерфейс 2, а другая служит дрейф-газом и поступает в ионно-дрейфовую трубу 5. Чувствительность и специфичность спектрометра ионной подвижности можно улучшить добавлением к потоку проходящего через ИДТ газа определенных реагентов, например: паров ацетона или аммиака при определении ФТХ; четырёххлористого углерода при определении хлорорганических ТХ. Источником таких реагент-газов служат фторопластовые ампулы или капиллярные течи. В случае использования реагент-газа образующиеся из его молекул ионы выступают в качестве реагент-ионов по отношению к молекулам анализируемых веществ.
Электрохимический метод Среди электрохимических методов следует выделить потенциометрический. Потенциометрический метод анализа основан на измерении потенциала индикаторного электрода, погруженного в исследуемый раствор. В качестве индикаторного электрода выбирается такой, потенциал которого зависит от концентрации определяемого вещества или вещества, добавляемого к определяемому веществу в качестве титрующего реагента. Потенциал индикаторного электрода всегда измеряют относительно какого-либо электрода сравнения, потенциал которого не зависит от концентрации определяемого вещества или реагента. Различают прямой и косвенный потенциометрические методы анализа. В прямом методе, зная зависимость потенциала индикаторного электрода от концентрации анализируемого вещества в растворе, по величине потенциала определяют концентрацию. Этот метод в настоящее время применяется в основном для определения концентрации водородных ионов в растворах, а также при исследовании некоторых комплексных соединений. В последнем случае по величине электродного потенциала определяют концентрацию свободных ионов металла, образующихся при диссоциации комплекса. Косвенный метод называется потенциометрическим титрованием. Потенциометрическое титрование представляет собой вариант объемного метода анализа, в котором точка эквивалентности определяется по изменению потенциала индикаторного электрода в процессе титрования. По сравнению с обычным титрованием, в котором используются цветные индикаторы, потенциометрия обладает рядом преимуществ. Она позволяет титровать окрашенные растворы, смеси нескольких веществ, использовать реакции, не применимые в обычном титровании. При титровании смеси веществ на кривой титрования получается несколько перегибов, по которым можно определить количество реагента, пошедшее на взаимодействие с каждым компонентом смеси. Для успешного применения потенциометрического метода анализа надо правильно выбрать подходящий индикаторный электрод. Индикаторный электрод должен быть обратим по отношению к определяемым ионам (в прямом методе) или по отношению к участвующим в реакции ионам (в потенциометрическом титровании). Кроме этого, индикаторный электрод должен быть химически устойчив в исследуемом растворе, а его равновесный потенциал должен устанавливаться достаточно быстро. Конкретный выбор индикаторного электрода зависит от природы определяемого вещества и характера реакции, используемой для титрования. Так, в случае реакций окисления – восстановления наибольшее применение находит платиновый электрод, а при потенциометрических измерениях, основанных на определении концентрации водородных ионов, – стеклянный электрод. В качестве электродов сравнения применяют электроды второго рода (каломельный, хлорсеребряный и др.). Потенциал индикаторного электрода относительно электрода сравнения, т.е. электродвижущая сила элемента, образованного индикаторным электродом и электродом сравнения, обычно измеряется компенсационным методом. В этом методе измеряемая ЭДС компенсируется противоположно направленной точно известной разностью потенциалов от внешнего источника напряжения. Компенсационный метод измерения ЭДС имеет то преимущество, что в момент достижения компенсации через исследуемый элемент не протекает ток, и, следовательно, электроды не поляризуются. Потенциометрическое титрование находит применение при индикации ФТХ биохимическим методом для определения количества кислоты, выделяющейся в результате ферментативного гидролиза субстрата. Помимо этого, разработаны методики высокочувствительного определения ФТХ потенциометрическим методом по скорости изменения потенциала платинового анода под воздействием тиохолина, образующегося при ферментативном гидролизе тиохолинового эфира. При наличии ФТХ каталитическая активность холинэстеразы уменьшается, в результате чего снижается скорость образования тиохолина и соответствующая ей скорость изменения потенциала анода. Эти методики позволяют применять малые концентрации холинэстеразы, обеспечивают чувствительность определения ФТХ до п · 10-8 мг/ли позволяют автоматизировать проведение анализа. В настоящее время потенциометрический метод реализован в газо-сигнализаторе ГСА-3, находящемся на снабжении ВС РФ.
|
|||||
|
Последнее изменение этой страницы: 2016-12-26; просмотров: 1526; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.123.182 (0.01 с.) |