Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Очистка экстрактов на втором этапе изолированияСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
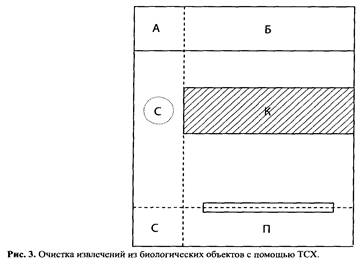
При извлечении токсических веществ из водной фазы в органической фазе вместе с токсическими соединениями будут содержаться так называемые соэкстрактивные вещества, среди которых жиры, белки, продукты их распада, птомаины, красящие, дубильные и другие вещества. Эти примеси мешают анализу, загрязняют колонки хроматографов, могут привести к получению ложноположительных результатов. Для очистки экстрактов используют возгонку, реэкстракцию, электрофорез, хроматографию в тонком слое сорбента и др. Возгонка (сублимация) применима для веществ, способных при нагревании возгоняться без разложения. То барбитураты, салициловая и бензойная кислоты и некоторые алкалоиды. С этой целью после удаления органического растворителя остаток нагревают. Возгон, содержащий исследуемые вещества, осаждается на охлаждаемой с помощью мокрой ваты или марли поверхности (обычно на стекле). При этом соэкстрактивные соединения не возгоняются. Полученный возгон подвергаются анализу. Электрофорез – разделение веществ под действием внешнего электрического поля. Разделению подвергаются вещества, находящиеся в ионизированном состоянии. С этой целью часто используют лист фильтровальной или специальной бумаги для электрофореза, на который наносят 1/25 часть в виде точки и рядом ½ часть в виде полосы полученного из объекта экстракта. Бумагу смачивают буферным раствором с определенным значением рН, помещают в аппарат для горизонтального электрофореза, устанавливают необходимую величину напряжения. Условия подбирают таким образом, чтобы степень миграции (передвижения в электрическом поле) искомых соединений и соэкстрактивных веществ была разной или чтобы разделяемые вещества имели неодинаковый заряд и перемещались к противоположным полюсам. Полученную электрофореграмму высушивают и зону, по которой мигрировали вещества из 1/25 части экстракта, обрабатывают подходящим реагентом-проявителем. Непроявленную часть электрофореграммы, соответствующую обнаруженному с помощью реагента-проявителя пятну, вырезают, измельчают, элюируют исследуемое вещество соответствующим растворителем и анализируют. Реэкстракция основана на переведении веществ из водной фазы в органическую при изменении рН среды. Этот метод применяют для очистки остатков, содержащих барбитураты и некоторые алкалоиды. Используется различная растворимость их молекулярных и ионизированных форм в воде и органических растворителях. При очистке остатков, содержащих барбитураты, используется их способность к лактим-лактамной (имидо-имидольной) таутомерии. Экстракт, полученный из водной вытяжки при рН=2, содержит барбитураты в лактамной (имидной) форме. После испарения органического растворителя к остатку добавляют раствор щелочи до рН=10. Барбитураты переходят в соли монолактимной формы. Их особенностью является растворимость в воде и нерастворимость в органическом растворителе. Примеси из полученного щелочного раствора экстрагируют диэтиловым эфиром. Очищенный щелочной раствор подкисляют до рН=2. При этом барбитураты вновь переходят в лактамную форму, способную экстрагироваться органическим растворителем. Особые трудности представляет анализ гнилостно разложившегося биологического материала, содержащего трупные яды. Очистка экстрактов от птомаинов. При очистке остатков, содержащих алкалоиды и птомаины, использование реэкстракции основано на способности алкалоидов (оснований) образовывать соли в слабокислой среде, а птомаинов (оснований) – в сильнокислой среде. Экстракт, полученный из водной вытяжки при рН=8-10, содержит алкалоиды и птомаины в виде оснований. После испарения органического растворителя такой остаток окрашен в бурый цвет и маслянистый на вид. Остаток после испарения органического растворителя растворяют в воде и добавляют щавелевую кислоту до слабокислой реакции среды, алкалоиды переходят в соли, а птомаины остаются в виде оснований. После экстракции раствора хлороформом в органическую фазу переходят птомаины-основания, а алкалоиды-соли остаются в растворе, который затем подщелачивают раствором аммиака до рН=8-10 и экстрагируют очищенные алкалоиды-основания хлороформом. Методы реэкстракции часто сочетают с хроматографической очисткой. Хроматография в тонком слое сорбента (ТСХ). Очистка извлечений с помощью ТСХ рекомендуется на последнем этапе химико-токсикологического анализа, когда необходимо определить найденное ядовитое вещество количественно или подтвердить его обнаружение с помощью физико-химических методов. С этой целью определенную часть экстракта наносят на пластинку в виде полосы (П) или в виде капель, а рядом наносят «стандарт» - раствор известного вещества – С (около 10-15 мг). (рис.3)
Пластинку помещают в частную систему растворителей, в которой происходит четкое разделение ядовитого вещества, его метаболитов и эндогенных соединений. Когда растворитель поднимается по пластинке на высоту 10 см, ее вынимают и высушивают. С помощью стеклянной пластинки закрывают часть Б и обрабатывают реагентом-проявителем ту часть пластинки (А), по которой двигался «стандарт». При этом фиксируют только «пятно-стандарта» С. Затем стеклянную пластинку снимают и зону сорбента (К), соответствующую «пятну-стандарту», соскабливают и элюируют подходящим растворителем (растворами кислот, щелочей, аммиака, спирта и др.). Полученный элюат используют для обнаружения или количественного определения найденного ядовитого вещества с помощью ГЖХ, ВЭЖХ, УФ-спектрофотометрии, хроматомасс-спектрометрии и др. [1, 3, 4, 9]
|
||||
|
Последнее изменение этой страницы: 2016-12-11; просмотров: 921; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.227.209.89 (0.006 с.) |