Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы обнаружения ядовитых веществ в извлечениях из объектовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Обнаружение ядовитых, сильнодействующих и наркотических веществ после их изолирования из биологических объектов является следующим этапом химико-токсикологического исследования. Химик-токсиколог для обнаружения в объекте какой-либо группы веществ или определенного вещества обязан использовать только те реакции и методы, которые апробированы на биологических объектах, рекомендованы для целей химико-токсикологического анализа с учетом всех факторов, влияющих на получаемые результаты. Только в этом случае полученные данные могут быть объективными и застрахованными от возможных ошибок, среди которых могут быть ошибки, связанные с получением ложноположительных или ложноотрицательных результатов. Ложноположительный результат – это заключение о наличии токсических, экзогенных веществ при анализе по определенной методике при фактическом их отсутствии. Это свидетельствует об использовании высокочувствительной, недостаточно специфичной методики и возможном отсутствии ее апробации на биологических объектах, особенно находящихся на стадии гнилостного разложения. Если какое-либо вещество или его метаболит присутствуют в объекте в концентрации ниже предела их обнаружения, то возможно получение ложноотрицательных результатов. Причиной этого чаще всего выступает фактор времени, т.е. интервал времени между контактом ядовитого вещества с организмом человека или животного и временем взятия и направления объекта на анализ. В этом случае даже правильно выбранная методика с высокой чувствительностью может дать отрицательный результат. Для обнаружения токсических соединений в биологических объектах в настоящее время применяются различные химические реакции, физические, физико-химические, биологические (фармакологические) и другие методы. Среди них выделяют методы и реакции предварительного анализа и методы и реакции подтверждающего исследования. Использование предварительного анализа или предварительных химических реакций преследует цель обнаружить или исключить из анализа группу веществ или какое-либо индивидуальное вещество. Таким реакциям или методам придают «судебно-химическое значение при отрицательном результате». Это означает, что если при использовании данного метода или реакции вещество или группа веществ не обнаружены, дальнейший анализ на эти соединения не проводят и в заключении указывают, что данное вещество или группа веществ в исследуемом объекте не найдены. Предварительные реакции и методы должны быть чувствительными, но не обязательно специфичными. Среди них – скрининговые методы (ТСХ, ГЖХ – скрининг, иммунохимические методы) и реакции, которые оцениваются как имеющие значение при отрицательном результате: групповые реакции осаждения, хромогенные реакции и др. Эти способы и реакции должны быть обязательно подтверждены химическими и физико-химическими методами. Предварительные реакции и методы, как правило, не позволяют определить индивидуальные вещества. Это требует проведения дополнительных исследований. В токсикологической химии такие исследования называют подтверждающим анализом, подтверждающими (частными) реакциями или частным внутригрупповым скринингом. Среди них методы ВЭЖХ, ГЖХ, ТСХ, УФ- и ИК-спектрометрия, спектрофотометрия в УФ области спектра, масс-спектрометрия, хроматомасс-спектрометрия, люминесцентный анализ, аналитические реакции разных типов (кислотно-основные, окислительно-восстановительные, комплексообразования), микрокристаллоскопический метод, фармакогностический анализ, фармакологические пробы, а также процессы осаждения, экстракции и др. Подтверждающие методы по чувствительности обычно выше или равны предварительным методам исследования. Это позволяет снизить возможность получения ложноотрицательных результатов. По специфичности подтверждающие методы обычно превосходят предварительные, что снижает количество ложноположительных результатов. Комплексное использование различных методов предварительного и подтверждающего анализов позволяет надежно диагностировать причину отравления или болезненного состояния организма. Обнаружение ядовитых веществ и их метаболитов в процессе предварительного и подтверждающего химико-токсикологического анализа не дает однозначного ответа о количестве яда, попавшего в организм, времени его приема, фазах распределения. Результаты количественного определения найденного токсического соединения позволяют выбрать способ детоксикации и лечения пострадавшего при остром и хроническом отравлении. Выбор метода количественного определения ядовитого вещества в извлечении из объекта зависит: · от предполагаемой концентрации токсического вещества по результатам предварительного и основного (подтверждающего) исследования; · от степени «свежести» объекта и наличия в извлечении продуктов разложения белковых молекул; · от времени, прошедшего от момента попадания яда в организм и до начала анализа; · от степени «чистоты» извлечения и наличия фона эндогенных соединений; · от способности токсического вещества и его метаболитов накапливаться в определенных органах и тканях; · от последствий отравления. В случае смертельного исхода чувствительность методик должны быть 10-3-10-7 г/мл. При наркотическом опьянении, затяжном отравлении или после проведенных детоксикационных мероприятий – 10-8-10-13 г/мл. [4]
Методы предварительного анализа. Аналитический скрининг Аналитический скрининг – это система методических приемов, позволяющих в ходе исследовательских операций исключить («отсеять») или определить группы веществ (индивидуальные соединения) на этапе предварительного исследования. Это позволяет построить дальнейший анализ в нужном направлении. Аналитический скрининг является эффективным при его соответствии определенным требованиям: · специфичность (чаще групповая); · высокая чувствительность; · экспрессность; · точность и воспроизводимость; · возможность сочетания с другими методами анализа. Скрининг используется при анализе многокомпонентных смесей, а в случае ненаправленного анализа – при исследовании извлечения из биологического объекта на неизвестное токсическое вещество. В настоящее время понятие скрининга в токсикологической химии значительно шире. Скрининг – это поэтапное движение к выявлению индивидуального вещества путем последовательного исключения групп ядовитых веществ, а затем отсеивания веществ в обнаруженной группе до выявления конкретного соединения. Из современных скрининговых методов в практике ХТА нашла широкое применение хроматография в тонких слоях сорбента (ТСХ) в нормально-фазовом и обращено-фазовом вариантах. Этот метод доступен, прост в выполнении, отличается высокой чувствительностью, эффективностью, экспрессностью и достаточной специфичностью (избирательностью). ГЖХ-скрининг используется, в основном, при анализе летучих, лекарственных и наркотических веществ. Не потерял своего значения аналитический скрининг с использованием различных химических реакций. Имеются разработки по использованию в качестве скрининговых методов высокоэффективной жидкостной хроматографии (ВЭЖХ), абсорбционной спектроскопии, иммунохимических методов, спектроскопии ядерного магнитного резонанса.
ТСХ-скрининг в нормально-фазовом варианте Метод используется в химико-токсикологическом анализе при исследовании веществ, изолируемых из объекта экстракцией и сорбцией (лекарственные, наркотические вещества, пестициды). Неподвижной фазой в ТСХ служит тонкий слой сорбента (0,1-0,5 мм), содержащий небольшое количество воды и нанесенный на пластинку (из стекла, фольги или полимера). Сорбентом чаще всего является силикагель или оксид алюминия, которые закрепляются на пластинке добавлением связующего компонента – гипса, крахмала и др.
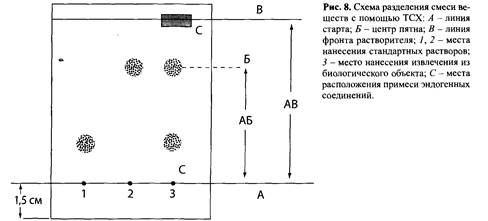
В качестве подвижной фазы (элюента, системы растворителей) предложены индивидуальные растворители или их смеси в определенных соотношениях. Комитет по токсикологическому анализу Международной ассоциации судебных токсикологов рекомендует ряд систем для проведения ТСХ-скрининга в качестве стандартных: · На вещества основного характера: · TA: метанол - 25% аммиак (100:1,5); · TB: циклогексан – толуол – диэтиламин (75:15:10); · TC: хлороформ – метанол (90:10); · TL: ацетон; · TAE: метанол; · TAF: метанол – н-бутанол (40:60). · На вещества кислого и нейтрального характера: · TD: хлороформ – ацетон (80:20); · TE: этилацетат – метанол – 25% аммиак (85:10:5); · TF: этилацетат; · TAD: хлороформ – метанол (90:10). · На вещества кислого, нейтрального и основного характера: · TAJ: хлороформ – этанол (90:10); · TAK: хлороформ – циклогексан – ледяная уксусная кислота (40:40:20); · TAL: хлороформ – метанол – пропионовая кислота (72:18:10). При движении элюента за счет капиллярных сил вверх по пластинке происходит разделение смеси веществ. Эффективность разделения зависит от сродства вещества к сорбенту и определяется коэффициентом распределения его между обеими фазами – подвижной и неподвижной. Чтобы обнаружить вещество на пластинке, используют различные способы детектирования: · визуальный, если само вещество окрашено; · облучение пластинки УФ-лучами, при этом вещество может флуоресцировать или давать темные пятна; · обработка пластинки соответствующими реагентами-проявителями, которые способны образовывать с веществом окрашенные соединения. Для идентификации вещества используют величину Rf – отношение длины пробега анализируемого вещества к длине пробега растворителя (рис.8).
После хроматографирования измеряют расстояние от центра пятна до стартовой линии (отрезок АБ) и от линии фронта жидкости до стартовой точки (отрезок АВ). Отношение отрезков АБ к АВ обозначают величиной Rf:
Величина Rf характерна для данного соединения на данном сорбенте в данной системе растворителей. Она зависит от качества и активности сорбента, толщины слоя, природы растворителей и их соотношения, а поэтому не всегда воспроизводима. Более надежной оценкой хроматографической подвижности вещества является величина Rs. Для ее определения находят величину Rf исследуемого вещества и Rf вещества, принятого за стандарт. Их отношение малочувствительно к влиянию случайных отклонений в условиях эксперимента:
Поэтому Rs – более воспроизводимая и относительно постоянная величина. Общий ТСХ-скрининг в нормально-фазовом варианте был разработан на кафедре токсикологической химии ММА им. И.М. Сеченова для систематического судебно-химического анализа биологических объектов на лекарственные и наркотические вещества, включенные по Приказу МЗ СССР №1021 в обязательный круг исследования эксперимента в случае ненаправленного анализа. Этот метод применим для веществ кислотного, нейтрального, слабоосновного и основного характера. ТСХ-скрининг предполагает разделение веществ в общих системах растворителей на хроматографические зоны с последующим исследованием каждой зоны, в которой были обнаружены те или иные соединения с использованием частных систем растворителей. Лекарственные и наркотические вещества из биологических объектов изолируются путем настаивания с подкисленным спиртом, нейтральным ацетоном, подкисленной водой, подщелоченной водой. Из полученных извлечений (вытяжек) вещества кислотного, нейтрального и слабоосновного характера экстрагируются диэтиловым эфиром или хлороформом при рН=2-2,5, а вещества основного характера – при рН=8-10. Хлороформные (эфирные) экстракты упаривают до небольшого объема и исследуют.
|
||
|
Последнее изменение этой страницы: 2016-12-11; просмотров: 1591; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.199.54 (0.01 с.) |