
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Крохмальним субстратом. Метод КаравеюСодержание книги
Поиск на нашем сайте
Мета: Дослідити активність α-амілази за реакцією розщеплення полісахаридів, за отриманими результатами зробити клініко-діагностичний висновок (стор. 91).
Принцип методу: α-амілаза гідролізує розщеплення крохмалю з утворенням кінцевих продуктів, які не дають кольорової реакції з йодом. Про активність α-амілази судять за вимірюванням зменшення концентрації крохмалю. Прилади та матеріали: колориметр фотоелектричний концентраційний КФК-2, водяний термостат, субстратно-буферний розчин, 0,2 г крохмалю, основний розчин йоду, робочий розчин з молярною концентрацією еквівалентів йоду 0,01 моль/л, досліджувана сироватка крові.
Готування робочих розчинів 1. Субстратно-буферний розчин. 13,3 г безводного натрій гідрогенфосфату і 4,3 г бензойної кислоти кип'ятять у 250 мл дистильованої води. Суспендують 0,2 г розчинного крохмалю в невеличкій кількості холодної води і вводять у киплячу суміш. Кип'ятять 1 хвилину, охолоджують і доводять водою до 500 мл. 2. Основний розчин йоду. 30 г калій йодиду розчинити в 250 мл дистильованої води, внести 12,7 г кристалічного йоду і довести об’єм до 1000 мл (можна використовувати розчин Люголю). 3. Робочий розчин йоду. 25 г калій фториду внести в колбу, додати 350 мл дистильованої води, внести 50 мл основного розчину йоду і довести об’єм до 500 мл. Якщо в робочий розчин не додавати калій фториду, то його необхідно готувати перед кожним дослідом. Хід визначення У дві колби об’ємом 25 мл (досліджувана та контрольна) відмірюють по 2,5 мл крохмального субстрату. Досліджувану пробу прогрівають у термостаті при температурі 37 0С протягом 5 хвилин, після чого до неї додають 0,1 мл сироватки або відфільтрованої сечі. Вміст пробірок перемішують та інкубують протягом 7,5 хвилин при температурі 37 0С. Відразу ж після прогрівання досліджуваної проби в обидві колби додають по 2,5 мл робочого розчину йоду, обсяг реактивів доводять до 25 мл дистильованою водою і негайно заміряють екстинкціюрозчинів за довжини хвилі 630 – 690 нм (червоний світлофільтр) у кюветі з товщиною шару 10 мм проти дистильованої води (розд. 2.1.1). Розрахунок активності α-амілази виконують за формулою:
де Норма активності α–амілази в сироватці крові: 12 – 32 г/(год. · л). Лабораторна робота №11 Визначення активності α–амілази Зі стійким крохмальним субстратом. Метод Каравею (модифікований) Мета: Дослідити активність α-амілази за реакцією розщеплення полісахаридів, за отриманими результатами зробити клініко-діагностичний висновок (стор. 91). Принцип методу: α-амілаза гідролізує розщеплення крохмалю з утворенням кінцевих продуктів, які не дають кольорової реакції з йодом. Про активність α-амілази судять за вимірюванням зменшення концентрації крохмалю. Прилади та матеріали: колориметр фотоелектричний концентраційний КФК-2, водяний термостат, субстратно-буферний розчин, 0,2 г крохмалю, основний розчин йоду, робочий розчин йоду – розчин з молярною концентрацією еквівалентів І2 0,01 моль/л, досліджувана сироватка крові. Хід визначення У звичайну хімічну пробірку вносять 1 мл розчину крохмалю, субстрат прогрівають 5 хвилин у водяному термостаті при температурі 37 0С, після чого до нього додають 0,02 мл сироватки. Пробу знову вміщують рівно на 5 хвилин у термостат. Контрольну пробу проводять так саме, як і досліджувану, але сироватку в неї не вносять. Потім у всі пробірки (досліджувані і контрольні) доливають по 1 мл робочого розчину йоду і по 8 мл дистильованої води, пробірки добре збовтують і розчини негайно фотометрують за допомогою фотоколориметру за довжини хвилі 630 – 690 нм (червоний світлофільтр) у кюветі з товщиною шару 10 мм (розд. 2.1.1). Розчин порівняння – дистильована вода. Розраховують активність ферменту (Аам.) в грамах розщепленого крохмалю на 1 л сироватки за 1 годину інкубації при температурі 37 0С за формулою:
де 240 = 0,4 ∙ 600; 0,4 – кількість крохмалю (мг), внесеного в досліджувану та контрольну проби; 600 = 50 ∙ 12; (50 – коефіцієнт перерахунку на кількість крохмалю в г, яка гідролізована 1 л сироватки; 12 – коефіцієнт перерахункуз 5хвилин на 60хвилин), Еконтр. – екстинкція контрольної проби, Едосл. – екстинкція досліджуваної проби.
Норма активності a–амілази в сироватці крові – 12 – 32 г/(год. · л).
Лабораторна робота № 12 Визначення активності α-амілази в сироватці крові. Метод Кінга
Мета: Дослідити активність α-амілази за реакцією розщеплення полісахаридів, за отриманими результатами зробити клініко-діагностичний висновок (стор. 91). Принцип методу: Активність амілази визначають за часом, що необхідний для розщеплення крохмалю, введеного в реакційну суміш. Метод заснований на здатності крохмалю у присутності йоду забарвлюватися в синьо-фіолетовий колір. Прилади та матеріали: водяний термостат; основний розчин йоду (розчин з молярною концентрацією еквівалентів І2 0,1 моль/л); робочий розчин йоду (готують безпосередньо перед дослідом розведенням основного розчину йоду в 15 – 20 разів дистильованою водою); розчин з масовою часткою крохмалю 0,075 %; досліджувана сироватка крові.
Хід визначення У пробірку вносять 2 мл розчину крохмалю і вміщують у водяний термостат при температурі 37 0С, де вона знаходиться до кінця реакції. Після 2 хвилин прогрівання в пробірку вносять 0,5 мл сироватки крові, перемішують і відзначають час початку реакції. Готують серію пробірок із 5 – 6 шт., що містять по 0,2 мл робочого розчину йоду. Кожні 2 – 5 хвилин у залежності від швидкості реакції беруть невеличкі проби – 0,1 мл (1 – 2 краплі) і вносять їх у пробірки, що містять по 0,2 мл робочого розчину йоду. Кінець реакції визначають за зникненням синьо-фіолетового забарвлення і появі жовтого. У цей момент ферментативний гідроліз крохмалю, узятого для реакції, закінчено. Розрахунок активності α-амілази За одиницю активності приймають кількість ферменту, що розщеплює 1,5 мг крохмалю протягом 8 хвилин. Це довільне число вибрано, щоб наблизити цей метод до інших, у яких враховується утворення сахару за його редукуючою дією. Активність α-амілази розраховується за формулою:
де А ам – активність α-амілази, яка виражена в одиницях на 100 мл сироватки; 8 – час у хвилинах, необхідний для розщеплення 1,5 мг крохмалю у 0,5 мл сироватки, в якій активність амілази дорівнює 1 (одиниці); 0,5 – кількість сироватки, яку взяли для аналізу (мл); Т – час реакції в хвилинах.
Норма. У здорової людини активність α-амілази, яка визначена за даним методом, складає 90 – 163 одиниць на 100 мл сироватки. Лабораторна робота № 13
|
||||
|
Последнее изменение этой страницы: 2016-09-20; просмотров: 235; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.141.12.224 (0.009 с.) |

 ,
, – кількість крохмалю в мг, який гідролізований 1 мл біологічної рідини за 1 годину інкубації при 37 0С, Еконтр. – екстинкція контрольної проби, Едосл. – екстинкція досліджуваної проби, К – коефіцієнт розведення; 2 – кількість крохмалю, введеного в досліджувану і контрольну проби, (мг); 80 – коефіцієнт перерахунку на 1 мл біологічної рідини і 1 годину інкубації.
– кількість крохмалю в мг, який гідролізований 1 мл біологічної рідини за 1 годину інкубації при 37 0С, Еконтр. – екстинкція контрольної проби, Едосл. – екстинкція досліджуваної проби, К – коефіцієнт розведення; 2 – кількість крохмалю, введеного в досліджувану і контрольну проби, (мг); 80 – коефіцієнт перерахунку на 1 мл біологічної рідини і 1 годину інкубації.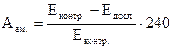 ,
,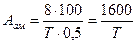 ,
,


