Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Херсонський державний технічний університетСодержание книги
Поиск на нашем сайте
В.М. Безпальченко КЛІНІЧНА БІОХІМІЯ Практикум Навчальний посібник для студентів Вищих навчальних закладів Рекомендовано Міністерством освіти і науки України Херсон – 2003 ББК 53.4 Б-39 УДК 577.1: 616-073.524 В.М. Безпальченко. Б-39 Клінічна біохімія. Практикум. Навчальний посібник для студентів вищих навчальних закладів/ В.М. Безпальченко. – Херсон: ХДТУ, 2003. – 124 с.; іл.11.
ISBN 7763-1140-3
Практикум є складовою частиною навчального комплексу з курсу "Клінічна біохімія". Перші два розділи присвячені теоретичним основам та апаратурному забезпеченню інструментальних методів аналізу в медицині. В наступних розділах з урахуванням досягнень сучасної біохімії викладено лабораторні методи якісного та кількісного дослідження білків, ферментів, нітрогенвмісних речовин, вуглеводів і ліпідів. Більшість методик уніфікована. Дається діагностична оцінка певних біохімічних компонентів у ряді патологічних станах. Рекомендовано для студентів вищих навчальних закладів, які вивчають дисципліну "Клінічна біохімія".
Рецензенти: Новіков О.О. – професор, доктор хімічних наук, проректор Херсонського державного технічного університету, завідувач кафедри біомедичної електроніки. Яковлева С.Д. – кандидат медичних наук, завідувач кафедри дефектології Херсонського державного педагогічного університету. Землянкін О.О. – кандидат медичних наук, завідувач хірургічним відділенням клінічної лікарні Суворовського району м. Херсона. Шепель А.Ю. – кандидат хімічних наук, доцент кафедри хімії Херсонського державного педагогічного університету. Затверджено та рекомендовано до друку на засіданні кафедри фізичної та неорганічної хімії Херсонського державного технічного університету (протокол № 3 від 10 жовтня 2002 р.) Рекомендовано Міністерством освіти і науки України як навчальний посібник для студентів вищих навчальних закладів. Лист № 14/18.2-2348 від 10.12.2002.
ISBN 7763-1140-3 ББК 53.4
Безпальченко В.М., 2003 © ХДТУ, 2003 Передмова
Практикум є складовою частиною навчального комплексу з курсу "Клінічна біохімія". Він містить методичні вказівки до проведення лабораторних занять студентами. Основна мета цього практикуму – закріплення теоретичних знань шляхом формування практичних навичок у галузях динамічної та функціональної біохімії. До практикуму ввійшли типові лабораторні роботи з наступних розділів біохімії: білки, ферменти, вуглеводи, ліпіди. Розкриваються загальні методи дослідження цих класів органічних речовин та їх метаболітів. Приведені якісні реакції та запропоновані методи кількісного інструментального аналізу, в основному уніфіковані. Зазначені правила роботи з апаратурою для фотометричного, поляриметричного, рефрактометричного, потенціометричного аналізу. У лабораторних роботах викладено принципи методу, наведені структурні формули та реакції речовин, які взаємодіють, перелік основних матеріалів, реактивів і обладнання, докладний опис ходу роботи й очікуваних результатів. Така побудова дозволяє проводити визначення без додаткових вказівок, що має важливе значення для підготовки студентів до самостійного виконання наукових робіт. Практикум містить матеріал про клінічну значимість досліджуваних компонентів у біологічних рідинах. Під час виконання запропонованих робіт студенти не тільки опановують сучасні методи експериментальних досліджень, але й набувають уміння аналізувати одержані результати шляхом постановки приблизного діагнозу. Правила роботи в
До роботи в клініко-діагностичній лабораторії (КДЛ) допускаються особи, що володіють спеціальними знаннями та пройшли відповідний інструктаж з техніки безпеки.
Правила роботи В клініко-діагностичній лабораторії
1. Підготувати матеріали (хімічні та біологічні), інструмент, тару, приладита ін. 2. Перед роботою в КДЛ вдягти засоби індивідуального захисту (халати, гумові рукавички, маски). 3. При відбиранні проб біологічних матеріалів обов'язково користуватися гумовою грушею або автоматичними піпетками з одноразовими наконечниками. 4. У випадку забруднення рук біологічними рідинами необхідно негайно промити їх теплою водою та обробити антисептиком (6 % розчином Гідроген пероксиду Н2О2). 5. Роботу з концентрованими кислотами та лугами проводити тільки у витяжній шафі. У випадку потрапляння концентрованих кислот або лугів на поверхню шкіри негайно промити уражене місце проточною водою і провести обробку речовинами, що знаходяться в аптечці (відповідно, слабким розчином соди або оцтової кислоти). 6. У КДЛ суворо забороняється приймати їжу та курити. Розділ 1 В МЕДИЦИНІ Під інструментальними (фізико-хімічними) розуміють такі методи аналізу, що дозволяють вивчати хімічні, фізичні та фізико-хімічні властивості біологічного матеріалу. Під час роботи в КДЛ частіше використовують оптичні методи аналізу і значно рідше – електрохімічні, електрофоретичні, хроматографічні та кінетичні. До оптичних методів аналізу відносять: фотометрію, рефрактометрію та поляриметрію. Фотометрія. До фотометричних відносяться методи аналізу, які засновані на поглинанні або випромінюванні видимого світла розчинами або твердими прозорими тілами (рис. 1).
Рис. 1. Класифікація фотометричних методів аналізу
Абсорбційна фотометрія – метод аналізу, який заснований на вимірі ступеня послаблення монохроматичного світлового потоку внаслідок вибіркового поглинання світла розчиненою речовиною. Теоретичним обґрунтуванням фотометрії є закон Бугера-Ламберта-Бера:
де
Залежність екстинкціївід концентрації відповідно до закону лінійна і проходить через початок координат. Нахил прямої буде залежати від молярного коефіцієнту поглинання, де До методів абсорбційної фотометрії належать: спектрофотометрія та нефелометрія. При спектрофотометрії порівнюють інтенсивність забарвлення еталонного розчину та розчину, що аналізується. Виконують колориметрування за допомогою фотоелектроколориметрів (ФЕК) і спектрофотометрів. Нефелометрія – метод аналізу, який пов'язаний з оцінкою ступеня помутніння досліджуваного розчину. При власне нефелометрії джерело і приймач світла у фотометрі розташовані взаємно перпендикулярно. Таким чином, вимірюється розсіяне світло. При турбідиметрії джерело і приймач світла знаходяться на одній осі, тому вимірюється послаблення світлового потоку, що пройшов крізь мутний (колоїдний) розчин. Емісійна фотометрія базується на вимірі енергії, що випромінюється речовиною внаслідок енергетично збудженого стану. До методів емісійної фотометрії відносять флюориметрію, яка заснована на ефекті енергетичного збудження молекул і атомів досліджуваної речовини, як наслідок впливу жорсткого ультрафіолетового випромінювання, і полум'яну фотометрію, яка заснована на ефекті енергетичного збудження полум'ям структурних складових досліджуваної речовини. Звичайно для флюорометричних вимірів застосовують концентрації речовин 10–4 – 10–6 г/мл (залежність інтенсивності від концентрації прямолінійна). Якщо в якості розчину порівняння застосовується стандартний розчин речовини (спосіб порівняння або калібрувального графіку), то концентрацію досліджуваного розчину (Сх) розраховують за формулою:
де Рефрактометрія – метод визначення концентрації речовини шляхом виміру показника заломлення проміню світла, що проходить крізь розчин (h). Величина показника залежить від природи речовини, її концентрації, довжини хвилі світла, що падає, температури та тиску. Звичайно виміри при визначенні концентрації речовини проводяться при 20 0С і тиску 760 мм рт. ст. за допомогою приладів – рефрактометрів. У клінічних лабораторіях частіше використовують рефрактометри типу УРЛ, РЛ–2, які розраховані на безпосереднє визначення сахарози чи білків у водних розчинах. Поляриметрія – метод аналізу, заснований на вимірі кута обертання площини поляризації оптично-активними прозорими розчинами чи однорідними рідинами, який дозволяє кількісно визначати в біологічних рідинах вуглеводи. Серед електрохімічних методів аналізу в КДЛ застосовують потенціометричний метод, а саме рН-метрію. Потенциометричний метод заснований на залежності потенціалу електрода від концентрації, що визначається. Потенціал визначається за формулою: j = j0+ де j-електродний потенціал в умовах досліду, В; j0-стандартний електродний потенціал, В; R-універсальна газова стала, Дж/(моль∙К); F-стала Фарадея, Кл/моль; Т-абсолютна температура, К; z-число електронів, що беруть участь у елементарному акті електрохімічної реакції; При визначенні аніонів, катионів і активних нейтральних молекул використовують різноманітні типи електродів. Електрод, який чутливий до даного виду іонів, чи речовини називається індикаторним. Він завжди використовується в парі з електродом порівняння (каломельним або хлоридсрібним). Можливо безпосереднє визначення концентрації електрохімічно-активної речовини по електродному потенціалу. Для цього будують калібрувальний графік залежності j від lgс, що частіше усього має лінійний характер. За допомогою графіка по визначеному значенню j знаходять концентрацію невідомого розчину. рН-метрія – метод аналізу, який базується на залежності потенціалу індикаторного (скляного) електроду від концентрації йонів Гідрогену (Н+), що визначають у розчинах. рН – водневий показник, що застосовується для визначення реакції середовища (кислої, лужної або нейтральної). рН розраховується за формулою: рН = –lg С (Н+), де С – концентрація йонів Гідрогену. Визначення рН середовища має важливе практичне значення: 1) як один із показників гомеостазу – сталості внутрішнього середовища організму; 2) при виконанні біохімічного аналізу ряду компонентів живого організму, наприклад, ферментів, біологічна активність яких безпосередньо залежить від величини рН. Як прилади для потенціометричного аналізу застосовують рН-метри та йономіри. Фотоелектроколориметри
Фотоелектроколориметри є найбільш поширеною фотометричною апаратурою в клінічних лабораторіях. 2.1.1. Колориметр фотоелектричний концентраційний КФК-2 призначений для вимірювань в окремих ділянках діапазону довжин хвиль від 315 до 980 нм, які виділяються за допомогою 11 світлофільтрів (рис. 2). Межі вимірювань екстинкції від 0 до 2,0. Джерело випромінювання – галогенова лампа.
Правила роботи з фотоелектроколориметром КФК-2 1. Перед початком роботи прилад вмикають у мережу і прогрівають протягом 15 хвилин. При цьому кюветне відділення повинно бути відкритим. 2. Встановлюють світлофільтр, який зазначений у методиці. 3. У світловий пучок встановлюють кювету з контрольним розчином. 4. Закривають кришку кюветного відділення. 5. Ручками "Чувствительность" і "Установка 100 грубо", а потім "Точно" встановлюють відлік 100 по шкалі колориметра (Т) або "0" по шкалі оптичної густини (D чи Е). Ручка "Чувствительность" може знаходитись в положенні "1", "2" чи "3". 6. Замінюють кювету з контрольним розчином на кювету з досліджуваним розчином. 7. Знімають показання приладу по шкалі оптичної густини. 8. Виміри проводять не менше трьох разів і знаходять середнє арифметичне значення (Есер.). 9. По закінченні роботи вимкнути прилад.
6 5 1 3 4 2 7 8 9
Рис. 2. Колориметр фотоелектричний концентраційний КФК-2 1 – тумблер "Сеть"; 2 – амперметр; 3 – кришка робочої камери; 4 – важіль управління столиком тримача кювет; 5 – світловий індикатор; 6 – ручка перемикача світлофільтрів; 7 – ручка управління чутливістю; 8 – ручка "Установка грубо"; 9 – ручка встановлення "Точно".
Колориметр фотоелектричний Концентраційний КФК-2МП Особливістю конструкції цього приладу є мікропроцесорна система (МПС), яка розширює його експлуатаційні можливості (рис. 3). На передній панелі МПС розташовані клавіатура, цифрове табло та два сигнальні світлодіода. Клавіатура складається з 24 клавіш, які призначені для оперативного управління фотометром.
5 6 а в 3 4 2 б 7 1
Рис. 3. Колориметр фотоелектричний концентраційний КФК-2МП 1 – тумблер "Сеть"; 2 – мікропроцесорна система: а – цифрове табло, б – сигнальні світлодіоди, в – клавіатура управління; 3 – кришка робочої камери; 4 – важіль управління столиком тримача кювет; 5 – світловий індикатор; 6 – ручка перемикача світлофільтрів; 7 – ручка управління чутливістю світлоприймача.
Правила роботи з колориметром КФК-2МП 1. Увімкнути прилад у мережу, тумблер "Сеть", кнопку "Пуск"; на цифровому табло з’являється мерехтлива кома. Прогріти прилад 30 хвилин з відкритою робочою камерою. 2. Встановити необхідну довжину світлової хвилі ручкою "Светофильтры" і відповідне значення чутливості фотоприймача. 3. У світловий потік внести кювету з контрольним розчином. 4. При відчиненій кришці робочої камери натиснути кнопку "ц/р" – режим роботи "р" – ручний, загоряється світлодіод "р". При віджатій кнопці "ц/р" – режим роботи "ц" – циклічний, загоряється світлодіод "ц" (вимірювання через кожні 5 секунд). 5. Натиснути кнопку "Ш(О)" – нульовий відлік. На цифровому табло зліва від коми висвітлюється цифра "0", справа – значення нульового відліку, допустимі межі від 0,001 до 1,0. 6. Закрити кришку робочої камери. Натиснути кнопку "К(1)" – вимірювання контрольного розчину. На цифровому табло зліва від мерехтливої коми загоряється символ "1". 7. Ввести у світловий потік кювету з досліджуваним розчином. Для вимірювання екстинкції треба натиснути кнопку "Д(5)". На цифровому табло зліва від мерехтливої коми з’являється символ "5". Справа від мерехтливої коми – значення виміряної екстинкції. 8. Виміри проводять не менше трьох разів і знаходять середнє арифметичне значення. 9. По закінченні роботи вимкнути прилад.
2.1.3. Колориметр-нефелометр фотоелектричний ФЭК – 56М дозволяє проводити виміри у діапазоні довжин хвиль від 315 до 630 нм (рис. 4). Має 9 світлофільтрів, з яких дев’ятий є орієнтиром, для точних вимірів непридатний. Джерело світла – лампа розжарювання або ртутно-кварцева лампа. Прилад забезпечує вимірювання екстинкції у межах від 0 до 3,0 (оптимум 0,2 – 0,7). Вимірювальні барабани мають дві шкали: чорну – для коефіцієнтів проникнення та червону – для екстинкції.
9 8 7 5 6 2 4 3 6 5 1
Рис. 4. Колориметр-нефелометр фотоелектричний ФЭК – 56М 1 – вимірювальна частина приладу; 2 – важіль "шторка"; 3 – робоча камера; 4 – амперметр; 5 – відліковий барабан; 6 – шкала барабана; 7 – ручка управління чутливістю; 8 – ручка управління темнового електричного нуля; 9 – перемикач світлофільтрів.
Правила роботи з колориметром ФЭК – 56М
1. Увімкнути прилад у мережу, прогріти 30 хвилин. 2. Встановити "Електричний нуль" приладу: при закритій шторці ручкою "Нуль" встановити стрілку мікроамперметра на "0". 3. Ввести у лівий світловий потік на весь час вимірів кювету з контрольним розчином. 4. Встановити відлікові барабани у нульове положення екстинкції по червоній шкалі. 5. У правий світловий потік ввести кювету з досліджуваним розчином. 6. Відкрити шторки і обертанням лівого барабану встановити стрілку мікроамперметра на "0". 7. Замінити у правому світловому потоці кювету з досліджуваним розчином на кювету з контрольним. Стрілка мікроамперметра відхиляється вправо. 8. Встановити правим відліковим барабаном стрілку мікроамперметра в нульове положення. 9. Зняти показання екстинкції по червоній шкалі правого барабану. Виміри повторюють три рази, щоб виключити похибку приладу; знаходять середнє арифметичне значення. 10. По закінченні роботи вимкнути прилад із мережі. 2.1.4. Фотометр аналітичний медичний Прилад призначений для вимірювання коефіцієнту пропущення розчинів на обраній довжині хвилі випромінювання у діапазоні від 340 до 650 нм за кінцевою точкою колориметричної реакції по одно- та двохвильовій методикам, а також проведення обчислень оптичної густини, молярної концентрації за фактором та за стандартом із забезпеченням автоматичної побудови градуювальної характеристики по одному-шести стандартним розчинам. Фотометр застосовують у КДЛ усіх типів в якості базового фотометричного приладу для біохімічних досліджень. Прилад зберігає працездатність впродовж 8 годин при продуктивності 260 проб за годину. Він складається з фотометричного блоку та вакуумного насосу (рис. 5).
4б 4а 5 1 3 6 2
Рис. 5. Фотометр МЕФАН – 8001 1 – фотометричний блок; 2 – вакуумний насос; 3 – кюветне відділення; 4 – панель індикації світлофільтрів (а) і режиму роботи (б); 5 – блок клавіатури; 6 – трубка з’єднання.
Правила роботи з фотометром МЕФАН – 8001 1. Увімкнути прилад у мережу, переключити тумблер на задній панелі у положення “ ВКЛ” (нагору). На світловому табло загоряються послідовно усі індикатори – прилад самотестується. 2. Приготувати стандартний розчин. 3. По закінченні прогрівання на індикаторі “ РЕЖИМ”, замінюючи один одного загоряються символи “ С, Р, Е, F” і мерехтить кома. Прилад очікує вибору режиму. 4. Для визначення концентрації за стандартним розчином – натиснути “ С”. 5. Натиснути цифру, яка відповідає номеру світлофільтра: 1 – 340 нм, 2 – 405 нм і т.ін., напроти нього загориться світлодіод. 6. Натиснути "↑" для закінчення вибору режиму. 7. Фотометр перейде у режим обнуління, на індикаторі “ ПРОБА” – знак “ П0”. Необхідно зняти значення екстинкції контрольного розчину. а) Вийняти кювету з кюветного відділення і заповнити її дистильованою водою за допомогою піпетки або лійки. б) Увімкнути вакуумний насос і натиснути на корок ємності. При цьому вода буде вилучена із кювети. в) Промити 3 рази, а потім, обережно наливаючи по стінкам, залити контрольний розчин. г) Якщо в полі зору є пухирці повітря, видалити розчин і залити ще раз. д) Помістити кювету у прилад і натиснути “ НУЛЬ”. е) При миготінні коми натиснути “ КОНЕЦ” або "↑". 8. Фотометр у режимі завдання калібрувальної проби – прочерки на індикаторі “ ПАРАМЕТРЫ” і знак “ П1” на індикаторі “ ПРОБА”. 9. Цифрами вводять значення концентрації стандартного розчину. Для значень ≤ 1 необхідно ввести коефіцієнт 10, 100, 1000 для отримання 2-3 цифр перед комою. Наприклад, значення 0,015 необхідно помножити на 1000 і записати 15, а отримане значення розділити на 1000. 10. Кювету заповнити стандартним розчином (п.7). Натиснути “ РЕЗ”, при цьому на індикаторі “ РЕЗУЛЬТАТ” з'явиться значення екстинкції калібрувальної проби. Його необхідно записати. Наступного разу це значення можна ввести з паперу, натиснувши кнопку “ Е”. 11. Натиснути клавішу “ КОНЕЦ”, фотометр переходить у робочий режим. На індикаторі “ ПРОБА” горить “ 1”, на індикаторі “ РЕЖИМ” – “С”. Інші індикатори погашені. 12. Заповнити кювету досліджуваним розчином (п.7), натиснути “ РЕЗ”. Висвітлюється значення концентрації досліджуваної проби на індикаторі “ РЕЗУЛЬТАТ”. Для запису результату в пам'ять приладу після отримання значення натискують " ↑ ". На індикаторі “ ПРОБА” засвітиться номер наступної проби, а “ РЕЗУЛЬТАТ” буде погашений. 13. Для аналізу наступної проби виконують дії за п. 12. 14. По закінченні роботи кювету промити дистильованою водою, вимкнути прилад і вакуумний насос тумблером та із мережі, вилити вміст ємності вакуумного насосу.
|
|||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-09-20; просмотров: 259; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.161.178 (0.012 с.) |


 ,
, та
та  – відповідно вхідний та вихідний світлові потоки, e – коефіцієнт поглинання (залежить від природи речовини і температури),
– відповідно вхідний та вихідний світлові потоки, e – коефіцієнт поглинання (залежить від природи речовини і температури),  – товщина шару розчину, C – концентрація речовини.
– товщина шару розчину, C – концентрація речовини.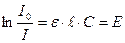 – оптична густинарозчину або
– оптична густинарозчину або  .
. ,
, – показання флуорометру для досліджуваного розчину;
– показання флуорометру для досліджуваного розчину;  – показання флуорометру для стандартного розчину;
– показання флуорометру для стандартного розчину;  – показання флуорометру для контрольного розчину;
– показання флуорометру для контрольного розчину;  – концентрація стандартного розчину.
– концентрація стандартного розчину. ,
, –активність (концентрація) визначаємої речовини чи йона.
–активність (концентрація) визначаємої речовини чи йона.