
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Енергетична структура кристалівСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Ізольований атом є потенціальною ямою, в якій електрон займає один із дискретних енергетичних станів. Енергетичну схему кристала можна подати у вигляді періодично розташованих потенціальних ям, розділених потенціальними бар’єрами. У кристалах відстань між атомами дуже мала (r0 ~0,1 нм), у зв’язку з чим кожний із них виявляється в сильному полі сусідніх атомів. На прикладі кристала Na можна проілюструвати вплив цього поля на енергетичні рівні електронів кожного атома (рис 2.1). Якщо відстань між атомами r>>r0, то електрони розміщені на енергетичних рівнях, ширина яких Коли утворюється кристал (r»r0), то різниця між повною енергією електрона в атомі і висотою потенціального бар’єра меншає, а сам бар’єр звужується настільки, що стає можливим тунельний перехід електронів із одного атома в інший. Імовірність тунельного ефекту значна для валентних
Рис. 2.1 - Схема енергетичних рівнів для атомів натрію: а – вільні атоми; б – зниження висоти потенціального бар’єру, утворення енергетичних зон
електронів і мала для електронів внутрішніх електронних оболонок атомів. Таким чином, валентні електрони в кристалі не локалізовані в конкретному атомі, а переходять від одного атома до іншого, тобто переміщаються від вузла до вузла кристалічної решітки. Швидкість такого руху ~105м/с, і знаходиться електрон в даному вузлі впродовж 10-15с. Але принцип Паулі при цьому не порушується, оскільки відбувається якісна зміна енергетичних рівнів електронів в атомах. Зменшення Наприклад, коли утворюється кристал Na, потенціальний бар’єр знижується нижче положення рівня 3s-електронів, і енергетичні рівні розщеплюються з утворенням енергетичних зон. Таким чином, валентні 3s-електрони стають повністю узагальненими, або вільними. Імовірність розміщення таких електронів у будь-якій точці решітки однакова. На рис. 2.2, показано найбільш простий випадок утворення енергетичних зон із дискретних атомних рівнів. Видно, що вищі рівні розщеплюються сильніше, що відповідає тому порядку, в якому електронні підоболонки атомів взаємодіють між собою при зближенні атомів. Середні енергії смуг спочатку зменшуються, що свідчить про наявність сил притягання. Рівноважна відстань між атомами відповідає умовам мінімальної середньої енергії.
Рис. 2.2 - Утворення енергетичних зон із дискретних атомних рівнів
Електрони у твердому тілі можуть мати тільки ті енергії, значення яких лежать всередині енергетичних смуг. Це так звані зони дозволених енергій. Проміжки між ними являють собою енергії, яких електрони даних речовин набувати не можуть, їх називають забороненими зонами. Із збільшенням енергії електрона в атомі ширина дозволених зон збільшується, а ширина заборонених зон — зменшується. Сформульовані висновки про зонний характер енергії електронів у кристалі безпосередньо випливають із теорії Ф.Блоха, яка є наслідком співвідношення невизначеностей Гейзенберга
де Якщо електрон розміщений на енергетичному рівні вільного атома, то Якщо електрон розміщений на збудженому енергетичному рівні, то Для колективізованих електронів у кристалі Якщо розглянути 1 моль одновалентної кристалічної речовини, то кількість вільних електронів буде дорівнювати числу Авогадро NА=6,02·1023моль-1. Це означає, що зона розщеплюється на число рівнів із дуже малою відстанню між рівнями. Усі зони дозволених енергій відокремлюються зоною заборонених енергій. В одновалентних кристалах існує лише зона дозволених енергій для вільних електронів (у зв’язаних електронів є також зони енергій (рис. 2.3), електрони в цих зонах не впливають на фізико-хімічні властивості кристалів). Оскільки згідно із принципом Паулі на кожному підрівні може розміщуватися не більше двох електронів із протилежно орієнтованими спінами, то у зазначеній зоні одного моля кристала буде лише NА/2 підрівнів зайнято електронами, а решта NА/2 підрівнів будуть вільними. Таким чином, при збільшенні енергії електронів (після нагрівання або під впливом електричного поля) вони можуть переходити на вище розміщені підрівні, беручи участь у кінетичних явищах, у т. ч. і в електропровідності.
а б в Рис. 2.3 - Зони будови металу (а), напівпровідника(б) та діелектрика (в)
У двовалентних кристалах буде 2NА вільних електронів, дві зони дозволених рівнів, у кожній із яких буде NА підрівнів. У результаті перша зона буде повністю заповнена електронами, а друга вільна. Якщо кристал є металом, то ці дві зони дотикаються, і електрони із першої зони (вона називається валентною зоною) будуть вільно переміщуватися по підрівнях другої зони (вона називається зоною провідності). У напівпровідників та діелектриків зона валентності та зона провідності розділяються забороненою зоною. Якщо ширина цієї зони Таким чином, між цими трьома типами кристалів немає якісної відмінності, вона лише кількісна у зв’язку з різним значенням ширини забороненої зони. Зміст самостійної роботи: Розглянути рисунок 2.3. та опрацювати матеріал про зони дозволених енергій та зони заборонених енергій.
|
||||
|
Последнее изменение этой страницы: 2016-08-10; просмотров: 575; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.19.29 (0.007 с.) |

 . Це випливає із співвідношення невизначеностей для енергії
. Це випливає із співвідношення невизначеностей для енергії  , де
, де  - час знаходження електрона в енергетичному стані з енергією від E до
- час знаходження електрона в енергетичному стані з енергією від E до  . Величина
. Величина  визначає ширину енергетичного рівня, якщо відомий час знаходження на ньому електрона. В ізольованому атомі електрон в нормальному (не збудженому) стані може знаходитись як завгодно довго, і ширина енергетичного рівня
визначає ширину енергетичного рівня, якщо відомий час знаходження на ньому електрона. В ізольованому атомі електрон в нормальному (не збудженому) стані може знаходитись як завгодно довго, і ширина енергетичного рівня  буде як завгодно мала.
буде як завгодно мала.
 1еВ. Отже, енергетичний рівень електрона при утворенні кристала із окремих атомів розщеплюється в енергетичну зону. Енергетична зона - це система дискретних енергетичних рівнів.
1еВ. Отже, енергетичний рівень електрона при утворенні кристала із окремих атомів розщеплюється в енергетичну зону. Енергетична зона - це система дискретних енергетичних рівнів.
 ~
~  ,
, – інтервал значень енергії електрона;
– інтервал значень енергії електрона;  – час життя електрона в даному енергетичному стані.
– час життя електрона в даному енергетичному стані. , а
, а  , тобто зона має нульову ширину.
, тобто зона має нульову ширину. ~10-8 с, а
~10-8 с, а 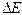 ~10-7 еВ, тобто рівень розмивається в дуже вузьку зону.
~10-7 еВ, тобто рівень розмивається в дуже вузьку зону. ~10-15 с, а
~10-15 с, а 
 еВ, то це буде напівпровідник, а якщо
еВ, то це буде напівпровідник, а якщо  досягає декількох еВ, то це буде діелектрик (рис. 2.3).
досягає декількох еВ, то це буде діелектрик (рис. 2.3).


