Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Мило і синтетичні миючі засоби.Содержание книги
Поиск на нашем сайте
Мила - солі високомолекулярних кислот і лужних металів.
пальмітат натрію стеарат калію C17H35COONa C15H31COOK стеарат натрію пальмітат калію Мило має ряд недоліків. В твердій воді мило має погану миючу здібність. 1) Миюча здібність знижується в солоній воді. 2) Мило не можна використовувати в кислотному середовищі. 3) 4) Мило добре миє лише в гарячій воді особливо при кип'ятінні. Всі ці недоліки синтетичним миючим засобом не характерні. Синтетичні миючі засоби виробляються на основі продуктів переробки нафти, вугілля, природних газів. СМЗ мають добру миючу дію тільки в розбавленому виді, а в концентрованих розчинах вони гублять свою миючу дію. Широке їх застосування згубно діє на навколишнє середовище. Питання та вправи. 1. Отримайте тверде мило із дипальмітину і рідке на основі пальмітоолеїна. 2. Складіть рівняння реакції отримання: диолеїну, пальмітодистеарину, олеолінолеопальмітину і тригліцериду масляної кислоти. 3. Скільки кілограмів 60 % - ного господарського мила одержить фабрика із 1 т. жиру, що містить по 40% тригліцирину і трипальмітину? 4. Напишіть рівняння реакцій гідролізу олеолінолеостеарину. 5. Написати рівняння реакцій утворення пальмітиномернциловогоестеру.
Самостійна робота № 8. Тема: Визначення фізико – хімічних показників жирів. План 1. Йодне число. Кислотне число. 2. Зміна жирів при тепловій обробці. 3. Види псування жирів. Література 1. Черних В.П., Грищенко В. М., Єлисєва Л.І. Органічна хімія: підручник для студентів вищих навчальних закладів I – II рівнів акредитації. К.: Либідь, 2004 – с. 177,178 2. Гурецька В.Л. Органічна хімія. М.: Вища школа, 1999 - с. 171-176.
Питання 1. Йодне число. Кислотне число. Фізико-хімічні константи жирів. Кислотне число, або коефіцієнт кислотності» показує скільки вільних жирних кислот міститься в жирі. Воно виражається числом МГ КОН, яке витрачається на нейтралізацію вільних кислот в 1 г. жиру. Кислотне число служить показником свіжості жиру. Йодне число, показник ненасиченості жиру, визначається кількістю грамів йоду, що приєднується до 100 г. жиру. Чим вище йодне число, тим більш ненасиченим є жир.
Питання 2. Зміна жирів при тепловій обробці. З жирами при нагріванні відбуваються різні перетворення, характер їх залежить від складу жиру, часу нагрівання і температури. В процесі варки і жарки відбувається гідроліз. Крім того при жарінні змінюються і самі продукти гідролізу. Гліцерин дегідрується і перетворюється в ненасичений альдегід - акролеїн, чим і обумовлений неприємний запах і сльозоточивість від кухонного чаду.
акролеїн
Кислоти жирів можуть окислюватись з утворенням оксидних, пероксидних форм і різних низькомолекулярних сполук, придаючи жиру неприємний смак. При тривалому нагріванні жирів з ними відбуваються глибокі хімічні зміни.
Питання 3. Види псування жирів. Розрізняють 3 основні види псування жирів. 1. Прокисання є початковою стадією псування жирів. Воно пов'язане лише з гідролізом жиру, який призводить до накопичення жирних кислот, які придають кислий присмак. 2. Прогіркання пов'язане в першу чергу з окисненням ненасичених жирних кислот, які знаходяться в вільному і зв'язаному стані. Кінцевими продуктами окислення є низькомолекулярні сполуки: кислоти, альдегіди, кетони і інші сполуки, яка придають жирам гіркий смак. При енергійних процесах можуть окислюватись і насичені кислоти. 3. Осалення - найбільш глибокий процес псування жирів. Воно пов'язане з окисленням ненасичених кислот до оксикислот. В процесі осалення змінюється консистенція жиру, підвищується температура плавлення, жир знебарвлюється і набуває салистий присмак. Процесу осалення сприяє прогіркання, Осаленний жир не може бути використаний як харчовий продукт: його використовують лише в технічних цілях. Питання та вправи. 1. Які речовини утворюються при гідролізі жиру в лужному середовищі? Яке практичне використання цього процесу? 2. Кислотне число ялового топленого жиру вищого ґатунку не більше 1.1. Чи можна віднести до вищого ґатунку жир, якщо на нейтралізацію кислот в 12 г. його пішло 0.0038 г. їдкого калію? 3. Йодне число напіввисихаючих олій знаходиться в межах 120-150. Чи можна віднести до напіввисихаючих кукурудзяне масло, яке містить у своєму складі гліцериди типу олеїнолевопальмітинового тригліцириду?
Самостійна робота Тема: Моносахариди План 1. Визначення та класифікація моносахаридів. 2. Фізичні і хімічні властивості, принцип утворення глікозидів 3. Глікозиди харчових продуктів: амігдалін, вакцинін, синігрин, соланін. 4. Використання процесів бродіння в харчовій промисловості. 5. Пентози: арабікоза, ксілоза. Будова поширення в природі. Література 1. Черних В.П., Грищенко В. М., Єлисєва Л.І. Органічна хімія: підручник для студентів вищих навчальних закладів I – II рівнів акредитації. К.: Либідь, 2004 – с. 12,13,18, 207. 2. Гурецька В.Л. Органічна хімія. М.: Вища школа, 1999 – с. 192 - 196
Питання 1. Визначення та класифікація моносахаридів. Вуглеводи являються нарівні із білками, жирами необхідною живильною речовиною для людини і тварин. Вуглеводи відносяться до гетерофункціональних сполук, мають змішані функції, так як містять альдегідну або Катону групу і декілька гідроксильних груп. Вуглеводи представляють собою багатоатомні альдегідо - або кетоноспирити. Вуглеводи часто називають цукристими речовинами або просто ц у к р а ми. Повну класифікацію вуглеводів можна представити слідуючою схемою:
(С6Н12О6)
сахароза, лактоза, крохмаль, гліпоген трегалоза, мальтоза інулін, клітковина
Вуглеводи широко розповсюдженні в природі, вони входять до складу всіх рослинних і тваринних організмів. В рослинних організмах вуглеводи утворюються в результаті фотосинтезу світло
хлорофіл
Моносахариди - вуглеводи загальної формули СnН2nОn з невеликою молекулярною масою. Вони не здатні при гідролізі розщеплюватися на більш прості молекули цукрі.
Питання 2. Фізичні і хімічні властивості, принцип утворення глікозидів Моносахариди тверді безбарвні речовини. Добре розчинні в воді, легко утворюють сиропи, гідроскопічні, в спирті розчиняються погано, в естері не розчиняються. Всі моносахариди мають солодкий смак. Ступінь солодощі окремих представників різна. Моносахариди оптично активні речовини, так як містять асиметричний атом Карбона. Розчини моносахаридів мають нейтральну реакцію на лакмус. моносахаридам властиві реакції на карбонільну і спиртову групи, а також реакції, обумовленні їх взаємним впливом Окислення Моносахаридів При окисленні альдогексоз в ні тральному та кислому середовищі утворюються одноосновні багатоатомні оксикислоти. крейда
О О
Фруктоза, як і всі кетози, в подібних умовах не окислюється. При обережному окисленні в особливих умовах може окислюватися неальдегідна група, а спиртова, розмішена при останньому атома карбона моносахарида О О
галактоза Н галактуронова кислота Н
Галакитуронові кислоти - основна частина пектинових речовин, що знаходяться в плодах, овочах, фруктах. При більш енергійному окисленні в кислому середовищі () окисляються одночасно і альдегідна, і спиртова група, розміщена у останнього атома карбона О
глюкоза Н сахарна кислота Окислення моносахаридів у лужному середовищі так же як і альдегідів, проводять при нагріванні в присутності аміачного розчину оксиду срібла та гідроксиду міді (2). Оксид срібла відновлюється до металевого срібла (реакція срібного дзеркала), а гідроксид міді (2) - до оксиду міді (1). Це якісна реакція на альдози: О
Н Ці дві реакції дають і пентози. При окисленні пентози розщеплюються з утворенням більш простих молекул
O фруктоза триоксімасляна оксіацтова кислота кислота Відновлення моносахаридів. Всі моносахариди (альдози і пентози), подібно альдегідам кетонам, відновлюються з утворенням спиртів (у випадку,гексоз - шестиатомний спирт) О
глюкоза Н сорбіт Відповідно при відновленні галактози утворюється спирт дульцит. Реакція гідроксильних груп. Моносахариди дають всі хімічні реакції характерні для багатьох атомних спиртів. При взаємодії з гідроксидами металів вони утворюють сахарити (цукрати).
глюкоза глюконат міді Моносахариди дають прості і складні естери. Якісної реакції на фруктозу є реакції «Селіванова». Утворення глюкозидів і глюкозиди харчових продуктів. Глікозиди утворюються заміщенням атома гідрогена полуацетального гідроксиду моносахарида на радикал. Загальному вигляді глікозиди можна представити слідуючим видом:
піранозна форма одної із альдогексоз грікозид Полуацетальний гідроксил називається глікозиди, а естери цукрів утворенні за рахунок цього гідроксила - глікозидами, не цукриста частина глікозида називається агліконом, а залишок цукру геліконом.
Питання 3. Глікозиди харчових продуктів: амігдалін, вакцинін, синігрин, соланін. Глікозиди глюкози називаються глюкозидами, глікозиди галактози - галактози дами. Глікозиди на відміну від простих естерів підлягають гідролізи під дією мінеральних кислот. Багато глікозидів гідролізуються під впливом ферментів. Глікозиди представляють собою кристалічні речовини, мають специфічний аромат, гіркий смак, широко розповсюдження в природі. Природні глікозиди утворюються різними агліконами: кислотами, барвниками. В складі харчових продуктів зустрічаються слідуючі глікозиди. Амігдалін — знаходиться в кісточках вишні, слив, персиків, абрикос, в гіркому мигдалі, в лавровому листі. При його гідролізі утворюється бензойний альдегід, глюкоза і вільна синильна кислота, яка є сильнішою отрутою, а тому тривале зберігання вишневих настойок з кісочками не безпечні.
2Н2О
амігдалін глюкоза бензойний синильна альдегід кислота Вакцинін знаходяться в клюкві, брусниці. При гідролізі дає глюкозу і бензойну кислоту. Н2О
вакцинін глюкоза бензойна кислота Синігрін - знаходиться в насінні гірчиці. При гідролізі утворюються глюкоза гірчична олія Н2О
синігрін глюкоза гірчична гідросульфат олія калію Соланін С45Н73NО15 знаходиться в позитивних частинах картоплі. При гідролізі утворює глюкозу і ядовиті речовини.
Питання 4. Використання процесів бродіння в харчовій промисловості. Бродіння називається процес розщеплення моносахаридів під впливом різних мікроорганізмів, краще всього бродінню підлягає глюкоза В якості сировини для отримання моносахаридів використовують крохмаловмісні продукти (картопля, пшениця) або клітковина Найбільш важливими видами бродіння для харчової промисловості є: Спиртове молочно кисле, масляно кисле і лимоннокисле. Спиртове бродіння: дріжджі
глюкоза При бродінні утворюються побічні продукти: гліцерин, янтарна кислота і сивушні масла. Процес бродіння залежить від температури; найбільш енергійно протікає при 30-40 С також він залежить від концентрації цукру 15%. швидкість реакції залежить від кислотності середовища;нормальна реакція перебігає при рН 4-4,5. Спиртове бродіння використовують для отримання спирту пива вина в хлібопекарні. Молочнокисле бродіння відбувається під впливом молочно кислих бактерій з утворенням молочної кислоти. Молочнокисле бродіння дає можливості виробляти різні види молочнокислих продуктів (кефір, просто, кваша, ацидофілін сметани, сирі і т.д.); воно відбувається при засолюванні огірків квашенні капусти, а також при бродінні тіста, надає йому відповідно кислотність. Масляно кисле бродіння відбувається під впливом масляно кислих бактерій з утворенням масляної кислоти. Бродіння відбувається в молоці, сирі, в маслі в результаті його продукти набувають гіркий смак і неприємний запах властивий масляній кислоті. Лимоннокисле бродіння відбувається під впливом деяких видів плісеней,в результаті із глюкози утворюється лимонна кислота. маслянокислі бактерії
глюкоза масляна кислота
Оцтовокисле бродіння відбувається під впливом оцтовокислих бактерій, в результаті із етилового спирту утворюється оцтова кислота. [О]
Питання 5. Пентози: арабікоза, ксілоза. Будова поширення в природі. Пентози - моносахариди складу С5Н10О5. В природі зустрічається в складних вуглеводах - пентозанах (С5Н8О4). Самі пентозами входять до складу деревини, ошурок, сіна, соломи. При їх гідролізі (в присутності кислоти) утворюються пентози. HCl
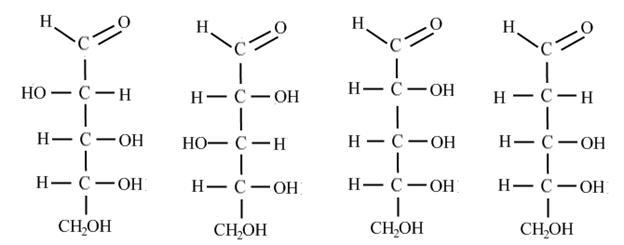
пентозан пентоза Так же, як і гексози, пентози - білі кристалічні речовини, солодкі на смак,розчинні в воді, дають всі основні хімічні реакції гексоз. Найбільш поширеними альдопентозами є:
Д-арабіноза Д-ксилоза Д-рибоза Д-дезоксирибоза Арабіноза - міститься в соці фруктових дерев в буряці. Ксілоза утворюється при гідролізі ксілана (пентозан), ксілоза дає спирт - ксиліт. ксілоза не засвоюється організмом, не зброджується до спирту. Рібоза і дезоксирибоза входять до складу нуклеїнових кислот, ядерних білків - нуклеопротеїдів мають велике біологічне значення. Контрольні питання 1. Які речовини називаються вуглеводами? В результаті якого преса утворюється вуглеводи в природі? В чому його сутність? 2. На які групи і по яким признакам діляться вуглеводи? 3. Як діляться моносахариди по числу карбованих атомів? Які вуглеводи можна віднести до пентоз, гексоз? 4. Які функціональні групи є в молекулі фруктози? Як їх можна виділити? 5. Чому розчини глюкози і фруктози проявляють оптичну активність? 6.-Як утворюється циклічна форма моносахаридів? 7. Чим відрізняється глікозидний гідроксид від других гідроксильних груп в молекул моносахаридів? 8. Які речовини називаються глюкозидами? Наведіть приклади таких речовин. 9. На чому базується процес бродіння моносахаридів? Які види бродіння простого цукру ви знаєте? 10. В яких виробництвах використовується бродіння моносахаридів?
Самостійна робота № 11
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 223; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.216 (0.012 с.) |

 Мило легко гідролізує у воді з утворенням лугу, що шкідливо впливає на шкіру.
Мило легко гідролізує у воді з утворенням лугу, що шкідливо впливає на шкіру.

 СНОН СН2 = СН - С
СНОН СН2 = СН - С СН2ОН Н
СН2ОН Н
 глюкоза, фруктоза
глюкоза, фруктоза nСО2 + nН20 СnН2nОn + nО2
nСО2 + nН20 СnН2nОn + nО2
 Br2 + H2O HBrO + HBr
Br2 + H2O HBrO + HBr
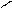

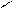
 СН2ОН – (СНОН)4 - С
СН2ОН – (СНОН)4 - С




 СН2ОН – (СНОН)3 - С - СН2ОН + 2O СН2ОН – (СНОН)2 – СООН + СН2ОН – СНОН
СН2ОН – (СНОН)3 - С - СН2ОН + 2O СН2ОН – (СНОН)2 – СООН + СН2ОН – СНОН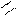
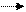
 + Н2 СН2ОН – (СНОН)4 – СН2ОН
+ Н2 СН2ОН – (СНОН)4 – СН2ОН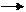 С5Н6(ОН)5СНО + Сu(ОН)2 С5Н6(ОН)3(OС4О) + Сu2О + 2Н2О
С5Н6(ОН)5СНО + Сu(ОН)2 С5Н6(ОН)3(OС4О) + Сu2О + 2Н2О
 С20Н27О11N 2С6Н12О6 + С6Н5CHO + HCN
С20Н27О11N 2С6Н12О6 + С6Н5CHO + HCN С13Н16О7 С6Н12О6 + С6Н5CООH
С13Н16О7 С6Н12О6 + С6Н5CООH С10Н16KNS2О9 С6Н12О6 + С3Н5SCN + KHSO4
С10Н16KNS2О9 С6Н12О6 + С3Н5SCN + KHSO4
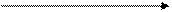 С6Н12О6 С3Н7СООН + 2Н2 + 2СО2
С6Н12О6 С3Н7СООН + 2Н2 + 2СО2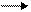 С2Н5ОН СН3СООН + Н2О
С2Н5ОН СН3СООН + Н2О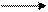 (С5Н8О4)n + nH2O nС5Н10О5
(С5Н8О4)n + nH2O nС5Н10О5