Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теория химического строения органических соединений.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Основные положения Т.Х.С. 1.______________________________________________________________________________________________________________________________________________________________________________________________ ________________________________________________________________________________________________________________________________ _____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ 2. _____________________________________________________________ ________________________________________________________________
3. ____________________________________________________________________________________________________________________________________________________________________________________ 4. ____________________________________________________________________________________________________________________________________________________________________________________ Гомологический ряд и гомологическая разность. Органические соединения можно расположить в ряды сходных по составу, строению и свойствам – гомологические ряды.
Например: ____________________________________________________________________________________________________________________________________ Для гомологических рядов можно вывести общую формулу, для «Алканов» она СnH2n+2 Формулы молекулярные и структурные. В органической химии широко используют различные виды химических формул:
Например: _________________________________________________________
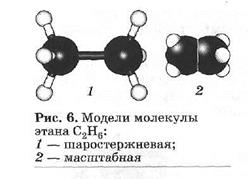
Например ______________________________________________________________________________________________________________________________________________________________________________________________________ Часто нет необходимости детально изображать химические связи между атомами углерода и водорода, поэтому в большинстве случаев используют сокращённые структурные формулы. Например,________________________________________________________ Строение молекул органических веществ наглядно отражают с помощь различных моделей: объёмные (масштабные) и шаростержневые.
Классификация реакций по типу реагирующих частиц и принципу изменения состава молекулы. 1. По направлению (результату) реакции: - реакции присоединения
__________________________________________________________________ 2. реакции замещения
__________________________________________________________________ 3. реакции отщепления
__________________________________________________________________ 4. реакции перегруппировки атомов
__________________________________________________________________ 2. По типу разрыва связи в исходных молекулах: - радикальный (гомолитический) разрыв связи
____________________________________________________________________________________________________________________________________ Свободные радикалы – это __________________________________________ __________________________________________________________________ - гетеролитический (ионный) разрыв связи
____________________________________________________________________________________________________________________________________ Гомолитические реакции - ___________________________________________ __________________________________________________________________ Гетеролитические реакции - __________________________________________ __________________________________________________________________ 3. По типу реагента (атакующих чпстиц) в ионных реакциях: Электрофильные реагенты - __________________________________________ __________________________________________________________________ _________________________________________________________________________________________________________________________________ Например, _________________________________________________________ Электрофильные реакции – это _______________________________________ __________________________________________________________________ Нуклеофильные реагенты - __________________________________________ __________________________________________________________________ __________________________________________________________________________________________________________________________________________________________________________________________________ Например, _________________________________________________________ Нуклеофильные реакции – это _______________________________________ __________________________________________________________________ 4. По числу реакционных частиц, участвующих в самой медленной стадии: 1. ________________________________________________________________ 2._________________________________________________________________ 3._________________________________________________________________
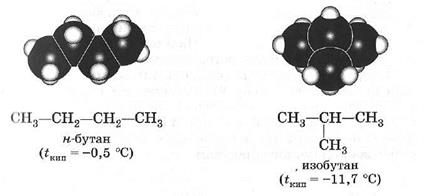
Лекция №2 «ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ В ОРГАНИЧЕСКОЙ ХИМИИ. АЛКАНЫ. ЦИКЛОАЛКАНЫ» 1. Общая характеристика предельных углеводородов. Номенклатура и гомологический ряд алканов. 2. Физические свойства алканов. Основные способы получения. 3. Строение и химические свойства предельных углеводородов. Радикально-цепной механизм реакции в алканах. 4. Циклоалканы. Особые свойства циклопропана и циклобутана. 1.Общая характеристика предельных углеводородов. Номенклатура и гомологический ряд алканов. Углеводороды - ______________________________________________ ____________________________________________________________________________________________. Предельными углеводородами, или алканами (международное название), называются ______________________________ __________________ где n - число атомов углерода. В молекулах предельных углеводородов атомы углерода связаны между собой ___________________ связью, а все остальные валентности насыщены атомами водорода. Алканы называют также насыщенными углеводородами или парафинами. Номенклатура Первым членом гомологического ряда алканов является ____________. Окончание -ан является характерным для названий предельных углеводородов. Далее следует __________, ______________, _____________. Начиная с пятого углеводорода, название образуется из греческого числительного, указывающего число углеродных атомов в молекуле, и окончания -ан. Это _______________________________________ _______________________________________. Алканы, начиная с четвертого члена ряда (бутана), имеют изомеры. Чтобы подчеркнуть, что алкан имеет неразветвленную углеродную цепь, часто к названию добавляют слово нормальный (н-), например: __________________________________________________________________ н-бутан н-гептан (нормальный бутан) (нормальный гептан) При отрыве атома водорода от молекулы алкана образуются одновалетные частицы, называемые__________________________________ (сокращенно обозначаются буквой R). Названия одновалентных радикалов производятся от названий соответствующих углеводородов с заменой окончания –ан на ___. Вот соответствующие примеры:
При отнятии от молекулы углеводорода двух атомов водорода получаются _____________________. Их названия также производятся от названий соответствующих предельных углеводородов с заменой окончания -ан на: –илиден: _________________________________________________________________________________________________________________________________ - илен: ________________________________________________________ ______________________________________________________________ Радикал СН2= имеет название ____________. Для названия изомеров широко применяют три номенклатуры: 1._________________________________________________________________2._____________________________________________________________________________________________________________________________________________________________________________________________________ 3. _________________________________________________________________________________________________________________________________
По рациональной номенклатуре углеводороды рассматриваются как ______________________________________________________________________________________________________________________________________________________________________________________________________Если в формуле одинаковые радикалы повторяются несколько раз, то их указывают греческими числительными: ди - два, три - три, тетра - четыре, пента - пять, гекса - шесть и т. д. Например: _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Рациональная номенклатура удобна для не очень сложных соединений. По заместительной номенклатуре основой для названия служит 1. _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ 2. _____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ 3. _________________________________________________________________________________________________________________________________________________________________________________ 4. _______________________________________________________________________________________________________________________ Если в формуле содержится несколько одинаковых радикалов, то перед их названием указывают число прописью (ди-, три-, тетра- и т. д.), а номера радикалов разделяют запятыми. Вот как по этой номенклатуре следует назвать изомеры гексана:
А вот более сложный пример:
При написании формул изомеров легко заметить, что атомы углерода занимают в них неодинаковое положение. Атом углерода, ________________ ___________________________________, называется первичным, с двумя - вторичным, с тремя - третичным, с четырьмя - четвертичным. Например _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Правило Марковникова №1 _________________________________ ________________________________________________________________________________________________________________________________ 2. Физические свойства алканов. Основные способы получения. В обычных условиях первые четыре члена гомологического ряда алканов (С1 — С4) — __________. Нормальные алканы от пентана до гептадекана (C5 — C17) — __________________, начиная с С18 и выше — т-______________________. По мере увеличения числа атомов углерода в цепи, т.е. с ростом относительной молекулярной массы, возрастают __________ __________________________________________________________________. При одинаковом числе атомов углерода в молекуле алканы с разветвленным строением имеют более низкие температуры кипения, чем нормальные алканы. Алканы практически нерастворимы в ___________, так как их молекулы малополярны и не взаимодействуют с ____________________, они хорошо растворяются в___________________________________________, таких как бензол. СПОСОБЫ ПОЛУЧЕНИЯ АЛКАНОВ Основные природные источники алканов — _____________________ ___________. Различные фракции нефти содержат алканы от C5H12 до С30Н62. Природный газ состоит_____________________________________ __________________.
Из синтетических методов получения алканов можно выделить следующие: 1. Получение из ненасыщенных углеводородов. ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________2. Получение из галогенпроизводных (реакция Вюрца): ____________________________________________________________________________________________________________________________________ 3. Получение из солей карбоновых кислот. ______________________________________________________________________________________________________________________________________________________________________________________________________4. Получение метана. В электрической дуге, горящей в атмосфере водорода, образуется значительное количество метана: __________________________________________________________________Такая же реакция идет при нагревании углерода в атмосфере водорода до 400-500 °С при повышенном давлении в присутствии катализатора. 5. В лабораторных условиях метан часто получают из карбида алюминия: __________________________________________________________________ 3. Строение и химические свойства предельных углеводородов. Радикально-цепной механизм реакции в алканах. В предельных углеводородах ______________________________________
Все алканы насыщены водородом до предела (максимально). Их атомы углерода находятся в состоянии ___________________, а значит, имеют ______________________ связи. В обычных условиях алканы химически _____________. Они устойчивы к действию многих реагентов: не взаимодействуют с концентрированными серной и азотной кислотами, с концентрированными и расплавленными щелочами, не окисляются сильными окислителями - перманганатом калия KMnО4 и т.п. Химическая устойчивость алканов объясняется высокой прочностью ________________ __________________________. Неполярные связи С-С и С-Н в алканах не склонны к ионному разрыву, но способны расщепляться гомолитически под действием активных свободных радикалов. Поэтому для алканов характерны ____________________________, в результате которых получаются соединения, где атомы водорода замещены на другие атомы или группы атомов. Следовательно, алканы______________________________________ _________________________________________________________________. По этому механизму легче всего замещаются атомы водорода ____________ ____________________________________________________________________________________________________________________________________ 1. Галогенирование. При взаимодействии алканов с галогенами (хлором и бромом) под действием УФ-излучения или высокой температуры. Общая схема этой реакции показана на примере метана: Сl2 Сl2 Сl2 Сl2 СН4 → СН3Сl → СН2Сl2 → СНСl3 → ССl4 -HCl -HCl -НСl -HCl Реакция образования хлорметана протекает по цепному механизму, который характеризуется следующими стадиями: а) инициирование цепи: hv __________________________________________________________________ б) рост цепи. __________________________________________________________________ __________________________________________________________________Эти реакции повторяются до тех пор, пока не произойдет обрыв цепи по одной из реакций: в) обрыв цепи: ___________________________________________________________________________________________________________________________________ Суммарное уравнение реакции: ____________________________________________________________________________________________________________________________________ Развитие теории цепных свободнорадикальных реакций тесно связано с именем выдающегося русского ученого ___________________(1896-1986). 2. Нитрование (реакция Коновалова). При действии разбавленной азотной кислоты на алканы при 140°С и небольшом давлении протекает радикальная реакция: ____________________________________________________________________________________________________________________________________ 3. Изомеризация. Нормальные алканы при определенных условиях могут превращаться в алканы с разветвленной цепью: ______________________________________________________________________________________________________________________________________________________________________________________________________ 4. Крекинг —_________________________________________________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________Эти реакции имеют большое промышленное значение. Таким путем высококипящие фракции нефти (мазут) превращают в бензин, керосин и другие ценные продукты. 5. Окисление. При мягком окислении метана кислородом воздуха в присутствии различных катализаторов могут быть получены метиловый спирт, формальдегид, муравьиная кислота: ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Мягкое каталитическое окисление бутана кислородом воздуха - один из промышленных способов получения уксусной кислоты: ____________________________________________________________________________________________________________________________________ 6. На воздухе алканы сгорают до СО2 и Н2О: СН4 + 2О2→СО2 +2Н2О
4. Циклоалканы. Особые свойства циклопропана и циклобутана.
Циклоалканы-_______________________________________________. Простейшие представители этого ряда:
__________________________________________________________________ Общая формула гомологического ряда циклоалканов _________. Точно такой же формулой описывается гомологический ряд _________. Из чего следует, что каждому циклоалкану изомерен соответствующий алкен. Это пример так называемой ____________________________________ изомерии. Строение циклоалканов. Каждый атом углерода в циклоалканах находится в состоянии __________________ и образует__________________________________. Углы между связями зависят от размера цикла. В простейших циклах С3 и С4 углы между связями С-С сильно отличаются от тетраэдрического угла 109,5°, что создает в молекулах напряжение и обеспечивает их высокую реакционную способность. Свободное вращение вокруг связей С-С, образующих цикл, _____________________. Изомерия и номенклатура. 1) Для циклоалканов как и для всех классов органических соединений, характерна ________________________________________________________. 2) Отсутствие свободного вращения вокруг связей С-С в цикле создает предпосылки для существования ______________________________________ __________________________________________________________________. Например, в молекуле 1,2-диметилциклопропана две группы СН3 могут находиться по одну сторону от плоскости цикла (цис-изомер) или по разные стороны (транс-изомер): ______________________________________________________________________________________________________________________________________________________________________________________________________ цис-изомер транс-изомер По размеру цикла циклоалканы делятся на ряд групп - __________ (С3, С4) и ___________________ (С5-С7) циклы. Названия циклоалканов строятся путем добавления приставки цикло- к названию алкана с соответствующим числом атомов углерода. Структурные формулы циклоалканов обычно записывают в сокращенном виде, используя геометрическую форму цикла и опуская символы атомов углерода и водорода. ______________________________________________________________________________________________________________________________________________________________________________________________________ Физические свойства. При обычных условиях первые два члена ряда (С3 - С4) — _______, (С5 - С16) — ________________, начиная с C17 — _____________________. Температуры кипения и плавления циклоалканов выше, чем у соответствующих алканов. Получение. 1. Основной способ получения циклоалканов - отщепление двух атомов галогена от дигалогеналканов: ______________________________________________________________________________________________________________________________________________________________________________________________________ 2. Каталитическое гидрирование ароматических углеводородов: ______________________________________________________________________________________________________________________________________________________________________________________________________ Химические свойства. По химическим свойствам малые и обычные циклы существенно различаются между собою. Циклопропан и циклобутан склонны к реакциям ________________________, т.е. сходны в этом отношении с алкенами. Циклопентан и циклогексан по своему химическому поведению близки к алканам, так как вступают в реакции _____________________. 1. Так, например, циклопропан и циклобутан способны присоединять бром: ______________________________________________________________________________________________________________________________________________________________________________________________________ 2. Циклопропан, циклобутан и даже циклопентан могут присоединять водород: ______________________________________________________________________________________________________________________________________________________________________________________________________ 3. В реакцию присоединения с галогеноводородами опять же вступают только малые циклы. Присоединение к гомологам циклопропана происходит по правилу Марковникова: ______________________________________________________________________________________________________________________________________________________________________________________________________ 4. Реакции замещения: ____________________________________________________________________________________________________________________________________5. Дегидрирование циклоалканов: ____________________________________________________________________________________________________________________________________ ЛЕКЦИЯ №3 «Алкены, алкадиены. Алкины» 1. Общая характеристика алкенов. Номенклатура и изомерия. Строение. Получение и свойства. 2. Общая характеристика диеновых угдеводородов. Номенклатура и изомерия. Строение. Получение и свойства. 3. Общая характеристика алкинов. Номенклатура и изомерия. Строение. Получение и свойства. 1. Общая характеристика алкенов. Номенклатура и изомерия. Строение. Получение и свойства. Простейшими непредельными (ненасыщенными) соединениями являются углеводороды, содержащие _________________________________. Алкены, содержащие две двойные связи, называются ___________, содержащие три двойные связи — ______________ и т.д. Соединения с несколькими двойными связями имеют общее название ________________. Алкенами называются___________________________________________ ______________________________________________________________. Первый представитель этого класса — _______________________________ Ближайшие гомологи этилена: ____________________________________________________________________________________________________________________________________Простейший алкен с разветвленным углеродным скелетом: ____________________________________________________________________________________________________________________________________ Общая формула гомологического ряда алкенов __________.
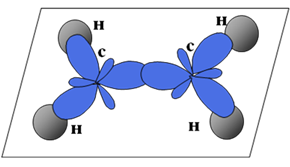
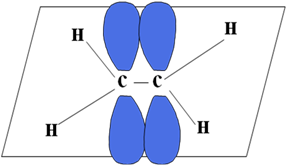
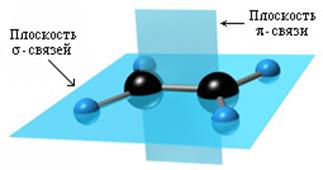
СТРОЕНИЕ Атомы углерода при двойной связи находятся в состоянии __________________. Три s-связи, образованные гибридными орбиталями, располагаются в одной плоскости ____________________________________; p-связь образована _________________________________________________
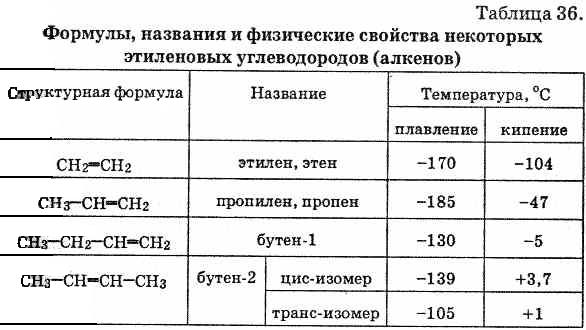
Структурная изомерия алкенов обусловлена ________ ______________________________________________________________. Если каждый из атомов углерода при связи С=С связан с двумя разными заместителями, то эти заместители могут располагаться __________________ Эти два изомера нельзя перевести друг в друга без вращения вокруг двойной связи С=С, а это вращение требует разрыва p-связи и затраты большого количества энергии. Поэтому цис- и транс-изомеры представляют собой _____________________________________________________________________________________________________________________________________________. Алкены, у которых хотя бы один из атомов углерода при связи С=С имеет два одинаковых заместителя, _______________________________. В алкенах с неразветвленной углеродной цепью нумерацию начинают __________________________________________________________________. В названии соответствующего алкана окончание _______________________. В разветвленных алкенах выбирают ________________________________ __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Физические свойства алкенов ________ на свойства алканов, хотя все они имеют несколько __________________ температуры плавления и кипения, чем соответствующие ___________. Например, пентан имеет температуру кипения 36 °С, а пентен-1 — 30 °С. При обычных условиях алкены С2 - С4 — ___________. С5 – С15 — ____________, начиная с C16 — _____________________. Алкены _________________в воде, хорошо растворимы в органических растворителях.
|
|||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-06-29; просмотров: 500; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.01 с.) |