
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Что происходит при длительном пропускании углекислого газа через из-Содержание книги
Поиск на нашем сайте вестковую воду: а) выпадает осадок карбоната кальция; б) некоторое время раствор остается прозрачным, так как вначале образуется растворимый в воде гидрокарбонат кальция, затем начинает выпадать оса- док карбоната кальция; в) сначала выпадает осадок карбоната кальция, затем осадок растворяется, так как образуется растворимый в воде гидрокарбонат кальция; г) никаких видимых изменений не происходит
При обжиге 1кг известняка было получено 179,2л углекислого газа (н.у.) Найдите массовую долю карбоната кальция в известняке. а) 0,8кг; б) 80%; в) 0,2кг; г) 20%
Металлы Вариант 1 1.В ряду Be – Mg – Ca – Sr – Ba металлические свойства: а) не изменяются; б) усиливаются; в) ослабевают; г) нет верного ответа 2.Какой из металлов легче всего вступает в реакции: а) Al; б) Mg; в) Na; г) Be 3.В какой паре оба гидроксида амфотерны: а) AL(OH)3 и Ba(OH)2; б) Zn(OH)2 и NaOH; в) Ca(OH)2 и Mg(OH)2; г) Zn(OH)2 и Al(OH)3 4.Гидроксид натрия не образуется в реакции: а) Na + H2O = б) Na2О +H2O = в) Na2CO3 + HCl = г) нет верного ответа 5.С каким из веществ реагирует гидроксид кальция: а) NaOH; б) K2O; в) HCl; г) NaNO3 6.Какие вещества образуются при взаимодействии Al(OH)3 и раствора NaOH: а) Na2O; б) Na[Al(OH)4]; в) Al2O3; г) H2O 7.Формула мрамора: а) K2CO3; б) MgCO3; в) CaCO3; г) CaSO4 8.Что общего в строении атомов Mg и Ca: а) одинаковый заряд ядра; б) одинаковый радиус атома; в) 2 электрона на последнем энергетическом уровне; г) 1 электрон на последнем энергетическом уровне 9.Какая реакция лежит в основе алюминотермии: а) 2Al +3S = Al2S3; б) 3TiO2 + 4Al = 3Ti + 2Al2O3; в) Al + FeCl3 = Fe + AlCl3; г) Al + P = AlP 10. 800г руды, содержащей 80% оксида свинца (IV), нагрели с 400г кокса. Найти массу полученного свинца. Вариант 2 1.Как изменяются металлические свойства в ряду Li – Na – K – Rb: а) не изменяются; б) ослабевают; в) усиливаются; г) нет верного ответа 2.Какой металл легче окисляется кислородом: а) K; б) Mg; в) Be; г) Al 3.В какой паре оба гидроксида являются щелочами: а) NaOH и Al(OH)3; б) Mg(OH)2 и Ca(OH)2; в) Ba(OH)2 и KOH; г) Zn(OH)2 и LiOH 4.С каким из веществ вступит в реакцию кальций: а) H2O; б) Na2O; в) CuO; г) NaCl 5.Какой из указанных металлов является менее активным, чем алюминий: а) Са; б) Ba; в) Hg; г) K 6.Формула гипса: а) CaSO4 × 3H2O; б) CaSO4 × 0,5H2O; в) CaSO4; г) CaSO4 × 2H2O 7.В какой группе все вещества будут реагировать с гидроксидом калия: а) Ca, HI, CuCl2; б) CO2, Na, H2SO4; в) CaO, CuO, H2S; г) P2O5, HI, FeCl3 8.Что общего в строении атомов Li и Rb: а) номер периода; б) одинаковый радиус атома; в) одинаковый заряд ядра; г) 1 электрон на последнем электронном уровне 9.Какая из данных реакций показывает амфотерные свойства алюминия: а) 4Al +3O2 =2Al2O3; б) 2Al + 2NaOH +6H2O = 2Na[Al(OH)4] +3H2 ; в) 2Al + Ni2O3 = 2Ni +Al2O3; г) 2Al + 6HI = 2AlI3 +3H2 Какая масса лития образуется при электролизе 60г расплава бромида лития? Вариант 3 1.Алюминий - это: а) металл; б) неметалл; в) переходный элемент; г) нет верного ответа 2.Какой осадок образуется при взаимодействии растворов солей фосфата натрия и нитрата кальция: а) NaNO3; б) Ca3(PO4)2; в) Ca(OH)2; г) Na3PO4 3.Какой из данных металлов является щелочным: а) Ba; б) Be; в) Sr; г) Fr 4.С каким из указанных веществ реагирует алюминий: а) CaO; б) Cl2; в) NaCl; г) Na2O 5.Формула магнезита: а) CaSO4; б) MgSO4; в) ZnCO3; г) MgCO3 6.Щелочные металлы получают: а) электролизом расплавов солей; б) электролизом растворов солей; в) разложением солей при t°; г) нет верного ответа 7.В какой группе все вещества будут реагировать с гидроксидом бария: а) H2SO4, CuO, Cu; б) CO2, Si, HI; в) SO3, HCl, Na2SO4; г) Ca, CaO, CuO 8.Что общего в строении атомов Sr и Ba: а) 2 электрона на внешней электронной оболочке; б) 3 электрона на внешней электронной оболочке; в) одинаковый радиус атома; г) одинаковый номер периода 9.Какая реакция лежит в основе кальцийтермии: а) Ca + S = CaS; б) Ca + H2SO4 = CaSO4 + H2; в) V2O5 + 5Ca = 5CaO +2V; г) Ca + Cl2 = CaCl2 10. 250г оксида хрома (III), содержащего 14% примесей, восстановили водородом. Найти массу хрома. Вариант 4 1.Какой из данных металлов является щелочноземельным: а) K; б) Al; в) Fe; г) Ca 2.Какая конфигурация у атома алюминия: а) 1 s2 2s2 2p1; б) 1 s2 2s2 2p3; в) 1 s2 2s2 2p6 3s2 3p1; г) 1 s2 2s2 2p6 3s2 3p6 3d1 4s2 3.Формула поташа: а) CaCO3; б) K2CO3; в) Na2CO3; г) NaHCO3. 4.Щелочноземельные металлы получают: а) электролизом растворов; б) электролизом расплавов; в) восстановлением водородом из оксидов; г) восстановлением из оксидов алюминием 5.Что общего в строении атомов K и Na: а) одинаковый радиус атома; б) одинаковый заряд ядра; в) 3 электрона на последнем уровне; г) 1 электрон на последнем уровне 6.Какая реакция лежит в основе магнийтермии: а) MgO + H2O = Mg(OH)2; б) Mg + 2HCL = MgCL2+ H2; в) Mg + ZnCl2 = MgCl2 +Zn; г) Mg + MnO = Mn + MgO 7.С каким из веществ вступит в реакцию гидроксид калия: а) Na; б) H2O; в) CO2; г) NaCl 8.В каких группах все вещества будут реагировать с алюминием: а) H2O, HCl, BaO; б) CaO, HCl, CO2; в) Cr2O3, H2SO4, KOH; г) Na, Na2O, MnO2 9. Какой из данных металлов необходимо хранить под слоем керосина: а) Mg; б) Al; в) Be; г) K Г лития растворили в воде. Выделившийся газ пропустили над оксидом железа (III). Найти массу получившегося железа. Вариант 5 1.Какой из данных металлов является щелочным: а) Ba; б) Na; в) Mg; г) Al 2.Что общего в строении атома Be и Ra: а) одинаковый радиус; б) одинаковый заряд ядра; в) 2 электрона на последнем уровне; г) 1 электрон на последнем уровне 3.Формула гашеной извести: а) CaO; б) CaCO3; в) Ca(OH)2; г) MgO 4.С каким из веществ вступит в реакцию натрий: а) H2O; б) K2O; в) К2SO4; г) KOH 5.В каких группах все вещества будут реагировать с водой: а) Na, Be, S; б) Ca, Ba, Li; в) P,Cu, K; г) K, Ca, BeO 6.С каким из данных веществ не вступит в реакцию алюминий: а) H2SO4; б) KOH; в) Na2SO4; г) Cr2O3 7.Какие две из данных реакций подтверждают амфотерный характер оксида алюминия: а) Al2O3 + 3Mg = 3MgO + 2Al; б) Al2O3+2NaOH +3H2O = 2Na[Al(OH)4]; в) Al2O3+6HCl =2AlCl3 + 3H2O; г) Al2O3+ 3CO2 = Al2(CO3)3 8.В какой группе находятся только щелочи: а) NaOH, Ba(OH)2; б) KOH, Mg(OH)2; в) Al(OH)3, Ca(OH)2; г) Ca(OH)2, Be(OH)2 9.Какой металл в ряду Na – K – Rb – Cs обладает наименьшими металлическими свойствами: а) Rb; б) Cs; в) K; г) Na Какую массу ванадия можно получить кальцийтермией из 200г оксида ванадия (V)?
Тесты по органической химии
Непредельные углеводороды
Вариант 1 1) Как называется вещество: СН3 – СН – СН = СН – СН3 | СН3 а) н – гексан; б) 2 – метилпентен – 3; в) 4 – метилпентен – 2; г) нет верного ответа 2) Какое из данных веществ не является изомером пентена – 1: а) СН3 – СН = СН – СН2 – СН3; б) СН3 – С = СН – СН3 в) СН2___ СН2; | | | СН3 СН2 ___ СН – СН3 г) СН3 – СН2 – СН – СН3 │ СН3 3) В какой из групп все вещества взаимодействуют с раствором перманганата калия: а) метан, этан, ацетилен; б) пропен, хлорвинил, бутадиен – 1,3; в) бутин, бутен, циклобутан; г) гексен, этин, хлорметан
4) Укажите реагент, с которым взаимодействуют этиленовые углеводороды: а) Na; б) KMnO4; в) NO2; г) NH4OH
5) p – связь имеется в молекуле: а) пентана; б) циклопентана; в) пропина; г) пропана
6) Взаимодействие этилена с бромом является реакцией: а) замещения; б) присоединения; в) гидрирования; г) дегидратации
7) Ацетилен не может реагировать с: а) водородом; б) кислородом; в) водой; г) гидроксидом натрия
8) Гомологом пропина не является: а) СН º С – СН2 – СН3; б) СН2 = СН – СН3; в) СН3 – СН2 – С º СН; г) СН º С – СН2 – СН2 – СН3 9) Каучук получают, используя реакцию: а) изомеризации; б) гидрирования; в) окисления; г) полимеризации
10) Реакцию с раствором Br2 можно использовать для обнаружения: а) циклобутана; б) дихлорэтана; в) гексана; г) ацетилена
11) 4,48л этилена пропустили через 100г 6%-го р-ра брома. Найти массу продукта, если его выход составляет 95% от теоретического.
Вариант 2
1) Какая структурная формула соответствует 3-метилгексену –2: а) СН3 – СН – СН = СН ─ СН3; б) СН = С – СН2 – СН2 – СН3; ½ ½ ½ СН3 СН3 СН3
в) СН2 = СН – СН – СН3; г) СН3 – СН2 – СН2 – СН = С – СН3 ½ ½ СН3 СН3 2) У какого из перечисленных веществ возможна цис-транс-изомерия: а) 2-метилбутен –1; б) бутен –1 в) 1,2 – дихлорпропан; г) 3-метилпентен –2 3) Какой способ не используют для получения ацетилена: а) гидролиз карбида б) крекинг в) разложение г) нет верного кальция; метана; бутана; ответа 4) Укажите реакцию, не являющуюся реакцией присоединения: а) СН3 – С º С – СН3 + НCl ® СН3 – СН = С – СН3 ½ Cl hn б) СН4+3Cl2 ® СНCL3 + 3НCL
в) СН3 – СН – СН = СН2 + Вr2 ® СН3 – СН – СН – СН2 ½ ½ ½ ½ СН3 СН3 Br Br г) СН3 – СН2 – СН = СН2 + Cl2 ® СН3 – СН2 – СН ─ СН2 ½ ½ Cl Cl 5) Укажите в правильном порядке реагенты, которые нужно использовать, чтобы осуществить превращения: 1 2 3 СН3СООNa ® CH4 ® C2H2 ® CHCl = CHCl а) Cl2; б)»1000°С; в) Н2О,t°; г) NaOH, t° 6) Бутадиен относится к классу веществ, общая формула которого: а) СnH2n+2; б) Cn H2n; в) CnH2n-2; г) Cn H2n-1ОН 7) p-связь имеется в молекуле: а) циклогексана; б) пропена; в) гексана; г) 2-метилбутана 8) Природным сырьем для получения ацетилена является: а) метан; б) каменный уголь; в) нефть; г) нет верного ответа 9) С раствором КMnО4 реагируют: а) пропан и бутен; б) этилен и ацетилен; в) циклопропан и бутадиен; г) метан и пропин 10) Гомологами являются: а) бутан и бутен; б) этен и ацетилен; в) бутан и бутадиен; г) пропадиен и бутадиен – 1,2 11) Ацетилен, полученный из 200г карбида кальция, содержащего 5% примесей, подвергли полному гидрированию. Найти объем продукта гидрирования, если его выход 80% (н.у.)
Вариант 3 Cl ½ 1) Дайте названию веществу: СН3 – С – СН = СН2 ½ Сl а) 2,2 – дихлорбутен – 3; б) 3,3 – дихлорбутен – 2; в) 3,3 –дихлорбутен –1; г) 3 – хлорбутен – 1
2) Какое из данных веществ не является изомером гексена – 2:
СН2 СН2 СН – СН – С2Н5
СН2
в) СН3 – С = С ─ СН3 г) СН2 ─ СН2 ─ СН2 – СН2 ½ ½ ½ ½ СН3 СН3 СН3 СН3
3) С помощью бромной воды можно отличить: а) этин от этена; б) этан от метана; в) ацетилен от бутена; г) гексен от циклогексана 4) Какие из перечисленных реагентов и в каком порядке нужно использовать, чтобы осуществить превращения: 1 2 3 СН3 – СН2 – СН = СН2 ® СН3 – СН2 – СНBr – CH2Br ®CH3 – CH2 – C º CH ® CH3 ─ CH2 ─ C º CAg а) Ag; б) Br2; в) Ag2O (аммиачный раствор); г) КОН (избыток, спирт.) 5) Что можно использовать, чтобы отличить алкан от алкина: а) р-ры КМnO4 и Br2; б) НNO3 (k); в) Н2О; г) Н2SO4 (k) 6) При взаимодействии пропилена с бромоводородом получается: а) 1-бромпропан; б) 1,1 – дибромпропан; в) 2-бромпропан; г) 2,2- дибромпропан 7) Гомологом пропилена является: а) этилен; б) бензол; в) ацетилен; г) 2-метилпропан 8) В основе применения ацетилена для сварки металлов лежит реакция: а) CaC2 + 2Н2О ® С2Н2 + Са(ОН)2; б) 2СН4 ® С2Н2 + 3Н2; в) С2Н2 + Н2 ® С2Н4; г) 2С2Н2 + 5О2 ® 4СО2 + 2Н2О 9) p-связи нет в молекуле: а) ацетилена; б) циклобутана; в) этилена; г) бутадиена – 1,3 10) Для алкинов характерны реакции: а) присоединения; б) замещения; в) дегитратации; г) изомеризации 11) Найти массу ацетиленида серебра, полученного при взаимодействии 10л ацетилена, содержащего 8% примесей, с 40г оксида серебра (н.у.)
Вариант 4 1) Какая структурная формула соответствует 2-метилпентену-2:
а) СН3 – СН – СН = СН – СН3 б) СН2 = С – СН2 – СН2 ─ СН3 ½ ½ СН3 СН3
в) СН3 – С = СН – СН3 г) СН3 – СН2 – СН = С – СН3 ½ ½ СН3 СН3 2) Для какого из перечисленных веществ возможна цис-транс-изомерия: а) пропен; б) 2,2 – диметилпропан; в) пентен-2; г) пентин –1 3) Ацетилен не используют: а) как растворитель; б) для получения уксусной кислоты; в) для получения бензола; г) как горючее для сварки 4) Чтобы отличить ацетилен от этилена, необходимо использовать: а) бромную воду; б) хлорную воду; в) аммиачный раствор оксида серебра; г) раствор перманганата калия 5) Вещества с общей формулой CnH2n относятся к классу: а) алканы; б) алкины; в) алкены; г) нет верного ответа 6) Полиэтилен получают, используя реакцию: а) гидрирования; б) изомеризации; в) гидратации; г) полимеризации 7) Гомологом СН3 – СН2 – СН2 – СН = СН2 является: а) пентен-2; б) циклобутан; в) 2-метилбутан; г) нет верного ответа 8) Веществом, при добавлении которого к раствору КМnO4 раствор обесцветился, является: а) циклогексан; б) гексан; в) гексин; г) нет верного ответа 9) С бромной водой не реагирует: а) пропин; б) пропен; в) пропадиен; г) бутан 10) При дегидрировании этана образуется: а) метан; б) пропилен; в) этилен; г) пропин 11) 4,48л пропадиена сожгли. Выделившийся газ пропустили через 200г 40%-го р-ра гидроксида калия. Найти массу образовавшейся соли. Ароматические углеводороды Вариант 1 1. В молекуле бензола атомы углерода связаны: а) тремя простыми и тремя двойными связями б) шестью s - связями в) шестью s - связями и p - связью из шести электронов г) нет верного ответа 2. Сколько существует изомерных диметилбензолов: а) 4; б) 3; в) 2; г) 1 3. Электронные облака атомов углерода в молекуле бензола находятся в состоянии гибридизации: а) sp- б) sp3- в) sp2- г) нет верного ответа 4. Бензол, как и непредельные углеводороды, вступает в реакции: а) полимеризации; б) изомеризации; в) гидрирования; г) нет верного ответа 5. В результате какой из приведенных реакций образуется хлорбензол: hv а) C6H12 + Cl2 → в) C6H14 + 3Cl2 → t0, kt hv б) C6H6 + Cl2 → г) C6H6 + 3Cl2 → 6. Одним из способов получения бензола является реакция: а) Зелинского; б) Лебедева; в) Зайцева; г) Кучерова 7. Какой углеводород является гомологом бензола: а) С7Н8; б) С7Н16; в) С7Н14; г) С7Н12 8. При бромировании толуола, взятого количеством 1 моль, получено 230,3г бромпроизводного. Вычислить выход продукта в % от теоретического. а) 80% б) 70% в) 40% г) 90% 9. Какой продукт образуется при окислении перманганатом калия 1 – метил – 2 – этилбензола: а) м- фталевая кислота б) 1-метил – 2 –этилциклогексан в) о – фталевая кислота г) бензойная кислота 10. Представителем гомологического ряда бензола является: а) толуол б) метанол в) циклогексан г) нет верного ответа 11.* Получите все изомерные метилнитробензолы, исходя из бензола. 12.* Предложите схему получения 3- нитробензойной кислоты из этилбензола в две стадии. Укажите условия реакций.
Вариант 2 1. Бензол, как и предельные углеводороды, вступает в реакции: а) гидрирования; б) изомеризации; в) замещение на галоген; г) присоединения галогена; 2. Как можно отличить этилен от бензола: а) по цвету пламени; б) по действию бромной воды или раствора перманганата калия; в) по действию на индикатор; г) по действию известковой воды 3. Сколько существует изомерных триметилбензолов: а) 4; б) 3; в) 2; г) 1 4. В какой из реакций образуется бромбензол: kt а) С6Н6 + Br2 ® б) С6Н6 + Br2 ® hn hn в) С6Н12 + Br2 ® г) С6Н12 + Br2 ® 5. Какую общую формулу имеют ароматические углеводороды: а) СnН2n-2 б) СnН2n в) СnН2n+1OH г) СnН2n-6 6. Какие из соединений являются изомерами:
7. В лаборатории из 110,7г бензола получено 157,14г нитробензола. Каков выход продукта в % от теоретического? а) 75% б) 90% в) 45% г) 50% 8. Какое вещество образуется при окислении пропилбензола: а) бензойная кислота б) n – фталевая кислота в) пропилциклогексан г) нет верного ответа 9. Гомологами являются: а) толуол и циклогексан б) бензол и этилбензол в) стирол и ацетилен г) толуол и метилбензол 10. Какое из веществ не вступает в реакцию с раствором перманганата калия: а) толуол б) о- ксилол в) бензол г) n – ксилол 11.* Получите все изомерные этилнитробензолы, исходя из бензола. 12.* Ароматический углеводород состава C8H10 при окислении раствором перманганата калия превращается в 0–фталевую кислоту. Какую структурную формулу имеет углеводород? Напишите формулы его изомеров. Какие они дадут продукты при окислении раствором перманганата калия?
Спирты. Фенолы
Вариант 1 1) Какая структурная формула соответствует 2-метилгексанолу-3: а) СН3 – СН2 - СН – СН2 – СН – СН3 ½ | ОН СН3 б) СН3 – СН – СН – СН2 – СН3 ½ ½ СН3 ОН в) СН3 – СН2 – СН2 – СН - СН – СН3 ½ | ОН СН3 г) СН3 – СН – СН2 – СН – СН3 ½ ½ СН3 ОН 2) Какое из перечисленных веществ не является изомером бутанола-1: а) СН3 – О – С4Н9 б) СН3 – СН – СН2ОН в) С2Н5 – О – С2Н5 ½ СН3 СН3 ½ г) СН3 – С – ОН │ СН3 3)Число изомеров пентанола, отличающихся только положением гидроксильной группы, равно: а) 5; б) 4; в) 3; г) 2 4) Какое из перечисленных веществ имеет самую высокую температуру кипения: а) пропанол-2; б) бутанол-1; в) диэтиловый эфир; г) этанол 5) С каким из перечисленных веществ может взаимодействовать метанол: а) КОН; б) С2Н6; в)HCl; г) С2Н2 6) Этанол не образуется: а) при гидратации этилена; б) при гидролизе этилата натрия; в) при брожении глюкозы; г) при окислении этана 7) По какому признаку можно отличить водный раствор глицерина от водного раствора этанола: а) по действию на щелочные металлы; б) по цвету; в) по действию на свежеосажденный гидроксид меди (II); г) нет правильного ответа 9) Какое из перечисленных веществ не является фенолом:
б) - OH
10) У какого из перечисленных соединений наиболее сильно выражены кислотные свойства: а) угольная кислота; б) фенол; в) вода; г) метанол
11) С помощью какого реактива можно распознать фенол в водном растворе: а) Ag2O; б) Cu(OH)2; в) FeCl3; г) Br2
12) В результате какой химической реакции образуется этилфениловый эфир: t а) СН3СН2ОН + С6Н5ОН ® …….. H2SO4
ZnCL2 б) С6Н5ОН + СН2 = СН2 ® ……
в) С6Н5ОNa + (CH3 – CH2)2 SO4 ®……
г) С6Н5ОН + СН3 – СН3 ® …..
13) При бромировании 28,2г фенола получен осадок массой 79,44г Вычислите выход продукта в % от теоретического. а) 60% б) 75% в) 80% г) нет верного ответа
Вариант 2
1) Какая структурная формула соответствует 2,3,3-триметилбутанолу –1: СН3 СН3 | | а) СН2 – С – СН – СН3 б) СН3 – С – СН - ОН | | | | | ОН СН3 СН3 СН3 СН3
СН3 СН3 | | в) СН3 – СН – С – СН3 г) СН3 – С – СН – СН2ОН | | | | СН3 ОН СН3 СН3
2) Какое из перечисленных веществ не является изомером пентанола: СН3 | а) СН3 - О – С4Н9; б) С2Н5 – С – С2Н5; в) СН3 - С – СН2ОН; || | О СН3 г) СН3 – СН – СН – СН3 | | ОН СН3
3) Способность к образованию водородных связей является причиной одного из физических свойств спиртов: а) водные растворы неэлектропроводны; б) токсичны; в) имеют запах; г) низкомолекулярные спирты хорошо растворяются в воде
4) Дайте название веществу по систематической номенклатуре:
СН3 СН3 а) нанол - 1; | | б) 2,2,3,4-тетраметилпентанол-1; СН – СН – С – СН2ОН в) 2,2,3,4,4-пентаметилбутанол-1; | | | г) 2,3,4,4-метилпентанол-1 СН3 СН3 СН3 5) Какое из перечисленных веществ будет взаимодействовать с этанолом: а) Сu (ОН)2; б) Сl2; в) НСl; г) ВаСl2
6) Метанол не образуется: а) при восстановлении водородом из метаналя; б) при гидратации непредельных углеводородов; в) из синтез – газа; г) при гидролизе хлорметана
7) По какому признаку глицерин можно отличить от пропанола: а) по реакции с Сu(ОН)2; б) по действию на щелочные металлы; в) по растворимости в воде; г) правильного ответа нет
8) Какое вещество относится к фенолам:
а) - СH2 – CH2OH б) - СООН в) - OH
\ ОН
г) О
9) У какого из перечисленных веществ наиболее слабо выражены кислотные свойства: а) глицерин; б) фенол; в) этанол; г) угольная кислота
10) Сколько разных веществ представлено следующими названиями: а) 2-гидрокси-3-метилфенол; б) гидроксибензол; в) орто-дигидроксибензол; г) 2,3-дигидрокситолулол; д) фенол; е) 1,2,3-тригидроксибензол;
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-21; просмотров: 375; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.01 с.) |

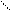





 СН2 СН2 СН3
СН2 СН2 СН3

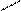 С2Н5 ∕ СН= СН2 СН3 СН3
С2Н5 ∕ СН= СН2 СН3 СН3




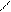



 а) б) в) СН3 г) С2Н5
а) б) в) СН3 г) С2Н5


 СН3 СН3 СН3 СН3
СН3 СН3 СН3 СН3
 а) - CH2OH
а) - CH2OH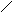 OH
OH


 в) CH3 OH
в) CH3 OH
 г) HО CH2OH
г) HО CH2OH ОН
ОН










