
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Биохимия и основы патологии липидного обменаСодержание книги
Поиск на нашем сайте
БИОХИМИЯ И ОСНОВЫ ПАТОЛОГИИ ЛИПИДНОГО ОБМЕНА
УЧЕБНОЕ ПОСОБИЕ
Киров 2014
УДК 577.125 (075.8) БКК 28.072 Я 73 В 63
Рекомендовано учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России (№ 197/05.05-20 от 09.06.2014г.).
Биохимия и основы патологии липидного обмена: учебное пособие / сост. А.В. Еликов, П.И. Цапок. – Киров: Кировская государственная медицинская академия, 2014. – 131 с.
Настоящее учебное пособие представляет собой руководство для организации самостоятельной аудиторной и внеаудиторной работы студентов медицинских вузов по одному из основных разделов биологической химии – липидный обмен. Для активного овладения изучаемым материалом студентам предлагаются обучающие тесты и клинические ситуационные задачи. Учебное пособие предназначено для студентов медицинских вузов по специальности «Лечебное дело», «Педиатрия», «Медико-профилактическое дело», «Медицинская биохимия» и «Стоматология».
Рецензенты: зав. кафедрой биологической химии ГБОУ ВПО "Курский государственный медицинский университет" Минздрава России, доктор медицинских наук, профессор, заслуженный работник высшей школы РФ, заслуженный деятель науки РФ А.И. Конопля. зав. кафедрой биологической химии ГБОУ ВПО "Пермская государственная медицинская академия имени академика Е.А. Вагнера" Минздрава России, доктор медицинских наук, профессор Н.А. Терехина.
© ГБОУ ВПО Кировская государственная медицинская академия, 2014 © Еликов А.В., Цапок П.И. - Киров, 2014 СОДЕРЖАНИЕ Предисловие……………………………………………………………………..5 Классификация и характеристика основных групп липидов. ………......6 Начальные этапы обмена липидов ………………………………………….14 Переваривание липидов в желудочно-кишечном тракте………………….....14 Всасывание продуктов гидролиза липидов……………………..…………......19 Транспорт липидов………………….……………………………………….......20 Энергетическая функция липидного обмена …..…………………………..21 Мобилизация жиров (липолиз).………………………………………………...21 Окисление жирных кислот……………………………………………………...23 Окисление глицерина…………..………………………………………………..26 Особенности окисления жирных кислот с нечетным числом атомов углерода……………………………………………………………………..……29
β-окисление жирных кислот в пероксисомах ………………………….……..30 α- и ώ-окисление жирных кислот……………………………………………….30 Нарушение окисления жирных кислот………………………………………...30 Биосинтез липидов …..…….…………………………………………………...34 Биосинтез жирных кислот……………………………………………………....34 Биосинтез кетоновых (ацетоновых) тел..……………………………………....43 Биосинтез ТАГ и фосфолипидов……….………………………………………45 Жировое перерождение печени………………………………………………...49 Биосинтез и обмен холестерола.………………………………………………..52 Транспортные формы липидов ……..………………………………………..61 Липопротеины (ЛП) плазмы крови и их классификация……………………..61 Хиломикроны……………………..……………………………………………...62 Липопротеины очень низкой плотности (пре-β-ЛП)……………………….....66 Липопротеины низкой плотности (β-ЛП). …………………………………….68 Липопротеины высокой плотности (α-ЛП)………………………………….....69 Роль липидного обмена в адаптации к мышечной деятельности..….…..72 Биохимические основы патологии липидного обмена ….………………...74 Биохимические основы атеросклероза………………………………………....74 Гиперлипопротеинемии (ГЛП)…………………………………………………80 Биохимические основы желчно-каменной болезни…………………………...98 Вопросы и задания для самоконтроля.……………………………………......101 Эталон к ответам на тестовые задания………………………………………..125 Эталон решения ситуационных задач……………………………………...…126 Рекомендуемая литература…………………………………………………….131
Список сокращений ГЛП - гиперлиполпротеинемии ЖКБ - желчно-каменная болезнь ИА - индекс атерогенности ИБС - ишемическая болезнь сердца КЭ – коэффициент эстерификации ЛП - липопротеины ЛПВП – липопротеины высокой плотности ЛПЛ -липопротеинлипаза ЛПНП – липопротеины низкой плотности ЛПОНП – липопротеины очень низкой плотности ЛППП - липопротеины промежуточной плотности ЛХАТ -лецитин-холестерол-ацилтрансфераза МДА – малоновый диальдегид ОЛ – общие липиды ОХС – общий холестерол ПОЛ – перекисное окисление липидов
СЖК - свободные жирные кислоты СХС – свободный холестерол ТАГ – триацилглицеролы ФЛ - фосфолипиды ХС – холестерол ЭХС – эстерифицированный холестерол ПРЕДИСЛОВИЕ
Липидный обмен является важнейшей составляющей обмена веществ у человека. Нарушения липидного обмена приводят к таким заболеваниям как атеросклероз и его осложнения, ожирение, онкологические заболевания и многие др. В соответствии с Федеральным Государственным образовательным стандартом третьего поколения высшего профессионального образования (ФГОС-3) преподавание биологической химии ориентировано на конечные цели обучения: создать прочную теоретическую базу, необходимую для усвоения медико-биологических и клинических дисциплин. В соответствии с учебной программой по биохимии, на основе современных научных представлений формируется понимание обмена липидов и роль нарушений липидного обмена в развитии распространенных в популяции заболеваний. При составлении данного пособия учтен большой опыт преподавания биологической химии студентам высших образовательных медицинских учреждений России и зарубежья. Представлены сведения по патохимии и клинической биохимии. Мы будем благодарны за любые замечания и пожелания, направленные на улучшение данного пособия.
1. КЛАССИФИКАЦИЯ И ХАРАКТЕРИСТИКА ОСНОВНЫХ ГРУПП ЛИПИДОВ Под названием липиды объединяют большую группу веществ биологической природы, не растворимых в воде и растворимых в органических растворителях. Липиды подразделяют на омыляемые и неомыляемые в зависимости от способности к гидролизу с образованием в щелочной среде солей высших карбоновых кислот, т.е. мыл. Классификация омыляемых липидов по Н.А. Тюкавкиной и др. представлена на рисунке 1. Неомыляемые липиды не гидролизуются в щелочной или кислой среде. Неомыляемая липидная фракция содержит вещества двух основных типов: стероиды (преобладают в липидах животного происхождения) и терпены (преобладают в липидах растительного происхождения). Главным представителем стероидов является холестерол. Наиболее важные группы липидов: 1. Жирные кислоты. Самые простые по строению липиды. В организме служат промежуточными продуктами при распаде или синтезе других липидов. Жирные кислоты являются характерными структурными компонентами большинства липидов. Представляют собой одноосновные карбоновые кислоты, содержащие от 4 до 24 углеродных атомов. Благодаря длинному неполярному «хвосту» этих кислот большинство липидов нерастворимы в воде и проявляют свойства масел и жиров. Практически все природные жирные кислоты содержат четное число атомов углерода, наиболее часто — 16 или 18. Углеводородный радикал может быть как насыщенным, так и содержащим двойные связи (в растениях и животных ненасыщенные кислоты встречаются в два раза чаще насыщенных). В природных кислотах не встречаются сопряженные двойные связи; между ними всегда находится хотя бы одна CH2-группа. В подавляющем большинстве случаев двойные связи в природных кислотах имеют цис -конфигурацию. Некоторые жирные кислоты из природных источников представлены в таблицах 1 и 2.
Рис. 1. Классификация омыляемых липидов
Таблица 1 Переваривание ТАГ Панкреатическая липаза вырабатывается в неактивном виде, активируется колипазой и желчными кислотами. Оптимум рН липазы в присутствии желчи смещается с 8 до 6, т.е. до значения рН которое бывает после приема жирной пищи в верхних отделах тонкого кишечника. Есть данные о существовании 2-х типов липаз:
1-й тип - гидролизует связи 1 и 3; 2-й тип - (карбоксиэстераза) - гидролиз связи по 2-му положению. Гидролиз жира идет в составе жировой капли на границе раздела фаз.
ДАГ 1,2-ДАГ
МАГ
Глицерин
Рис. 11. Схема гидролиза триацилглицерола (ТАГ)
Под действием панкреатической липазы отщепляется жирная кислота по 1 или 3 положению, затем еще одна и образуется 2-моноацилглицерол. 2-МАГ может всасываться через стенку кишечника, но может отсекаться еще одна жирная кислота и образуется глицерол и жирные кислоты. Таким образом, конечными продуктами гидролиза жира будут ВЖК и глицерол. Переваривание фосфолипидов Осуществляется специальными липолитическими ферментами, которые называются фосфолипазами. Существуют следующие виды фосфолипаз: А1, А2, С и D.
Рис. 12. Схема гидролиза лецитина фосфолипазами
Фосфолипаза А1 гидролизует эфирную связь в положении 1. Фосфолипаза А2 гидролизует эфирную связь в положении 2. Под действием фосфолипазы А2 образуются очень токсичные продукты лизофосфатиды - вызывают разрушение клеточных мембран. Образуются в большом количестве под действием яда змей, скорпионов (за счет высокой активности фосфолипазы А2 в яде этих животных), что приводит к гемолизу. Фосфолипаза А2, как и все ферменты является с химической точки зрения белком, причем фосфолипаза А2 содержащаяся в яде с белком, чужеродным для организма человека, с соответствующей иммунной реакцией на него. В основе терапии укуса животных обладающих ядом гемолитического действия лежит переливание иммунизированной сыворотки крови, содержащей готовые антитела к фосфолипазе А2, как к белку. Следует учитывать, что для каждого вида ядовитого животного своя сыворотка. Существуют и комбинированные сыворотки. В желудочно-кишечном тракте человека очень важно согласованное действие фосфолипаз А1 и А2 на фосфолипид. Некоторые авторы считают, что в составе панкреатического и кишечного соков существуют специальные ферменты - лизофосфолипазы, осуществляющее гидролиз лизофосфолипидов при их случайном образовании. Защита от токсического действия фосфолипазы А2 также достигается тем, что она вырабатывается в неактивном виде. Активируется трипсином путем отщепления гексапептида.
Фосфолипаза С - гидролизует связь между фосфорной кислотой и глицерином. Фосфолипаза D - гидролизует связь между фосфорной кислотой и азотистым основанием. Таким образом, под действием фосфолипаз в процессе переваривания фосфолипидов образуются следующие продукты: 1. Глицерол. 2. Высшие жирные кислоты. 3. Фосфорная кислота. 4. Азотистое основание. Гидролиз эфиров холестерола осуществляется холестеролэстеразой на холестерол и жирные кислоты. Транспорт липидов Ресинтезированные в энтероцитах ТАГ, эфиры холестерола и подавляющее большинство фосфолипидов вследствие их гидрофобности в свободном виде транспортироваться кровью не могут. Поэтому в энтероцитах из них синтезируются специальные транспортные частицы - хиломикроны (ХМ). Состав ХМ в данном пособии будет рассмотрен в главе «Транспортные формы липидов». ХМ являются крупными частицами (100-1200 нм) и поэтому сразу поступать в сосуд не могут. ХМ поступают в лимфатические капилляры кишечника, затем через лимфатические сосуды брыжейки в общий грудной лимфатический проток и оттуда через яремную вену в общий кровоток. Через 1-2 часа после приема жирной пищи наблюдается явление алиментарной гиперлипемии, т.е. увеличение общих липидов крови за счет ХМ (в основном ТАГ). Пик гиперлипемии приходится через 4-6 часов после приема жирной пищи. Плазма крови, содержащая большое количество взвешенных в ней ХМ имеет молочно-белый цвет. Такая плазма называется липимической. Через 10 - 12 часов ХМ из кровяного русла исчезают, плазма просветляется. Поэтому все биохимические исследования, особенно липидного обмена, проводятся утром, натощак. Плазма крови просветляется при работе в крови фермента - липопротеинлипазы. Данный фермент работает на поверхности эндотелия жировой ткани, сосудов, в печени. Активируется гепарином. ХМ крупные частицы и самостоятельно проникнуть в клетки не могут, поэтому осуществляется их предварительный гидролиз липопротеинлипазой. Образующиеся при этом глицерин и жирные кислоты поступают в жировую ткань, таким образом, плазма крови просветляется. В жировой ткани из них вновь синтезируются ТАГ и таким образом липиды депонируются. Мобилизация жиров (липолиз) Необходимость в жирах в качестве источника энергии возникает при: 1. Тяжелой физической работе. 2. Эмоциональном напряжении. 3. Голодании. Главными энергетическими субстратами липидного обмена являются жирные кислоты и глицерин. Источником жирных кислот и глицерина являются триацилглицеролы (ТАГ) жировых отложений. Процесс мобилизации ТАГ из жировых депо носит название липолиза и осуществляется внутриклеточными липазами.
Регуляция липолиза: Нервная - симпатическая нервная система липолиз активирует; парасимпатическая подавляет, способствует накоплению жира. Гуморальная - катехоламины (адреналин и норадреналин), глюкагон, соматотропный гормон (СТГ), тиреотропный гормон (ТТГ) - активируют; инсулин, простагландин Е и никотиновая кислота - подавляют.
Активация внутриклеточных липаз носит название липолитический каскад Стайнберга.
рецептор модифицированный рецептор
неактивная активная аденилатциклаза аденилатциклаза
АТФ ц АМФ
неактивная активная протеинкиназа протеинкиназа
неактивная активная липаза липаза
ТАГ ДАГ + ЖК
МАГ + ЖК
ГЛ + ЖК Рис. 13. Схема липолитического каскада (Т.Т. Березов, Б.Ф. Коровкин, 2007) Таким образом, в ходе липолиза образуются глицерин и жирные кислоты. Глицерин хорошо растворим в воде, поэтому переносится кровью в растворенном состоянии, а свободные жирные кислоты переносятся альбуминами плазмы крови. Свободные жирные кислоты - одна из форм транспорта липидов в крови. Нормальное содержание составляет 0,08 - 0,20 г/л, или 0,3 - 0,9 ммоль/л. Отдельные жирные кислоты в процентах от общего количества составляют: олеиновая кислота - 26 - 45, пальмитиновая кислота - 20 - 25, стеариновая кислота - 10 - 14, линолевая кислота - 8 - 16. Увеличение концентрации жирных кислот в крови происходит при феохромоцитоме, болезни Гирке, алкоголизме, неконтролируемом сахарном диабете, печеночной энцефалопатии, врожденном нарушении метаболизма жирных кислот (болезни Рефсума), а также при введении гепарина, кофеина, резерпина, адреналина и др. Снижение содержания жирных кислот отмечено при муковисцидозе, а также при введении аспарагиназы, никотиновой кислоты, пропрапанола, клофибрата, инсулина, сахарозы, глюкозы и др. Окисление жирных кислот Процесс извлечения энергии из жирных кислот носит название β-окисление или по имени авторов внесших наибольший вклад в изучение данного процесса - цикл Кноопа-Линена. Процесс β-окисления протекает в 3 стадии. 1 стадия. Активация жирных кислот. Происходит в цитоплазме. Реакция заключается во взаимодействии свободной жирной кислоты (ацила) с коферментом А, с образованием ацил-КоА. O O ║ Ацил-КоА-синтетаза (тиокиназа) ║
АТФ АМФ+ ФФн Рис. 14. Схема активации жирной кислоты в цитоплазме клеток Процесс β-окисления протекает в матриксе митохондрий, а образовавшийся ацил-КоА не проходит через внутреннею мембрану митохондрий. Данная проблема решается путем функционирования специального переносчика - карнитина. Карнитин синтезируется из лизина и метионина в печени и почках. Особенно много в мышцах. Химическое строение карнитина представлено на рисунке 15.
(CH3)3+N - CH2 - CHOH - CH2 - COOH
Рис. 15. Химическое строение карнитина (γ-триметиламино-β-гидроксибутират)
При действии карнитин-ацилтрансферазы к спиртовой группе карнитина присоединяется жирная кислота (сложноэфирной связью):
Ацил-SКоА + Карнитин ó Ацилкарнитин + НSКоА
Ацилкарнитин может диффундировать в митохондрию. Окисление глицерина Обмен глицерина тесно связан с гликолизом. В первой реакции глицерин активируется глицеролкиназой. В дальнейшем активированный глицерин - глицерол-3-фосфат включается в процесс гликолиза. Ниже представлена схема включения глицерина в обмен веществ для получения энергии:
│ Глицеролкиназа │ Глицерол-3-Ф-ДГ │ │
ЦПЭ гликолиз АТФ (23-1) АТФ
Рис. 18. Схема включения глицерина в гликолиз
Таким образом, при полном окислении глицерина до СО2 и Н2О образуется 22 молекулы АТФ. БИОСИНТЕЗ ЛИПИДОВ Биосинтез липидов (липогенез) необходим для создания запасных форм. Биосинтез липидов начинается с биосинтеза жирных кислот. Биосинтез жирных кислот Система синтеза жирных кислот находится в растворимой цитоплазматической фракции многих органов и тканей, таких какпечень, почки, молочная железа, жировая ткань. Биосинтез жирных кислот протекает с участием: 1. НАДФН∙Н+ ; 2. АТФ; 3. Mg2+; 4. НСО3-; 5. ацетил-КоА в качестве субстрата и пальмитиновая кислота в качестве конечного продукта. Митохондрия Цитоплазма
Ацетил-КоА + оксалоацетат ацетил-КоА + оксалоацетат + АДФ + Фн
цитрат-синтаза
НО - С - СООН цитрат + АТФ + HSKoA
СН2 - СООН
цитрат
Рис. 20. Схема транспорта ацетил-КоА через мембрану митохондрий Цитрат образуется в митохондриальном матриксе путем конденсации ацетил-КоА и оксалоацетата. Затем диффундирует в цитоплазму, где расщепляется цитратлиазой. Таким образом, ацетил-КоА и оксалоацетат переносятся из митохондрий в цитоплазму с использованием одной молекулы АТФ. Источники НАДФН·Н+ для биосинтеза жирных кислот Оксалоацетат, образовавшийся в результате переноса ацетил-КоА в цитоплазму должен быть возвращен обратно в митохондрию. Данный процесс сопряжен с генерацией НАДФН·Н+. Реакция происходит в цитоплазме и протекает в 2 этапа:
МДГ
МДГ (декарбоксилирующая)
Образовавшийся пируват легко диффундирует в митохондрии, где он карбоксилируется в оксалоацетат под действием пируваткарбоксилазы (с затратой энергии АТФ).
Нормальное окисление жиров в организме тесно связано с циклом Кребса. Основной путь образования оксалоацетата - карбоксилирование ПВК. Для сгорания 1,5 г жирных кислот, требуется 1 г углеводов. Отсюда, среди биохимиков есть поговорка, что «жиры сгорают в пламени углеводов». Оксалоацетат, который синтезировался в данной реакции, затем взаимодействует с ацетил-КоА с образованием цитрата, который окисляется в ЦТК. Таким образом, на каждую молекулу ацетил-КоА, которая переходит из митохондрий в цитоплазму, образуется одна молекула НАДФН·Н+. Следовательно, при переходе 8 молекул ацетил-КоА необходимых для синтеза пальмитиновой кислоты, образуется 8 молекул НАДФН·Н+. Еще 6 молекул требуемых для этого процесса генерируются в пентозофосфатном пути. II этап - образование малонил-КоА. Является первой реакцией биосинтеза жирных кислот. Катализируется ферментом ацетил-КоА-карбоксилазой. Коферментом является биотин. Реакция заключается в карбоксилилировании ацетил-КоА, источником СО2 является бикарбонат. H3C COOH │ Mg2+ │
│ │ SKоA C = O │ SKоA ацетил - KоA малонил - KоA
Рис. 21. Карбоксилирование ацетил-КоА (коферментом ацетил-КоА-карбоксилазы является биотин) Малонил-КоА, по сути, является активированным ацетил-КоА. Энергия запасается заранее в виде карбоксильной группы и освобождается при декарбоксилировании непосредственно при биосинтезе жирных кислот. В дальнейшем биосинтезе жирных кислот ацетил-КоА используется как затравка, а непосредственно синтез идет из малонил-КоА. III этап - биосинтез жирных кислот. HS - ФП - 2 - CYS - SH
Каждый мономер включает 6 индивидуальных ферментов и ацилпереносящий белок (АПБ). При этом тиольная группа цистеина (-CYS-SH) одного мономера находится в непосредственной близости от тиольной группы 4-фосфопантетеина (-ФП-SH) другого мономера. Это указывает на расположение мономеров по типу «голова к хвосту». Каждый из мономеров включает все ферменты, катализирующие биосинтез жирных кислот. В состав функциональной единицы входят фрагменты обоих мономеров. При этом половина одного мономера взаимодействует с комплементарной половиной другого мономера. Синтетазный комплекс катализирует одновременный синтез 2-х молекул жирных кислот.
Рис. 22. Схема строение пальмитатсинтетазы
Биосинтез жирных кислот
Трансацилаза Ацетил-КоА (ацетилтрансацилаза) HS-KoA
Ацил (ацетил) - фермент Малонил-КоА Трансацилаза (малонилтрансацилаза) HS-KoA
3-Кетоацилсинтаза
CO2
Ацетоацетил-фермент НАДФН2 3-Кетоацилредуктаза НАДФ+
Гидроксиацил-фермент
Гидратаза Н2О
(кротонил-Е)
Еноилредуктаза НАДФ+
Ацил-фермент
Трансацилаза 7 циклов
Пальмитоил-Е Н2О Тиоэстераза Е Пальмитиновая кислота Рис. 23. Схема синтеза пальмитиновой кислоты
Для синтеза пальмитиновой кислоты требуется 7 таких циклов, соответственно требуется 7 остатков малонил-КоА и один ацетил-КоА. Образовавшийся пальмитоил-Е гидролизуется тиоэстеразой с образованием свободной жирной кислоты. CH3-C(О)-SКоА + НООC-C(О)-SKoA + 14НАДФН∙Н+ →
Н3С-(СН2)14-СООН + 7CO2 + 14НАДФ+ + 8КоАSH + 6Н2О Рис. 24. Суммарное уравнение биосинтеза пальмитиновой кислоты Таблица 3 Ацетил-КоА
Пальмитиновая кислота -2Н +С2
Пальмитоолеиновая Стеариновая кислота кислота (16:1) +С2 (18:0) -2Н
+С2
+С2 Олеиновая кислота (18:1) Лигноцериновая +С2 кислота (24:0) +С2
+С2
Невроновая кислота (24:1)
Рис. 25. Схема путей биосинтеза жирных кислот в организме Синтез линоленовой и арахидоновой кислот возможен по схеме:
Линолевая кислота (поступает с пищей) 18: 2 (9, 12)
Линоленовая кислота
+ С2 - 2Н
Арахидоновая кислота 20: 4 (5, 8, 11, 14) Рис. 26. Схема синтеза полиненасыщенных жирных кислот в организме
При этом обязательным условием является поступление с пищей линолевой кислоты.
Биосинтез ТАГ Две молекулы ацил-КоА взаимодействуют с глицерол-3-фосфатом. В результате образуется 1,2-диацилглицеролфосфат (фосфатидная кислота). H2C - OH H2C - OН
H2C - OH АТФ АДФ H2C - O -
Глицерол Глицерол-3-фосфат
H2C - OH H2C - O - CO - R
H2C - O - PO3H2 2 ацил-КоА 2 КоАSH H2C - O - PO3H2
Глицерол-3-фосфат Фосфатидная кислота
Рис. 28. Образование фосфатидной кислоты
Фосфатидная кислота является ключевым метаболитом как в синтезе ТАГ, так и фосфолипидов. Если веществ, которые способствуют биосинтезу фосфолипидов мало, то активируется синтез ТАГ, если много, то синтезируются преимущественно фосфолипиды. Эти вещества называются липотропные факторы. В том случаи если синтезируются ТАГ, то: H2C - O - CO - R
- Н3РО4 H2C - OH Диацилглицерин H2C - O - CO - R H2C - O - CO - R
H2C - OH Ацил-КоА КоАSH H2C - O - СО - R''
ДАГ ТАГ
Рис. 29. Синтез ТАГ из фосфатидной кислоты
Синтезированные ТАГ накапливаются в клетках в виде жировых включений. Нормальное содержание в крови ТАГ составляет 0,5-1,5 г/л, в плазме концентрация несколько ниже, чем в крови. С возрастом содержание ТАГ увеличивается. Желательные уровни для мужчин - 0,45-1,84 ммоль/л, для женщин - 0,40-1,53 ммоль/л. Повышение концентрации ТАГ отмечается при введении кортикостероидов, эстрогенов, пероральных контрацептивов, этанола, при стрессе, диете с высоким содержанием углеводов, гиперлипопротеинемии I, IIб, III, IV типов, вирусном гепатите, циррозе печени, обтурации желчных путей, панкреатите, нефротическом синдроме, гипертонической болезни, ИБС, гипотиреозе, сахарном диабете, подагре, талассемии. Снижение концентрации ТАГ происходит при введении аскорбиновой кислоты, гепарина, при абеталипопротеинемии, хронических обструктивных заболеваниях легких, гиперпаратиреозе, недостаточности питания, синдроме мальабсорбции. Биосинтез фосфолипидов При наличии достаточного количества липотропных факторов может идти 2-ми путями. И в том и другом случае требуется ЦТФ. 1-й путь (основной) связан с активацией фосфатидной кислоты (рис. 30).
+ серин ЦМФ
- СО2 (кефалин) +3СН3 (лецитин)
Рис. 30. Схема основного пути биосинтеза фосфолипидов
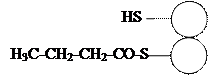
2-й путь (запасной) синтеза фосфолипидов осуществляется в том случае, если с пищей поступает достаточное количество холина. Этот путь связан с предварительной активацией холина (рис 31).
O ║ CH2 – O –C – R │ O │ ║
│ ЦМФ CH2 – OH
ДАГ Рис. 31. Схема запасного пути биосинтеза фосфатидилхолина (лецитина)
Фосфолипиды в организме осуществляют активный транспорт жирных кислот из печени. Нарушение синтеза фосфолипидов ведет за собой жировое перерождение печени, т.е. ТАГ заменяют соединительную ткань печени. Кроме того, фосфолипиды входят в состав клеточных мембран. Нормальное содержание в сыворотке крови составляет 2,52 - 2,91 ммоль/л, или 1,25 - 2,75 г/л, у людей старше 65 лет - 1,90 - 3,65 г/л, у детей - 1,80 - 2,95 г/л. Увеличение содержания фосфолипидов отмечается при холестазе, легких формах гепатита, гиперлипопротеинемии IIа и IIб, алкоголизме, циррозе печени, панкреатите, нефротическом синдроме, болезни Гирке, приеме эстрогенов, пероральных контрацептивов. Снижение концентрации имеет место при тяжелых вирусных гепатитах, гипертиреозе, танжерской болезни, абеталипопротеинемии, перницетозной анемии, серповидно-клеточной анемии, рассеянном склерозе. Нарушение метаболизма фосфолипидов, главным образом сфинголипидов, может иметь наследственный характер - сфинголипидоз. При этом развиваются такие состояния, как генерализованный ганглиозидоз, синдром Тея-Сакса, синдром Фабри, болезни Гоше, Краббе, Нимана-Пика, метахроматическая лейкодистрофия. В зависимости от метода разделения в сыворотке крови выделяют 5 - 11 фракций фосфолипидов в следующем соотношении: фосфатидилхолин - 74,5 %, сфингомиелин - 15,2 %, лизофосфатидилхолин - 6,5 %, фосфатидилэтаноламин - 2,1 %, фосфатидилинозитол - 1,7 %. Указывают также на наличие в сыворотке крови фракций лизофосфатидилэтаноламина, фосфатидилглицерина, фосфатидилсерина, кардиолипина и фосфорных кислот лецитина. Жировое перерождение печени По различным причинам, липиды, главным образом ТАГ, могут накапливаться в печени. Избыточное накопление жира рассматривается как патологическое состояние. Когда накопление становится хроническим, в клетках печени происходят фиброзные изменения, приводящие к фиброзу печени. Существует два типа жирового перерождения. 1-й тип связан с увеличением свободных жирных кислот в плазме крови. Возникает при: 1. Голодании. 2. Длительном потреблении пищи богатой жирами. 3. Сахарном диабете. 1-й тип жирового перерождения обусловлен либо повышенной мобилизацией жира из жировых депо, либо повышенным гидролизом транспортных форм липидов липопротеинлипазой. Образующегося в печени количества липопротеинов оказывается недостаточным для утилизации поступающих жирных кислот, которые накапливаются в печени в виде ТАГ, вызывая ее перерождение. 2-й тип жирового перерождения связан с нарушением образования транспортных форм лип
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 2237; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.16.44 (0.019 с.) |



 ТАГ
ТАГ



 Гормон
Гормон R - C - OH + КоА R - C - O - S KoA
R - C - OH + КоА R - C - O - S KoA
 H O
H O H2C - OH
H2C - OH 




 │ АТФ АДФ │ НАД+ НАДН·Н+ │ │
│ АТФ АДФ │ НАД+ НАДН·Н+ │ │




 СН2 - СООН цитрат-лиаза
СН2 - СООН цитрат-лиаза

 1. Оксалоацетат + НАДН·Н+ Малат + НАД+
1. Оксалоацетат + НАДН·Н+ Малат + НАД+ 2. Малат + НАДФ+ Пируват + СО2 + НАДФН·Н+
2. Малат + НАДФ+ Пируват + СО2 + НАДФН·Н+ Пируват + НСО3- + АТФ Оксалоацетат + АДФ + Фн
Пируват + НСО3- + АТФ Оксалоацетат + АДФ + Фн C = O + HCO3- + АТФ Е– биотин CН2+ АДФ+H3PO4
C = O + HCO3- + АТФ Е– биотин CН2+ АДФ+H3PO4

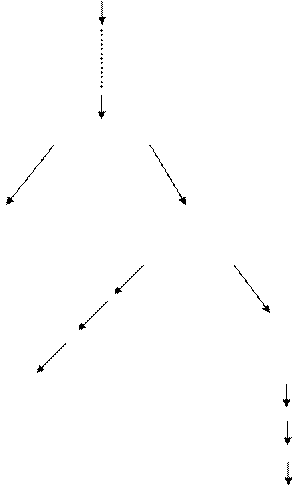
 Ацил (ацетил)-малонил-фермент
Ацил (ацетил)-малонил-фермент

 2,3-Ненасыщенный ацил-фермент
2,3-Ненасыщенный ацил-фермент
 НАДФН2
НАДФН2
 - 2Н
- 2Н




 H - C - OH
H - C - OH  H - C - OH
H - C - OH


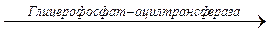 H - C - O - CO - R'
H - C - O - CO - R'
 Фосфатидная к-та
Фосфатидная к-та  H - C - O - CO - R'
H - C - O - CO - R'
 H - C - O - CO - R'
H - C - O - CO - R'



 Фосфатидная +ЦТФ Н2С - О - СО - R + инозит Фосфатидил-
Фосфатидная +ЦТФ Н2С - О - СО - R + инозит Фосфатидил- кислота ФФ Н-С - О - СО - R' инозитол
кислота ФФ Н-С - О - СО - R' инозитол
 Н2С - О - ЦДФ ЦМФ
Н2С - О - ЦДФ ЦМФ
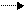 Фосфатидилсерин Фосфатидилэтаноламин Фосфатидилхолин
Фосфатидилсерин Фосфатидилэтаноламин Фосфатидилхолин
 ХОЛИН + АТФ ХОЛИНФОСФАТИД + ЦТФ ЦДФ – ХОЛИН + Фф
ХОЛИН + АТФ ХОЛИНФОСФАТИД + ЦТФ ЦДФ – ХОЛИН + Фф
 CH – O – C – R' + ЦДФ – холин лецитин
CH – O – C – R' + ЦДФ – холин лецитин


