
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Термодинамические функции. Функции состояния: внутренняя энергия, энтальпия, энтропия. Функции процесса: теплота, работа, располагаемая работа.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
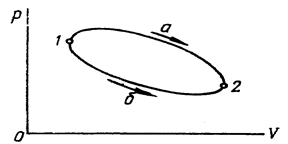
Графическое представление термодинамического процесса и его анализ: применение v-p координат для графического анализа совершения или затраты работы в термодинамическом процессе; применение s - T координат для графического анализа подвода или отвода теплоты в термодинамическом процессе. К функциям состояния относятся внутренняя энергия U, Дж; энтальпия Н, Дж; энтропия S, Дж/К. Изменение этих функций не зависит от пути процесса, а определяется лишь начальным и конечным состояниями рабочего тела. В процессах на рис.2.1
В круговом процессе 1а2б1:
Рис. 2.1 Внутренняя энергия
Для идеального газа
Здесь и далее в процессах с изменением температуры, в обозначении средних теплоемкостей, пределы изменения температуры для сокращения записи не приводятся. Для смеси газов
Энтальпия Энтальпия – сумма внутренней энергии и потенциальной энергии давления Для 1 кг Для идеального газа
Для смеси газов Энтропия Энтропия – функция, элементарное изменение которой равно отношению элементарной подведенной (отведенной) теплоты к абсо-
Для 1кг
В координатах sT (рис.2.2.) площадь под линией процесса (пл. 1’122’1’) соответствует подведенной (отведенной) теплоте. Так как всегда при при Рис.2.2 Функции процесса Работа L, Дж; располагаемая работа L0, Дж. Значения этих функций зависят как от начального и конечного состояний газа, так и от пути процесса.
Работа
Рис. 2.3 Для 1 кг
Работа зависит от пути процесса (работа - функция процесса). Рис.2.4 Располагаемая работа
Для 1 кг
В координатах vp (рис.2.5)
Рис.2.5 1)
2)
3)
Первый закон термодинамики: его формулировки и математические выражения. Первый закон термодинамики Первый законтермодинамики - частный случай всеобщего закона сохранения энергии, который гласит: энергия не исчезает и не создается вновь, она может лишь переходить от одного тела к другому или превращаться из одного вида в другой в равных количествах. В термомеханической системе теплота превращается в работу, а работа - в теплоту в равных количествах. В замкнутой системе, состоящей из теплового аккумулятора с запасом энергии Q, рабочего тела с внутренней энергией U, механического аккумулятора с запасом энергии L, dQ+ dU+ dL=0, т.е. алгебраическая сумма изменения энергии элементов системы равна нулю. Если dQ – теплота, подводимая к рабочему телу, то dQ= dU+ dL. (2.15) Для 1 кг В конечных разностях: Формулировки первого закона термодинамики. · Теплота, подводимая к рабочему телу, затрачивается на изменение его внутренней энергии и совершение им работы. · Невозможно в каком-либо механизме периодически получать работу без подвода энергии извне. · Вечный двигатель (perpetuum mobile) первого рода невозможен.
Вечный двигатель первого рода – гипотетический двигатель, способный производить работу, не получая энергию извне. Вторая форма математического выражения первого закона термодинамики:
· Теплота, подведенная к рабочему телу, затрачивается на увеличение его энтальпии и располагаемой работы.
Термодинамические процессы С идеальным газом
|
||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 487; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.219.74.193 (0.01 с.) |

 ;
;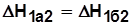 ;
;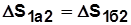 .
.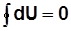 ;
; 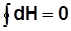 ;
; 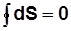 .
.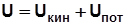 .
.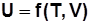 . Для 1 кг
. Для 1 кг 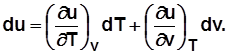
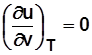 и
и 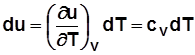 .
.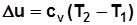 , Дж/кг; (2.1)
, Дж/кг; (2.1)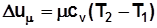 , Дж/кмоль; (2.2)
, Дж/кмоль; (2.2)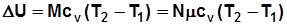 , Дж. (2.3)
, Дж. (2.3)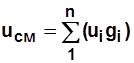 ; (2.4)
; (2.4)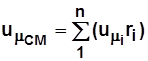 . (2.5)
. (2.5)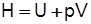 или энергия, затрачиваемая на перевод газа из абсолютного вакуума в данное состояние при р=const,
или энергия, затрачиваемая на перевод газа из абсолютного вакуума в данное состояние при р=const, 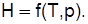
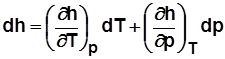 .
.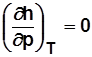 и
и 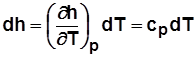 .
.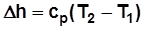 , Дж/кг; (2.6)
, Дж/кг; (2.6)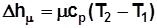 , Дж/кмоль; (2.7)
, Дж/кмоль; (2.7)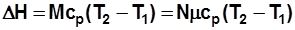 , Дж. (2.8)
, Дж. (2.8)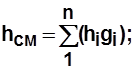 (2.9)
(2.9)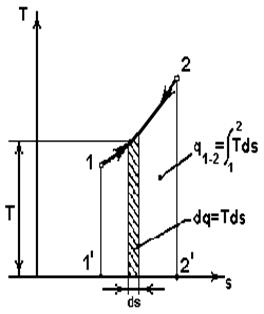 лютной температуре:
лютной температуре: 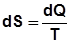 .
.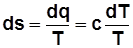 , где с – теплоемкость в данном процессе.
, где с – теплоемкость в данном процессе.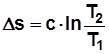 , Дж/(кг K); (2.11)
, Дж/(кг K); (2.11)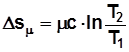 ,Дж/(кмоль К). (2.12)
,Дж/(кмоль К). (2.12)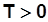 , то:
, то: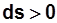
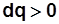 - подвод теплоты,
- подвод теплоты,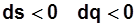 –отвод теплоты.
–отвод теплоты.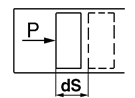
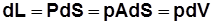 , где Р, р – сила и давление газа; А – площадь поршня; dS – элементарное перемещение (рис. 2.3.).
, где Р, р – сила и давление газа; А – площадь поршня; dS – элементарное перемещение (рис. 2.3.).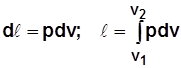 . (2.13)
. (2.13)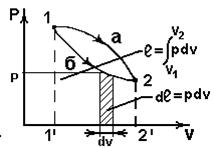 В координатах vp (рис.2.4)
В координатах vp (рис.2.4)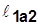 ~пл.1’1a22’1’;
~пл.1’1a22’1’;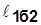 ~пл.1’1б22’1’;
~пл.1’1б22’1’; 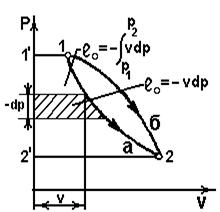 Располагаемая работа – работа изменения давления, т.е. работа, которую может совершить рабочее тело при истечении в окружающую среду под действием разности давлений тела и среды,
Располагаемая работа – работа изменения давления, т.е. работа, которую может совершить рабочее тело при истечении в окружающую среду под действием разности давлений тела и среды, 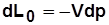 .
.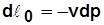 ;
;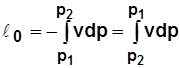 . (2.14)
. (2.14)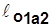 ~пл.1’1a22’1’;
~пл.1’1a22’1’; 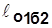 ~пл.1’1б22’1’;
~пл.1’1б22’1’;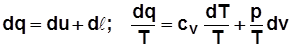 . С учетом
. С учетом 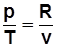 получим
получим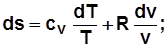
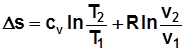 ; (2.18)
; (2.18)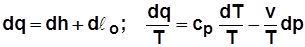 . С учетом
. С учетом 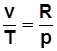 получим
получим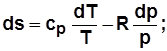
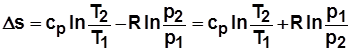 ; (2.19)
; (2.19)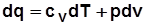 . Дифференцируя выражение
. Дифференцируя выражение 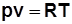 , получим
, получим 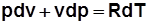 , отсюда
, отсюда 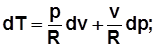
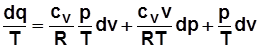 ;
;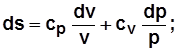
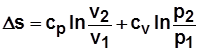 . (2.20)
. (2.20)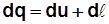 (математическое выражение первого закона термодинамики, первая форма).
(математическое выражение первого закона термодинамики, первая форма).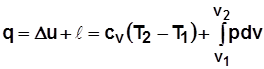 . (2.16)
. (2.16)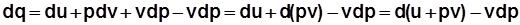 ;
;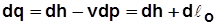 ; (2.17)
; (2.17)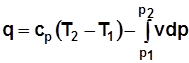 . (2.17а)
. (2.17а)


