
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Повышенный уровень сложности. 24. Все атомы углерода находятся в состоянии sp2-гибридизации в молекулах 1)Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
24. Все атомы углерода находятся в состоянии sp2-гибридизации в молекулах
25. Дивинил взаимодействует с
26. Для бутадиена-1,3 характерны
27. Изопрен в отличие от дивинила
28. И бутадиен-1,3, и бутен-1
29. Максимальная масса брома, которую может присоединить бутадиен-1,3 объемом 4,48 л (н.у.), равна _________ г. (Запишите число с точностью до целых.)
30. Максимальный объем (н.у.) водорода, который может присоединить бутадиен-1,3 объемом 150 л (н.у.), равен _________ л. (Запишите число с точностью до целых.) 31. Смесь бутана и бутадиена-1,2 объемом 0,448 л (н.у.) может максимально обесцветить 50 г бромной воды с массовой долей брома 3,2%. Объемная доля бутадиена-1,2 в исходной смеси газов равна _________ %. (Запишите число с точностью до целых.)
32. Объем углекислого газа (н.у.), который получится при полном сгорании 60 л (н.у.) дивинила, равен _________ л. (Запишите число с точностью до целых.)
33. Объем кислорода (н.у.), который необходим для полного сгорания 20 л (н.у.) дивинила, равен _________ л. (Запишите число с точностью до целых.) 34. Объем воздуха (н.у.), который необходим для полного сгорания 34 г изопрена, равен _________ л. (Запишите число с точностью до целых.)
35. Для получения бутадиена-1,3 по методу С.В. Лебедева взяли 920 мл этанола (плотность 0,8 г/мл). Выход продукта реакции составил 70%. Объем (н.у.) полученного бутадиена-1,3 равен _________ л. (Запишите число с точностью до десятых.)
Высокий уровень сложности
36. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: СО → С2Н6 Укажите условия протекания реакций.
37. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: пентанол-1 → изопрен Укажите условия протекания реакций.
38. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: СН3Вr → С2Н6 → C2H4 Укажите условия протекания реакций.
39. (С4) Смесь бутена-1 и бутадиена-1,2 объемом 1,12 л (н.у.) может максимально обесцветить 400 г бромной воды с массовой долей брома 3,2%. Определите объемную долю бутена-1 в исходной смеси газов.
40. (С4) Для полного гидрирования смеси бутена-2 и бутадиена-1,2 объемом 5,6 л (н.у.) израсходовали водород, выделившийся при взаимодействии цинка массой 19,5 г с 400 г соляной кислоты с массовой долей НСl 7,3%. Определите объемные доли газов в исходной смеси. 41. (С5) Относительная плотность паров алкадиена по кислороду равна 2,125. Установите молекулярную формулу алкадиена. 42. (С5) Алкадиен массой 20,4 г может максимально присоединить 13,44 л (н.у.) водорода. Установите молекулярную формулу алкадиена.
43. (С5) Алкадиен массой 4,1 может вступить в реакцию присоединения с бромом, образуя при этом 20,1 г тетрабромпроизводного. Установите молекулярную формулу алкадиена. 44. (С5) В результате сгорания алкадиена образовалось 17,6 г углекислого газа и 5,4 г воды. Установите молекулярную формулу алкадиена. 45. (С5) Для полного сгорания алкадиена потребовалось 3,136 л (н.у.) кислорода, в результате чего образовалось 4,4 г углекислого газа. Установите молекулярную формулу алкадиена.
Алкины
Базовый уровень сложности
1. Молекулярная формула алкинов
2. К соединениям с общей формулой СnН2n-2 относятся
3. Алкином может быть вещество, формула которого
4. Гомологом пропина является вещество, структурная формула которого
5. Пространственные цис-транс - изомеры имеет
6. Бутин-1 и бутадиен-1,3 являются
7. Последовательности алкан – алкен – алкин может соответствовать ряд веществ
8. В молекуле ацетилена атомы углерода находятся в состоянии гибридизации
9. В молекуле пропина атомы углерода находятся в состоянии гибридизации
10. Длина связи С≡С и валентный угол в молекулах алкинов соответственно равны
11. Число σ-связей в молекуле ацетилена равно
12. Число π-связей в молекуле пентина-1 равно
13. Геометрическая конфигурация молекулы этина
14. Раствор KMnO4 обесцвечивают оба вещества в ряду
15. Бромную воду обесцвечивают оба вещества в ряду
16. И этин, и этан взаимодействуют с
17. И пропин, и пропен взаимодействуют с
18. При гидратации ацетилена образуется
19. С каждым из трех веществ: бромом, бромоводородом, натрием – может реагировать
20. Реакция тримеризации ацетилена используется для получения
21. В результате реакции Кучерова образуется
22. При гидролизе карбида кальция образуются
23. Ацетилен в одну стадию можно получить из
24. Ацетилен в промышленности получают, используя
25. Пропин можно получить по реакции, схема которой
26. Этин можно отличить от этана с помощью
27. Пропин можно отличить от пропена с помощью
28. Бутин-2 можно отличить от бутина-1 с помощью
29. Какие из приведенных утверждений об алкинах и их свойствах верны? А. Алкины изомерны алкадиенам. Б. При полном гидрировании алкинов получают алкены.
30. Какие из приведенных утверждений об ацетилене и его свойствах верны? А. Ацетилен хорошо растворим в воде. Б. Ацетилен образует с воздухом взрывоопасные смеси.
31. Какие из приведенных утверждений об ацетилене и его свойствах верны? А. Атомы углерода в молекуле ацетилена находятся в sp-гибридном состоянии. Б. Ацетилен горит в кислороде коптящим пламенем.
32. Какие из приведенных утверждений об ацетилене и его свойствах верны? А. Молекула ацетилена имеет линейное строение. Б. Ацетилен в промышленности получают высокотемпературным пиролизом метана.
33. Какие из приведенных утверждений об ацетилене и его свойствах верны? А. Ацетилен – газ с резким запахом. Б. Ацетилен используется для сварки и резки металлов.
34. Какие из приведенных утверждений о пропине и его свойствах верны? А. Молекула пропина содержит атом углерода в sp2-гибридном состоянии. Б. В результате гидратации пропина образуется пропаналь.
35. Какие из приведенных утверждений о пропине и его свойствах верны? А. В молекуле пропина содержится тетраэдрический фрагмент атомов. Б. Пропин можно отличить от пропана с помощью бромной воды.
36. Какие из приведенных утверждений о бутине-2 и его свойствах верны? А. Для бутина-2 характерна цис-транс -изомерия. Б. Бутин-2 взаимодействует с натрием с выделением водорода.
37. В схеме превращений CaC2 веществами Х1 и Х2 являются соответственно
38. В схеме превращений CH3COONa веществами Х1 и Х2 являются соответственно
39. В схеме превращений CH4 веществами Х1 и Х2 являются соответственно
40. В схеме превращений CaC2 веществами Х1 и Х2 являются соответственно
41. В схеме превращений C2H6 веществами Х1 и Х2 соответственно являются
42. В схеме превращений CH2Br-CH2Br веществами Х1 и Х2 соответственно являются
43. В схеме превращений C2H2 веществами Х1 и Х2 являются соответственно
44. В схеме превращений пропин веществами Х1 и Х2 являются соответственно
45. В соответствии с термохимическим уравнением реакции 2С2Н2 + 5O2 = 4CO2 + 2H2O + 2610 кДж при сгорании 26 г ацетилена количество выделившейся теплоты равно
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 1275; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.137 (0.01 с.) |

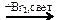 Х1 → СН3СН2СН2СН3 → бутадиен-1,3
Х1 → СН3СН2СН2СН3 → бутадиен-1,3 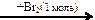 Х2
Х2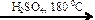 Х1 → н-пентан → 2-метилбутан →
Х1 → н-пентан → 2-метилбутан →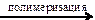 Х2
Х2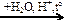 Х1 → бутадиен-1,3
Х1 → бутадиен-1,3 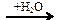 X1
X1 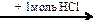 X2
X2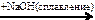 X1
X1 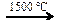 X2
X2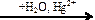 Х2
Х2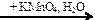 Х2
Х2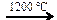 X1
X1 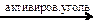 Х2
Х2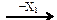 C2H2
C2H2 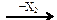 CH2=CHCl
CH2=CHCl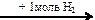 X1
X1 


