
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Структура и физические свойства сплавов железо-углеродСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Основой для определения структуры и свойств железоуглеродистых сплавов является диаграмма состояния железо-углерод (рисунок 2.6). Данная диаграмма показывает, какие фазы и структурные составляющие существуют в различных температурных интервалах при разном содержании углерода. На диаграмме точка 2,14% по оси абсцисс делит ее на две части. Левее данной точки находится область сталей, правее располагается область чугунов. До концентрации 0,8% находятся доэвтектоидные стали, после 0,8% - заэвтектоидные. С ростом содержания углерода в стали увеличивается предел прочности, текучести и твердости. В тоже время ударная вязкость и относительное удлинение уменьшаются. Обычные конструкционные стали имеют предел прочности порядка 300…700 МПа и должны без какой – либо обработки хорошо свариваться. При большом содержании углерода это становится затруднительным, особенно при таком его содержании, как в чугунах. Основными компонентами железоуглеродистых сплавов являются железо, углерод и цементит. Железо – переходной металл серебристо-светлого цвета. Имеет высокую температуру плавления – около 1539 оС. В твердом состоянии железо может находиться в двух модификациях. Полиморфные превращения происходят при температурах 911оС и 1392 оС. При температуре ниже 911 оС существует При температуре ниже 768 оС железо ферримагнитно, а выше – парамагнитно. Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (предел прочности 250 МПа, предел текучести 120 МПа) и высокими характеристиками пластичности (относительное удлинение 50 %, а относительное сужение 80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов. Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения. Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 оС, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000 оС). В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в некоторых чугунах). Феррит (Ф) – твердый раствор внедрения углерода в Физические свойства феррита близки к свойствам железа. Он мягок (твердость – 130 НВ, предел прочности 300 МПа) и пластичен (относительное удлинение 30 %). Аустенит (А) – твердый раствор внедрения углерода в Аустенит имеет переменную растворимость углерода: минимальную – 0,8 % при температуре 727 оС, максимальную – 2,14 % при температуре 1147 оС. Твердость аустенита равна 200…250 НВ, относительное удлинение – 40…50 %. Аустенит парамагнитен. При растворении в аустените других элементов могут меняться его свойства и температурные границы существования. Цементит (Ц) – химическое соединение железа с углеродом, карбид железа (Fe3C), содержит 6,67 % углерода. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. Температура плавления цементита точно не установлена (1250…1550 оС). При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре 217 оС. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую пластичность. Такие свойства у него проявляются по причине сложного строения кристаллической решетки. Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: азотом, кислородом; атомы железа – металлами: марганцем, хромом, ванадием и др. Такой раствор на базе решетки цементита называется легированным цементитом. Карбид железа является химически неустойчивым компонентом и легко распадается с образованием свободного углерода в виде графита. Перлит (П) – эвтектоидная механическая смесь феррита и цементита. Образуется в результате распада аустенита при его охлаждении. Перлит может быть пластинчатым или зернистым. Это определяет его механические свойства. Ледебурит (Л) – эвтектика аустенита и цементита. Является твердым и хрупким металлом. При температуре ниже 727 оС состоит из цементита и перлита.
2.6 Процессы при структурообразовании железоуглеродистых сплавов
Линия АСD – ликвидус системы. На участке AC начинается кристаллизация аустенита, на участке СD – кристаллизация цементита первичного. Линия AECF – линия солидус. При температуре ниже 727o С в состав ледебурита входят цементит первичный и перлит, его называют ледебурит превращенный (ЛП). По линии GS превращение аустенита в феррит, обусловленное полиморфным превращением железа. По линии PG превращение аустенита в феррит заканчивается. По линии E S начинается выделение цементита вторичного из аустенита, обусловленное снижением растворимости углерода в аустените при понижении температуры. По линии МО при постоянной температуре 768o С имеют место магнитные превращения. По линии PSK при постоянной температуре 727o С идет эвтектоидное превращение, заключающееся в том, что аустенит, содержащий 0,8 % углерода, превращается в эвтектоидную смесь феррита и цементита вторичного:
По механизму данное превращение похоже на эвтектическое, но протекает в твердом состоянии. Перлит может существовать в зернистой и пластинчатой форме, в зависимости от условий образования. По линии PQ начинается выделение цементита третичного из феррита, обусловленное снижением растворимости углерода в феррите при понижении температуры. Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А (от французского arret – остановка): А1 – линия PSK (727 o С) – превращение П A2 – линия MO (768o С, точка Кюри) – магнитные превращения; A3 – линия GOS (переменная температура, зависящая от содержания углерода в сплаве) – превращение Ф Acm – линия SE (переменная температура, зависящая от содержания углерода в сплаве) – начало выделения цементита вторичного (иногда обозначается A3). Так как при нагреве и охлаждении превращения совершаются при различных температурах, чтобы отличить эти процессы вводятся дополнительные обозначения. При нагреве добавляют букву с, т.е
|
|||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 828; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.113 (0.01 с.) |

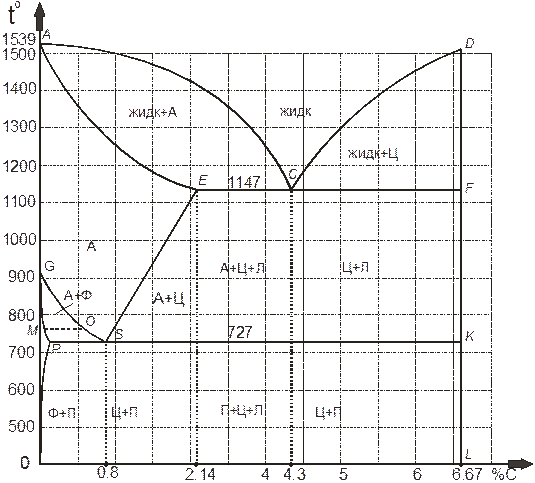 Рисунок 2.6 – Диаграмма состояния железо-углерод
Рисунок 2.6 – Диаграмма состояния железо-углерод
 модификация железа с объемно-центрированной кубической решеткой. В интервале температур 911…1392 оС устойчивой является
модификация железа с объемно-центрированной кубической решеткой. В интервале температур 911…1392 оС устойчивой является  модификация железа с гранецентрированной кубической решеткой. Выше 1392оС железо имеет объемно-центрированную кубическую решетку и называется
модификация железа с гранецентрированной кубической решеткой. Выше 1392оС железо имеет объемно-центрированную кубическую решетку и называется 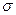 или высокотемпературное
или высокотемпературное 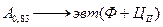
 А;
А; , при охлаждении – букву r, т.е.
, при охлаждении – букву r, т.е. 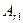 .
.


