
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Фаза, фазовые состояния веществаСодержание книги Похожие статьи вашей тематики
Поиск на нашем сайте
Фаза, фазовые состояния вещества Фаза ‑ однородн часть системы, отделенная от др частей замкнутыми поверхностями. Осн особенностью фазы явл-ся наличие поверхности раздела. Фазой наз-ют однородн части системы, имеющие одинаковый состав, стр-е и св-ва, одинаковое агрегатн сост-е и отделенн от др составн частей поверхностями раздела. Фаза может состоять из одного вещества, н-р, вода-жидкость или вода – лед, или из нескольких веществ, например, водный раствор сахара, спиртовой раствор бензола. Число веществ, входящих в состав фазы наз- ют числом компонентов, причем число компонентов – это наименьшее число веществ, с помощью которых можно выразить состав любой фазы. В каждой фазе любой компонент содержится в определенной концентрации, которую обычно выражают в молярных долях. Сумма молярных долей всех компонентов в данной фазе равна единице. Например, если в фазе имеется k компонентов, то справедливо соотношение: N1 + N2 + N3 + … + Nk = 1, где N1, N2, N3 … Nk – молярная доля соответственно 1-го, 2-го, 3-го и k-го компонента фазы. В зависимости от внешних условий (температуры, давления), почти каждое вещество может находиться в одном из агрегатных (фазовых) состояний: твердом, жидком, газообразном и плазменном, которые отличаются друг от друга характером движения частиц и свойствами. Для всякого вещества существуют такие значения температуры, давления, объема и плотности, которые называются критическими (в совокупности критическими параметрами вещества), а состояние, соответствующее критическим параметрам называется критическим состоянием или критической точкой вещества. По современным представлениям критическая точка является изолированной точкой фазового перехода второго рода и одновременно конечной точкой перехода первого рода жидкость – пар. Критическая точка характеризуется рядом физических явлений (например, бесконечная сжимаемость, бесконечная теплоемкость при постоянном объеме и т.д.), которые протекают идентично во всех веществах и определяются самыми общими свойствами межмолекулярных сил.
Жидкое состояние веществ В жидком состоянии расстояние между частицами значительно меньше, чем в газах, поэтому между ними возникают вандерваальсовы взаимодействия: дисперсионные, диполь-дипольные, индукционные. Эти взаимодействия удерживают молекулы друг около друга и приводят к некоторому их упорядочению или объединению частиц. Жидкое состояние характеризуется меньшим свободным пробегом молекул от одного межмолекулярного столкновения до другого, поэтому молекулы теряют способность перемещаться независимо и не удаляются значительно друг от друга. Жидкое вещество легко меняет свою форму, но незначительно изменяет объем. Если объем одного моль идеального газа при одинаковых условиях – величина постоянная, то для жидкостей объем различен и зависит от массы моль и плотности. Объем моль жидкости равен V = M/r, где М - молярная масса молекул жидкости, г/моль; r - плотность жидкости, г/см3. Жидкость в отличие от газов обладает значительно большей плотностью и силами притяжения между молекулами, а также почти постоянным объемом. Сжимаемость жидкости незначительна, что связано с наличием большого внутреннего давления. С ним связано значительное поглощение теплоты при испарении. Коэффициенты объемного расширения жидкостей значительно меньше, чем коэффициенты объемного расширения газов. Вещество находится в твердом состоянии, но структура его приближена к структуре жидкости. Такое состояние называется аморфным, например, стекло, некоторые смолы. Частицы в аморфном теле расположены беспорядочно, возможен лишь некоторый порядок в непосредственной близости от данной частицы. Однако в отличие от жидкостей, частицы в аморфных телах не обмениваются местами. Жидкости обладают поверхностью раздела, и, следовательно, поверхностной энергией. Из физических свойств жидкостей большое значение имеют поверхностное натяжение, вязкость и давление (упругость) насыщенного пара. Поверхностный слой жидкости обладает несколько иными свойствами, чем ее внутренний объем. Молекулы внутренних слоев равномерно окружены со всех сторон такими же молекулами, и силы их взаимного притяжения уравновешиваются. Молекулы поверхностного слоя оказываются под действием сил притяжения преимущественно со стороны жидкости, вследствие чего они как бы втягиваются во внутрь жидкости. Результирующая сила взаимодействия поверхностных молекул направлена в глубь жидкости и под действием этой силы жидкость стремится к сокращению площади поверхности при неизменном объеме. Этим объясняется сферическая форма капель. При любой температуре в замкнутом объеме над поверхностью жидкости устанавливается равновесие между скоростью испарения жидкости и скоростью конденсации пара в жидкость. Давление насыщенного пара зависит от температуры. Если давление насыщенного пара равно внешнему давлению и пар по мере испарения удаляется (давление не растет), то испарение протекает не только с поверхности, но и внутри жидкости, путем образования пузырьков пара во всем объеме. В этом случае происходит кипение и температура, при которой это происходит, называют температурой (точкой) кипения. Таким образом, если испарение с поверхности жидкости происходит при любой температуре, то кипение происходит только при определенной температуре, когда давление насыщенного пара становится равным внешнему давлению. Если уменьшать температуру, то давление насыщенного пара будет также уменьшаться. При температуре, когда давление пара над жидкостью станет равным давлению пара над поверхностью твердого тела, происходит замерзание жидкости и такую температуру называют температурой замерзания. Плазменное состояние веществ Плазменное состояние вещества образуется при очень высоких температурах (104 К и выше). При таких условиях в веществе происходит диссоциация молекул с образованием положительно заряженных ионов и свободных электронов, т.е. происходит частичное или полное разрушение электронных оболочек атомов. Плазму можно характеризовать как особое состояние вещества, обладающее высокой электропроводностью и другими специфическими свойствами. В плазменном состоянии движение частиц вещества является наиболее хаотичным. Поскольку плазма образуется при весьма высоких температурах, при которых вещество превращается в смесь ионов и электронов, вещество в плазменном состоянии находится во многих космических телах, в которых поддерживаются высокие температуры при термоядерном синтезе и т.д. Плазма может быть получена в искусственных условиях под воздействием высоких энергий в аппаратах, называемых плазмотронами. Существует также понятие низкотемпературной слабоионизированной плазмы (содержащей ионы, электроны и нейтральные атомы), которая образуется при дуговом или тлеющем разряде при электронной или ионной бомбардировке молекул газов в вакууме и т.д. Характерной особенностью плазмы является высокий энергетический уровень ее частиц, что позволяет проводить в плазме химические реакции, требующие подвода высоких энергий. Плазма подчиняется газовым законам, но основное отличие ее от обычных газов проявляется при воздействии электрических и магнитных полей. Вторая особенность плазмы состоит в том, что несмотря на общую электронейтральность, она часто оказывается неоднородной по отношению к внутреннему распределению зарядов и в ней легко возникают колебательные движения зарядов, в результате чего плазма становится источником электромагнитных колебаний.
Твердре состояние веществ Твердым называют вещество, имеющее определенную и неизменную форму и оказывающее сопротивление любому внешнему воздействию, направленному на изменение этой формы. У таких веществ степень хаотизации структурных единиц минимальна. Все твердые вещества можно разделить на кристаллические, форма которых обусловлена их внутренним строением, и аморфные или квазитвердые, которые можно рассматривать как жидкости с бесконечно большой вязкостью. Свойства кристаллических и аморфных твердых веществ также различны. Твердые кристаллические вещества характеризуются определенным дальним порядком расположения атомов, молекул, ионов, что приводит к образованию кристаллических решеток, т.е. трехмерных периодичных структур по всему объему твердого тела. Для них характерна анизотропия свойств – некоторые свойства по различным направлениям неодинаковы. Например, для кристаллических веществ наблюдается анизотропия механических, теплофизических, электрофизических, оптических и др. свойств. Кроме того, кристаллы имеют обычно геометрическую форму, ограниченную определенными кристаллическими плоскостями. Кристаллические вещества также имеют определенную температуру плавления. В отличие от них аморфные вещества такой температуры не имеют, которые при нагревании в определенном диапазоне температур постепенно размягчаются, пока не перейдут в жидкое состояние. Поэтому аморфные вещества принято рассматривать как переохлажденные жидкости, находящиеся в неустойчивом состоянии. Термодинамически большинство веществ стремится перейти из аморфного состояния в кристаллическое. Однако такой переход при умеренных температурах практически не возможен или протекает крайне медленно вследствие большой вязкости твердых тел. Для аморфных веществ характерна изотропия – т.е. все их свойства в различных направлениях одинаковы. Большинство аморфных веществ можно получить в кристаллической форме, и наоборот кристаллические – в аморфной форме. Поэтому будет правильным говорить не о кристаллических и аморфных веществах, а о кристаллическом и аморфном состоянии веществ. Поскольку подавляющее большинство твердых тел находится в кристаллическом состоянии, дальше мы будем рассматривать именно это состояние. Для некоторых веществ не все три агрегатных состояния возможны. Например, CaCO3 практически невозможно получить в жидком или газообразном состоянии, поскольку при нагревании это вещество разлагается с образованием CaO и СО2. Для некоторых веществ существуют условия, при которых они могут находиться одновременно в 2-х или трех состояниях. Например вода при 0,0098°С и давлении 4,579 мм.рт.ст. (518,9 Па) находится в устойчивом равновесии в трех состояниях ‑ льда, жидкости и пара.
Полиморфизм и аллотропия В зависимости от внешних условий одно и то же вещество может иметь различные типы кристаллических решеток. Способность вещества образовывать два и более типа кристаллических решеток называют полиморфизмом. Полиморфизм является наиболее частым проявлением аллотропии химических элементов.Аллотропией называют способность одного и того же элемента образовывать несколько различных типов простых веществ. Явление аллотропии может быть обусловлено либо различным составом молекулы простого вещества данного элемента (аллотропия состава), либо способом размещения атомов в кристаллах (аллотропия формы). Примером аллотропии состава являются кислород и озон. Характерным примером аллотропии формы (полиморфизма) являются три формы углерода: алмаз, графит и карбин. Карбин имеет цепную структуру, графит-гексагональную, алмаз – кубическую решетку. Существует четвертая искусственная форма углерода – фуллерен, представляющая собой полиэдрические кластеры, т.е. сферы состоящие из 60-70 атомов углерода, образуемых либо 5-гранниками,либо 6-гранниками, в вершинах которых находятся атомы.
13. Индексы кристаллогр. Плоскостей и направлений кристал.решеток Т.к. атомы кристалла образуют трехмерную пространственную решетку они могут быть отнесены к огромному числу атомарных плоскостей, формирующих определенную сис-му вдоль определенных направлений. Каждая такая сис-ма характ-ся строго определенными межплоскостными расстояниями. Для определения положения этих плоскостей в кристаллах используют индексы Миллера. Они представляют собой 3 целых рациональных числа, являющиеся величинами обратными отрезкам осей, отсекаемых данной плоскостью на осях координат. Единицы длины выбирают равными длине ребер элементарной ячейки. Эти числа заключают в круглые скобки. Например, в случае кубической ячейки, каждая плоскость куба пересекает только одну ось, при этом отсекаемые отрезки будут равны (1, ¥, ¥), (¥, 1, ¥) и (¥, ¥, 1). Обратные величины отсекаемых отрезков будут соответственно равны (1, 0, 0), (0, 1, 0) и (0, 0, 1), а индексы соответствующих плоскостей будут (100), (010) и (001). В кубической системе имеется также плоскость октаэдра (111) и плоскость додекаэдра (110) (рисунок (а – в)). Если индексы характеризуют не одну какую-либо плоскость, а целую группу параллельных плоскостей, тогда их заключают в фигурные скобки {h, k, l}. Помимо плоскостей с помощью инд. Миллера обозначают кристаллографическое направление. Обозначаются они аналогично плоскостям. Некоторые направления для кубической решетки приведены на рисунке 1.12 (г). Для кубической решетки индексы направлений, перпендикулярных к плоскости, численно равны индексам этой плоскости, например, индексы оси х равны [100], а индексы плоскости, перпендикулярной к оси х, равны (100).
Ударные исп-я материалов. Исп-я образцов матер-в сопротивлению удару проводят на машинах, наз копрами, к-рые по своему принципу действия делятся на вертикальные, маятниковые и ротационные. При исп-х на вертик-х копрах опред-ся сопротивление образца повторным ударам «бабы» опред-ой массы падающей с заданной высоты. Исп-я продолжают до разрушения и опред-т число требуемых для этого ударов. Также может опред-ся величина работы деформации (А), затраченной на разрушение.
Усталостные исп-я матер-ов Во время усталостных исп-й на образец дейст-т циклические напряж-я, в основном, подчиняющиеся синусоидальному закону. Наиболее распростр-ая схема нагружения при усталостных исп-ях – изгиб при вращении образца. Нагрузку приклад-т в 2 точках, что обеспеч-т постоянство изгибающего момента по всей длине образца. Помимо схемы чистого изгиба часто применяют круговой изгиб консольно закрепленного образца. В этом случае max изгибающий момент достигается только вблизи основания консоли. Хаар-ки выносливости зависят от размера образца. Рез-ты усталостных исп-й очень чувств-ны к состоянию поверх-ого слоя образца. Первичным рез-том усталостного исп-я единичного образца яв-ся число циклов нагружения до разрушения при заданных хар-ах цикла. Для исп-й необходимо провести целую серию опытов и в рез-те можно опред-ть предел выносливости – наибольшее знач max напряжения цикла, при действии к-рого не происходит усталостного разрушения образца после заданного числа циклов нагружения. По рез-там исп-й строят кривую усталости, в координатах: max напряжение цикла (smax) – долговечность (N - число циклов нагружения до момента разрушения образца). По мере уменьшения max напряжения цикла долговечность материалов возрастает. Для каждого образца опред-т усталостную долговечность – число циклов нагружения, к-рое выдерживает материал перед разрушением при опред-ом напряжении. Вязкость материалов. Вязкостью, или внутренним трением жид-ей (матер-в в жидком сост-и), наз сопротивление, исп-ое матер-ом при движении одних его частей относительно др. В случае ламинарного движения жид-ти все ее слои движутся параллельно др др со скоростями, возрастающими от слоя к слою. Между слоями, движущимися с различными скоростями, возникает сила (F), стремящаяся выровнять эти скорости. Эта сила (сила трения) прямо пропорциональна поверхности сопротивления (S) и градиенту скорости (Dv/х) Теплоемкость материалов Теплоемкостью наз кол-во теплоты, необходимое для нагревания 1 массы в-ва на 1 градус. Если в систему ввести бесконечно малое кол-во теплоты dQ и ее тем-ра повысится на величину dT, то теплоемкость системы выражается в виде
Термостойкость. При стационарном и нестационарном нагреве неоднородность тем-ого поля в образце или изделии вызвает мех напряжения, к-рые могут привести к деформации или разрушению образца. Устойчивость объекта к неоднородному тем-рному полю зависит преимущественно от термостойкости, степени неоднородности тем-рного поля, размеров и формы объекта. Термостойкостью наз способность материала в виде образцов опред-ой формы и размеров выдерживать без разрушения действие нек-рой разности тем-р в опред-ых усл-ях. Основные пара-ры, определяющие термостойкость материала, связаны след урав-ями: ‑ при стационарном режиме нагрева Ф; ‑ при нестационарном режиме нагрева Ф, где DТ – разрушающая разность тем-р;s - предел прочности;a - тем-рный коэф-т линейного расширения;Е – модуль упругости;c - коэф-т теплопроводности;К– коэф-т температуропроводности;с1 и с2 – поправочные коэф-ты;n – показатель степени, к-рый изменяется от 0,5 до 1. Больше всего термостойкость зависит от тем-рного коэф-та линейного расширения, а также от микростр-ры и строения материала. К материалам с высокой термостойкостью относятся такие, у к-рых a < 45×10-7 град.-1, а материалы, имеющие a > 80×10-7 град.-1, хар-ся низкой термостойкостью. В зависимости от природы материалов, их термостойкость определяют различными методами. Например, термостойкость стекол (нагревают и сбрасывают в воду, фиксируют трещины и разрушения).
Основные понятия в области коррозии материалов. Одним из осн-х св-в матер-в явл. устойчивость к коррозии. Слово «коррозия» озн. разъедать. Коррозия – это самопроизвольное разрушение матер-в вследствие хим. или электрохим взаимодействия их с окружающей средой. Разрушение известно как эрозия, истирания или взнос. В нек-рых случаях хим. или электрохим. Воздействия сопровождаются физ. разрушением и наз коррозионной эрозией, коррозионным износом или фреттинг-коррозией. Коррозию железа и его сплавов наз. ржавлением. Др материалы (напр., цветные мет.), следовательно, не ржавеют, но корродируют. Среда, в кот. происходит разрушение матер-в наз коррозионной или агрессивной, а образ в рез-те коррозии соединения – продуктами коррозии.Способность матер-в сопротивляться коррозионному воздействию среды наз Коррозионной стойкостью. Коррозия материалов происх-т на границе раздела фаз, т.е. на границе соприкосновения тв в-ва с газом или жид-тью. Причина коррозии – термодинамическая неустойчивость матер-в в окружающей среде. Возможность протекания любого процесса, включая взаимод-е материала с компонентами окруж. среды, опред. изменением свободной энергии Гиббса (дельта G).Чем выше отрицательное значение дельта G, тем больше термодинамическая возможность реакции.
Электрохимическая защита Электрохим. защита состоит в катодной или анодной поляризации защищаемой метал-ой конструкции. Она основан на том, что, сдвигая потенциал МЕ пропусканием тока, можно изменять скорость его коррозии. Электрохим. защита осущ-ся присоед-ем конструкции к внеш. источнику постоянного тока или к постороннему электроду – протектору. Катодная защита- применяется для предохранения от коррозии метал-их изделий находящихся в почве, морской воде (хранилища нефти и жидкого топлива, трубопроводы, сварные метал-ие основания, а также аппаратуру хим заводов и предприятий (реакторы, холодильники, конденсаторы, теплообменники и др.)). Она осущ-ся присоед-ем защищаемого оборудования и конструкций к отрицатель. полюсу внеш. источника постоянного тока. Увеличение внеш. тока до величины, обеспеч-щей достижение равновесного потенциала корродирующего МЕ, полностью подавляет коррозионный процесс. Вследствие этого вся поверхность металлического оборудования или конструкции становиться катодом и тем самым предохраняет МЕ от разрушения. Протекторная защита или гальваническая катодная защита- в этом случае катодная поляризация металлоизделия осущ-ся за счет его контакта с МЕ, имеющим более электроотрицательное знач окислительно-восстановительного потенциала. Протектор при этом яв-ся анодом. Его электрохим. растворение обеспечивает протекание катодного тока через защищаемое метал.изделие. Сам же анод (обычно это магний, цинк, алюминий и их сплавы) постепенно растворяется. Этот вид защиты применяют для небольших конструкций. Эффективность катодной и протекторной защиты возрастает, если их применять совместно с защитными покрытиями. Анодная защита применяется для снижения скорости коррозии аппаратов, изготовленных из нержавеющих и углеродистых сталей, никеля, титана и др способных легко пассивироваться при работе в агрессивных средах. Анодная защита применяется только в тех случаях, когда катодная или протекторная защита требует значительных энергетических затрат. Анодная защита осущ-ся присоединением защищаемого изделия к положительн. полюсу внеш. источника постоянного тока или к металлу с более положительным потенциалом (катодный протектор). Скорость коррозии при анодной защите мб снижена до min величины, соответствующей току полной пассивации, но никогда не уменьшается до нуля, как в случае катодной защиты.. Электродренаж. Блуждающие токи возникают вследствие утечки из электр-х цепей части тока в почву или водные р-ры, где они попадают на метал-е конструкции. В местах выхода этого тока из этих конструкций вновь в агрессивную среду происходит анодное растворение металла.(это наблюдается в места трамвайных путей).
Медь и сплавы на ее основе. Медь – розовато-красный металл, тяжелый, эластичный. Медь хорошо противостоит коррозии на воздухе, но во влажной среде и в атмосфере, загрязненной промышленными выбросами, быстро тускнеет, покрывается зеленым налетом с образованием токсичных соединений меди. В зависимости от чистоты медь изготавливают следующих марок – М00 (99,99% Cu), М0 (99,97% Cu), М1 (99,9% Cu), М2 (99,7% Cu), М3 (99,5% Cu). В зависимости от способа получения различают следующие марки меди - катодная(М00к), бескислородная (М0б), катодная переплавленная(М1у), раскисленная(М1р); огневого рафинирования(М2, МЗ). При этом М обозначает медь, В -высокочистая, Б - бескислородная; цифры - степень чистоты. Медь легко обрабатывается давлением, но плохо резанием, и имеет невысокие литейные свойства из-за большой усадки. Медь плохо сваривается, но легко подвергается пайке. Чистую медь применяют для электротехнических целей в виде проволоки, листов, лент, труб. Из-за малой механической прочности чистую медь не используют как конструкционный материал, а применяются ее сплавы с цинком, оловом, алюминием, кремнием, марганцем, свинцом. Различают две основные группы медных сплавов – латуни и бронзы. В марках сплавов на основе меди буквы обозначают: Л - латунь; Бр – бронза. Латуни – двойные и многокомпонентные сплавы на основе меди, в которых основным легирующим компонентом является цинк. Латуни обладают высокой прочностью, коррозионной стойкостью и лучшей обрабатываемостью, чем медь. Технические латуни содержат 40-45% цинка. Латуни нередко легируют Al, Fe, Ni, Mn, Pb и другими элементами. Такие латуни называют многокомпонентными или специальными. Легирующие элементы увеличивают прочность (твердость), но снижают пластичность латуни. Например, свинец облегчает обрабатываемость резанием и улучшает антифрикционные свойства, а примеси Al, Si, Mn и Ni повышают стойкость к коррозии. Латуни обозначают буквой Л, затем следуют первые буквы компонентов, образующих сплав. Цифры, следующие за буквами, указывают на количество легирующих компонентов в процентах. Например, ЛАЖМнЦ 66 – 6 – 3 – 2 – латунь, содержащая 66% меди, 6% алюминия, 3% железа, 2% марганца, а остальное цинк. Латуни применяют для изготовления листов, труб, лент, проволоки, деталей часовых механизмов и др. Простая латунь Л90 (томпак, 90% меди и 10% цинка) имеет красивый внешний вид и применяется для изготовления украшений.
Стекло и его св-ва. Стекло - это твердый прозрачный аморфный материал, получаемый с помощью охлаждения стеклообразных расплавов различного химического состава. Основу стекла составляют неорганические оксиды. Основным сырьем для производства стекла является сода, известняк, песок. Физико-химические свойства стекол: Плотность, она зависит от наличия в составе стекла оксидов тяжелых металлов и влияет на массу изделий, а также на оптические и термические свойства. Механические свойства стекла характеризуются отсутствием пластических деформаций, высокой прочностью при сжатии и низкой при растяжении и изгибе и особенно при ударе.Теплофизические свойства стекла характеризуются низкой теплопроводностью, значительной теплоемкостью и небольшим термическим расширением. Звукоизолирующая способность стекла достаточно высока.Оптические свойства стекол достаточно разнообразны. Стекла могут быть прозрачными и заглушенными, бесцветными и окрашенными, с блестящей и матовой поверхностью.Химическая устойчивость стекла весьма высока, особенно по отношению к воде, органическим и неорганическим. По водостойкости стекло делят на пять гидролитических классов: первый класс – неизменяемые водой стекла; пятый – неудовлетворительные.По химическому составу стекла делят на натрий-кальций-силикатное (обычное); кварцевое; боросиликатное; хрустальное и др.По свойствам стекла делят на специальные разновидности: огнестойкое термостойкое; нейтральное; электровакуумное; полупроводниковое; лазерное; оптическое; армированное; ламинированное; эмалированное и др.
Ситаллы Ситаллы представляют собой стеклокристаллические (микрокристаллические) материалы, получаемые путем направленной (каталитической) кристаллизации стекол специальных составов, протекающей в объеме заранее отформованного изделия. Ситаллы состоят из одной или нескольких кристаллических фаз, равномерно распределенных в стекловидной фазе. Главной особенностью ситаллов является тонкозернистая равномерная стеклокристаллическая структура, обуславливающая сочетание высокой твердости и механической прочности с отличными электроизоляционными свойствами, высокой температурой размягчения, хорошей термической и химической стойкостью. Для ситаллов решающую роль имеют структура и фазовый состав. Причина ценных свойств ситаллов заключается в их исключительной мелкозернистости, почти идеальной поликристаллической структуре. Свойства ситаллов изотропны. В ситаллах отсутствует пористость, усадка материала при его переработке незначительна, а большая абразивная стойкость делает их малочувствительными к поверхностным дефектам Твердость ситаллов близка к твердости закаленной стали, по теплопроводности ситаллы превосходят стекла. Термостойкость ситаллов достаточно высока. Ситаллы весьма износостойки, обладают высокой химической устойчивостью к кислотам и щелочам, не окисляются даже при высоких температурах, газонепроницаемы, обладают нулевым водопоглощением, хорошие диэлектрики. Ситаллы получают путем плавления стекольной шихты специального состава с добавкой нуклеаторов (катализаторов), охлаждения расплава до пластичного состояния и формования из него изделий методами стекольной технологии и последующей ситаллизации (кристаллизации). Ситалловые изделия получают также порошковым методом спекания. Ситаллы подразделяют на фотоситаллы, термоситаллы и шлакоситаллы. Ситаллы используются в промышленности в качестве облицовочного материала, элементов слоистых панелей в конструкциях зданий. Из ситаллов изготавливают жаропрочную хозяйственную посуду – кастрюли, жаровни, сотейники. Из ситаллов изготавливают подшипники, детали для двигателей внутреннего сгорания. Их применяют при производстве текстильных машин, абразивов для шлифования, фильер для вытягивания синтетических волокон. Большое распространение получили стеклокристаллические покрытия, наносимые на поверхность металлов для защиты от коррозии, окисления и износа при обычных и повышенных температурах. На предприятиях химической промышленности используют ситалловые трубы. В электронной промышленности ситаллы используют в качестве диэлектрической изоляции микросхем и межслойной изоляции печатных схем на керамических и других подложках. Стеклокерамические корпуса используются для герметизации полупроводниковых приборов и интегральных схем.
Пластмассы Пластмассами называются искусственные твердые материалы, получаемые на основе органических полимерных связующих веществ. Эти материалы способны при нагреве размягчаться, становиться пластичными, и им можно придать заданную форму, которая в последствии сохраняется. В зависимости от природы связующего переход отформованной массы в твердое состояние совершается или при дальнейшем нагреве, или при последующем охлаждении. Характерные свойства пластмасс - высокая механическая прочность, устойчивость к действию агрессивных сред, красивый внешний вид, возможность изготовления изделий в законченной форме, тепло-, звуко- и электроизоляция. Обязательным компонентом пластмасс является связующие вещества, в качестве которых используют синтетические смолы, реже применяют эфиры целлюлозы. Другим важным компонентом пластмасс является наполнитель (порошкообразные, волокнистые и другие вещества как органического, так и неорганического происхождения). Наполнители повышают механические свойства, снижают усадку при прессовании и придают материалу те или иные специфические свойства. Свойства пластмасс зависят от состава отдельных компонентов, их сочетания и количественного соотношения, что позволяет изменять их характеристики в достаточно широких пределах. По характеру связующего пластмассы подразделяют на термопластичные (термопласты), получаемые на основе термопластичных полимеров, и термореактивные (реактопласты), получаемые на основе термореактивных смол. По виду наполнителя пластмассы делят на порошковые (карболиты с наполнителями в виде древесной муки, графита, талька и др.; волокнистые с наполнителями в виде очесов хлопки и льна (волокниты), стеклянного волокна (стекловолокниты), асбеста (асбоволокниты); слоистые, содержащие листовые наполнители (листы бумаги в гетинаксе, хлопчатобумажные, стекланные, асбестовые ткани в текстолите, древесный шпон в древеснослоистых пластиках; газонаполненные – воздух или нейтральные газы (пено- и поропласты). По применению пластмассы можно подразделить на силовые (конструкционные, фрикционные, антифрикционные, электроизоляционные) и несиловые (оптически прозрачные, химически стойкие, электроизоляционные, теплоизоляционные, декоративные, уплотнительные, вспомогательные). Особенностями пластмасс являются малая плотность, низкая теплопроводность, значительное тепловое расширение, хорошие электроизоляционные свойства, высокая химическая стойкость, фрикционные и антифрикционные свойства. Недостатками пластмасс являются невысокая теплостойкость, низкие модуль упругости и ударная вязкость, а для некоторых видов пластмасс - склонность к старению. Термопластичные пластмассы. В основе термопластичных пластмасс лежат полимеры линейной или разветвленной структуры. Термопласты делят на полярные и неполярные. К неполярным пластмасса относят полиэтилен, полипропилен, полистирол и фторопласт-4. К полярным термопластам относят фторопласт-3, органические стекло, поливинилхлорид, полиамиды, полиуретаны, полиэтилентерефталат, поликарбонат, полиарилаты, пентапласт, полиформальдегид. На основе термопластичных полимеров изготавливают термостойкие пластики: ароматический полиамид (фенилон), арилокс-полифениленоксид, полисульфон, полибензимидазы и полиимиды, которые сохраняют устойчивость при достаточно высоких температурах (до 600°С и выше). Из них изготавливают пленки, волокна, ткани, бумагу (номекс), детали автомобилей, станков, бытовых машин, хирургические инструменты, изоляцию на высокочастотных установках, матрицы для типографских клише и др. Термор
|
||||
|
Последнее изменение этой страницы: 2016-08-12; просмотров: 1641; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.112.208 (0.013 с.) |

 G – масса «бабы»; q ускорение своб-го падения, v0 и v скорость падения “бабы» до и после удара. В случае исп-й на ротационном копре закрепленный образец ломается ударом ножа, закреп-ого на периферии стального диска вращающегося с опред-ой скоростью, а энергию, затраченную на излом, опред-т по изменению скорости или ускорения диска. Мех-ие св-ва матер-в склонных к хрупкому разрушению опред-т на маятниковых копрах. Исп-я осущ-т одним ударом тяжелого молота, разрушающего образец. У металлов или пластмасс делают надрез, чтобы затруднить пластическую деформацию, у хрупких матер-ов надрез не нужен. Работа, затраченная на излом
G – масса «бабы»; q ускорение своб-го падения, v0 и v скорость падения “бабы» до и после удара. В случае исп-й на ротационном копре закрепленный образец ломается ударом ножа, закреп-ого на периферии стального диска вращающегося с опред-ой скоростью, а энергию, затраченную на излом, опред-т по изменению скорости или ускорения диска. Мех-ие св-ва матер-в склонных к хрупкому разрушению опред-т на маятниковых копрах. Исп-я осущ-т одним ударом тяжелого молота, разрушающего образец. У металлов или пластмасс делают надрез, чтобы затруднить пластическую деформацию, у хрупких матер-ов надрез не нужен. Работа, затраченная на излом 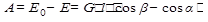 Исходный запас энергии (Е0) и остаток энергии (Е) маятника, G – масса маятника, l – длина маятника. В конечном итоге опред-т ударную вязкость образца
Исходный запас энергии (Е0) и остаток энергии (Е) маятника, G – масса маятника, l – длина маятника. В конечном итоге опред-т ударную вязкость образца  ;S – площадь поперечного сечения образца в месте надреза.
;S – площадь поперечного сечения образца в месте надреза.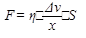 , где h - коэф-т внутр трения, коэф-т вязкости или динамическая вязкость. Вязкость жид-ей опред-т по скорости их истечения через сопло опред-ого диаметра. Для тв тел измеряют эффективную вязкость (h), к-рую опред-т как меру сопротив-я в-ва относит-ому перемещению участков материала, т.е. меру сопротивления пластической деформации. Эффективная вязкость хар-т мех-ую жаростойкость материалов. Мех-ая жаростойкость - это эф-ая вязкость при повышенных тем-рах. Кол-ные методы опред-я эф-ой вязкости (h) тв тел основаны на измерении скорости изменения неупругой деформации (Dl) образцов. Скорость неупругой деформации измеряется при заданной постоянной тем-ре и заданном напряжении. Наиболее простой способ измерения эф-ой вязкости основан на деформации растяжения или сжатия образца.
, где h - коэф-т внутр трения, коэф-т вязкости или динамическая вязкость. Вязкость жид-ей опред-т по скорости их истечения через сопло опред-ого диаметра. Для тв тел измеряют эффективную вязкость (h), к-рую опред-т как меру сопротив-я в-ва относит-ому перемещению участков материала, т.е. меру сопротивления пластической деформации. Эффективная вязкость хар-т мех-ую жаростойкость материалов. Мех-ая жаростойкость - это эф-ая вязкость при повышенных тем-рах. Кол-ные методы опред-я эф-ой вязкости (h) тв тел основаны на измерении скорости изменения неупругой деформации (Dl) образцов. Скорость неупругой деформации измеряется при заданной постоянной тем-ре и заданном напряжении. Наиболее простой способ измерения эф-ой вязкости основан на деформации растяжения или сжатия образца.  ±F – знач растягивающей или сжимающей силы, l – длина образца, ±Dl – величина неупругой деформации, t - время, S – площадь поперечного сечения образца. Применяют также схемы, основанные на изгибе образца и на кручении образца. Тв материалы при высоких тем-рах подвергают исп-ям на ползучесть. Опр-т условный предел ползучести – величину наибольшего напряжения, при к-ром материал в усл-ях длительной нагрузки при заданной тем-ре за опр-ый промежуток времени обнаруживает заданное удлинение или заданную скорость ползучести.
±F – знач растягивающей или сжимающей силы, l – длина образца, ±Dl – величина неупругой деформации, t - время, S – площадь поперечного сечения образца. Применяют также схемы, основанные на изгибе образца и на кручении образца. Тв материалы при высоких тем-рах подвергают исп-ям на ползучесть. Опр-т условный предел ползучести – величину наибольшего напряжения, при к-ром материал в усл-ях длительной нагрузки при заданной тем-ре за опр-ый промежуток времени обнаруживает заданное удлинение или заданную скорость ползучести. Теплоемкость, отнесенную к массе (m), наз удельной теплоемкостью.
Теплоемкость, отнесенную к массе (m), наз удельной теплоемкостью.  В зависимости от усл нагревания или охлаждения в-ва различают теплоемкость при постоянном объеме QV и теплоемкость при постоянном давлении QP. Кол-во теплоты, переданное телу при постоянном объеме, равно приращению внутр энергии тела QV = U. Кол-во теплоты, переданное телу при постоянном давлении, равно приращению энтальпии тела QР = DН. Для опред-я удельной теплоемкости применяют, как правило, калориметрические методы с этой целью испытуемый образец массой m нагревают до температуры T2, затем его помещают в калориметр с жид-тью, после чего опред-т кол-во теплоты, переданное образцом жид-ти за время, пока тем-ра образца и жид-ти не сравняются (Т1)
В зависимости от усл нагревания или охлаждения в-ва различают теплоемкость при постоянном объеме QV и теплоемкость при постоянном давлении QP. Кол-во теплоты, переданное телу при постоянном объеме, равно приращению внутр энергии тела QV = U. Кол-во теплоты, переданное телу при постоянном давлении, равно приращению энтальпии тела QР = DН. Для опред-я удельной теплоемкости применяют, как правило, калориметрические методы с этой целью испытуемый образец массой m нагревают до температуры T2, затем его помещают в калориметр с жид-тью, после чего опред-т кол-во теплоты, переданное образцом жид-ти за время, пока тем-ра образца и жид-ти не сравняются (Т1)  e - поправка, учитывающая потери теплоты в окружающую среду, Удельную теплоемкость образца
e - поправка, учитывающая потери теплоты в окружающую среду, Удельную теплоемкость образца 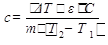 . Для металлов можно исп-ть метод импульсного нагрева. Образец кратковременно нагревают импульсом тока и опр-т приращение тем-ры.
. Для металлов можно исп-ть метод импульсного нагрева. Образец кратковременно нагревают импульсом тока и опр-т приращение тем-ры.


