
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Повышенный уровень сложности. 43. Установите соответствие между тривиальным названием органического вещества и его
43. Установите соответствие между тривиальным названием органического вещества и его формулой
44. Только в состоянии sp3-гибридизации атомы углерода находятся в молекулах
45. В состоянии sp3- и sp2-гибридизации атомы углерода находятся в молекулах
46. В реакцию полимеризации способны вступать
47. С аммиачным раствором оксида серебра взаимодействуют
48. С гидроксидом меди(II) взаимодействуют
49. Установите соответствие между схемой реакции и продуктом окисления органического вещества
50. Формальдегид взаимодействует с
51. Пропаналь взаимодействует с
52. Ацетальдегид взаимодействует с
53. И муравьиный, и прoпионовый альдегид могут взаимодействовать с
54. Для метаналя справедливы утверждения
55. Для ацетальдегида справедливы утверждения
56. И для пропаналя, и для пропанона справедливы утверждения
57. При взаимодействии уксусного альдегида с избытком аммиачного раствора оксида серебра выпал осадок массой 2,16 г. Масса уксусного альдегида, вступившего в реакцию, равна _________ г. (Запишите число с точностью до сотых.) 58. При взаимодействии уксусного альдегида массой 1,32 г с избытком аммиачного раствора оксида серебра выпал осадок, масса которого равна _________ г. (Запишите число с точностью до сотых.)
59. По реакции Кучерова с выходом 70% получили 61,6 г ацетальдегида. Объем (н.у.) ацетилена, вступившего в реакцию, равен _________ л. (Запишите число с точностью до десятых.)
60. Для восстановления пропаналя массой 29 г необходим водород, объем (н.у.) которого равен _________ л. (Запишите число с точностью до десятых.)
61. Масса этаналя, которая может полностью сгореть в кислороде объемом 5,6 л (н.у.), равна _________ г. (Запишите число с точностью до десятых.)
62. Объем углекислого газа (н.у.), который выделяется при полном сгорании пропаналя массой 5,8 г, равен _________ л. (Запишите число с точностью до сотых.)
63. Объем кислорода (н.у.), который необходим для полного сгорания пропаналя массой 2,9 г, равен _________ л. (Запишите число с точностью до сотых.)
64. Объем воздуха (н.у.), который необходим для полного сгорания метаналя массой 60 г, равен _________ л. (Запишите число с точностью до целых.)
65. В 150 г воды растворили 17,92 л (н.у.) метаналя. Массовая доля метаналя в полученном растворе равна _________ %. (Запишите число с точностью до десятых.)
66. Для получения формалина – 40%-ного водного раствора формальдегида – в 120 г воды надо растворить формальдегид, масса которого равна _________ л. (Запишите число с точностью до целых.)
Высокий уровень сложности
67. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Х1 → С2Н2
68. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: СН3СН2СН2СООNa → С3Н8 Укажите условия протекания реакций.
69. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Al4C3 Укажите условия протекания реакций.
70. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: C2H5Br Укажите условия протекания реакций.
71. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: бензол → метилбензол Укажите условия протекания первой реакции.
72. (С4) Бутаналь массой 28,8 г частично окислили в бутановую кислоту. Для нейтрализации полученной кислоты затратили 46,2 мл 24%-ного раствора гидроксида натрия (плотность 1,263 г/мл). Определите массу бутаналя, не подвергшегося окислению.
73. (С4) К 20 г водного раствора формальдегида добавили избыток аммиачного раствора оксида серебра и смесь слегка нагрели. Серебро, выделившееся в результате реакции, полностью растворили в концентрированной азотной кислоте, при этом выделилось 17,92 л (н.у.) газа. Определите массовую долю формальдегида в исходном растворе.
74. (С4) Смесь уксусного и пропионового альдегида массой 1,17 г полностью окислили до соответствующих кислот гидроксидом меди(II), который был получен в результате взаимодействия между 16%-ным раствором сульфата меди(II) массой 50 г и 10%-ным раствором гидроксида натрия массой 80 г. Определите массовые доли альдегидов в исходной смеси.
75. (С4) Уксусный альдегид массой 1,32 г обработали 5-%-ным раствором бихромата калия в сернокислотной среде массой 117,6 г. Определите массовую долю бихромата калия в растворе после окончания реакции.
76. (С5) Массовая доля углерода в предельном альдегиде равна 62,07%. Установите молекулярную формулу альдегида. 77. (С5) Массовая доля кислорода в предельном альдегиде равна 27,59%. Установите молекулярную формулу альдегида.
78. (С5) Установите молекулярную формулу предельного альдегида, массовая доля углерода в котором в 3,75 раза больше массовой доли кислорода.
79. (С5) Для окисления предельного альдегида массой 2,9 г до соответствующей кислоты потребовалось 9,8 г гидроксида меди(II). Определите молекулярную формулу альдегида.
80. (С5) При окислении 2,88 г предельного альдегида избытком аммиачного раствора оксида серебра выделилось 8,64 г серебра. Установите молекулярную формулу альдегида.
81. (С5) При полном сгорании 4,3 г предельного альдегида выделилось 4,5 г воды. Установите молекулярную формулу альдегида.
82. (С5) При сгорании органического вещества массой 6,6 г получили 6,72 л углекислого газа (н.у.) и 5,4 г воды. Плотность паров вещества по кислороду равна 1,375. Установите молекулярную формулу вещества. 83. (С5) При сгорании органического вещества массой 8,7 г получили 19,8 г углекислого газа (н.у.) и 8,1 г воды. Плотность паров вещества по азоту равна 2,071. Установите молекулярную формулу вещества.
84. При сгорании органического вещества массой 4,5 г получили 3,36 л углекислого газа (н.у.) и 2,7 г воды. Плотность паров вещества по метану равна 1,875. Установите молекулярную формулу вещества.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 1026; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.231.221 (0.024 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

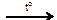
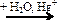 X2
X2  Х3
Х3  X2
X2 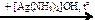 X4
X4 X1
X1 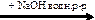 Х2
Х2  X3 → CO2
X3 → CO2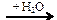 X1 → CH3Br → CH3OH → HCOH
X1 → CH3Br → CH3OH → HCOH 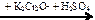 X2
X2 X1
X1 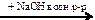 X3
X3 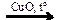 X4
X4 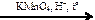 X5
X5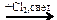 X1
X1 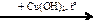 X4
X4


