
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Повышенный уровень сложности. 111. Установите соответствие между тривиальным названием спирта и его формулой
111. Установите соответствие между тривиальным названием спирта и его формулой
112. Для этанола справедливы утверждения
113. Глицерин взаимодействует с
114. Фенол взаимодействует с
115. Химические свойства фенола неправильно описывают уравнения реакций
116. И фенол, и этиленгликоль взаимодействуют с
117. И фенол, и глицерин взаимодействуют с
118. Для этиленгликоля справедливы утверждения
119. Для глицерина справедливы утверждения
120. Для фенола справедливы утверждения
121. Установите соответствие между названием органического вещества и цвет лакмуса в его водном растворе
122. При гидратации 44,8 л (н.у.) этилена с выходом 70% получили этанол, масса которого равна _________ г. (Запишите число с точностью до десятых.)
123. В результате гидратации пропилена с выходом 75% получили 300 г пропанола-2. Объем (н.у.) вступившего в реакцию пропилена равен _________ л. (Запишите число с точностью до целых.) 124. В результате межмолекулярной дегидратации 192 г метанола с выходом 60% получили простой эфир, масса которого составила _________ г. (Запишите число с точностью до десятых.) 125. При окислении 18, 4 г этанола оксидом меди(II) получили этаналь, масса которого составила _________ г. (Запишите число с точностью до десятых.)
126. Масса этанола, полученного в результате щелочного гидролиза 21,8 г бромэтана, равна _________ г. (Запишите число с точностью до десятых.) 127. Масса этиленгликоля, полученного в результате щелочного гидролиза 56,4 г 1,2-дибромэтана, равна _________ г. (Запишите число с точностью до десятых.) 128. Масса фенолята натрия, полученного при взаимодействии фенола массой 18,4 г с натрием массой 6,9 г, равна _________ г. (Запишите число с точностью до десятых.) 129. Объем (н.у.) водорода, который выделится при взаимодействии 73,6 г глицерина с избытком калия, равен _________ л. (Запишите число с точностью до сотых.) 130. При взаимодействии 0,94 г фенола с избытком бромной воды выпал осадок, масса которого равна _________ г. (Запишите число с точностью до сотых.) 131. При взаимодействии фенола с избытком бромной воды выпал осадок массой 13,24 г. Масса фенола, вступившего в реакцию, равна _________ г. (Запишите число с точностью до сотых.)
132. При полном сгорании 9,2 г этанола выделился углекислый газ, объем (н.у.) которого равен _________ г. (Запишите число с точностью до сотых.) 133. Для полного сгорания 12,8 г метанола необходим кислород, объем (н.у.) которого равен _________ л. (Запишите число с точностью до сотых.) 134. Для полного сгорания 23,5 г фенола необходим воздух, объем (н.у.) которого равен _________ л. (Запишите число с точностью до целых.) 135. Масса этиленгликоля, которая может полностью сгореть в кислороде объемом 11,2 л (н.у.), равна _________ г. (Запишите число с точностью до десятых.) 136. К 200 г 20%-ного раствора этанола добавили 150 г 30%-ного раствора того же вещества. Массовая доля этанола в полученном растворе равна _________ %. (Запишите число с точностью до десятых.) 137. Какой объем воды надо прилить к 300 г 20%-ного раствора этанола для получения 15%-ного раствора? Ответ: _________ мл. (Запишите число с точностью до целых.) Высокий уровень сложности
138. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: СО → СН3ОН → СН3Сl Укажите условия протекания реакций.
139. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Al4С3 Укажите условия протекания реакций.
140. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: X1 → C2H2 → C2H4 Укажите условия протекания реакций.
141. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: циклопропан → С3H8 Укажите условия протекания реакций.
142. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: бутан
143. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: C6H12O6 → C2H5OH Укажите условия протекания реакций.
144. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: С6H6 Укажите условия протекания реакций.
145. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: пропанол-1→ пропен Укажите условия протекания 1-й реакции.
146. (С4) В результате дегидратации 13,8 г этанола с выходом 80% получили этен. Определите массу 5%-ного раствора перманганата калия, которую может обесцветить полученный в результате дегидратации этен.
147. (С4) Cмесь этанола и этиленгликоля массой 21,6 г при взаимодействии с избытком натрия выделяет водород, который способен полностью гидрировать фенол массой 9,4 г. Определите массовые доли этанола и этиленгликоля в исходной смеси.
148. (С4) К раствору фенола в бензоле добавили избыток бромной воды. Масса выпавшего осадка составила 3,31 г. Такую же массу раствора полностью сожгли. Минимальный объем 20%-ного раствора гидроксида натрия (плотность 1,22 г/мл), который необходим для поглощения образовавшегося углекислого газа, равен 108,2 мл. Определите массовую долю фенола в растворе.
149. (С4) К этанолу массой 2,3 г добавили 60 г горячего 15%-ного раствора перманганата калия, подкисленного серной кислотой. Раствор нагревали до полного окисления этанола в уксусную кислоту. Определите массовую долю перманганата калия в полученном после окончания реакции растворе.
150. (С5) Массовая доля кислорода в предельном двухатомном спирте равна 42,11%. Установите молекулярную формулу спирта.
151. (С5) Установите молекулярную формулу предельного двухатомного спирта, массовая доля углерода в котором в 1,5 раза больше массовой доли кислорода.
152.(С5) Для окисления предельного одноатомного спирта массой 3,7 г до альдегида потребовалось 4,0 г оксида меди(II). Определите молекулярную формулу спирта.
153.(С5) При взаимодействии предельного одноатомного спирта массой 3,52 г с избытком натрия выделилось 0,448 л водорода. Определите молекулярную формулу спирта.
154.(С5) При взаимодействии предельного двухатомного спирта массой 2,7 г с избытком калия выделилось 0,672 л водорода. Определите молекулярную формулу спирта.
155. (С5) При сгорании предельного одноатомного спирта получили 26,4 г углекислого газа и 14,4 г воды. Установите молекулярную формулу спирта.
156. (С5) В результате межмолекулярной дегидратации предельного одноатомного спирта образовался простой эфир, массовая доля углерода в котором равна 52,17%. Установите молекулярную формулу спирта. 157. (С5) При сгорании предельного трехатомного спирта получили 1,12 л (н.у.) углекислого газа и 1,08 г воды. Установите молекулярную формулу спирта.
158.(С5) При взаимодействии гомолога фенола массой 9,76 г с избытком калия выделилось 0,896 л водорода. Определите молекулярную формулу гомолога фенола.
159. (С5) Установите молекулярную формулу органического вещества, если массовые доли углерода, водорода и кислорода в нем соответственно равны 60,00%, 13,33% и 26,67%. Плотность паров вещества по водороду равна 30.
160. (С5) При сгорании органического вещества массой 6,2 г получили 4,48 л углекислого газа (н.у.) и 5,4 г воды. Плотность паров вещества по азоту равна 2,214. Установите молекулярную формулу вещества.
161. При сгорании органического вещества массой 2,3 г получили 2,24 л углекислого газа (н.у.) и 2,7 г воды. Плотность паров вещества по метану равна 2,875. Установите молекулярную формулу вещества. 162. При сгорании органического вещества массой 4,8 г получили 3,36 л углекислого газа (н.у.) и 5,4 г воды. Плотность паров вещества по кислороду равна 1. Установите молекулярную формулу вещества.
Альдегиды и кетоны
Базовый уровень сложности
1. Состав предельных альдегидов выражается общей формулой
2. К карбонильным соединениям не относится
3. В молекуле пропаналя атомы углерода находятся в состоянии гибридизации
4. Число σ-связей в молекуле муравьиного альдегида равно
5. Число π-связей в молекуле муравьиного альдегида равно
6. Число π-связей в молекуле ацетона равно
7. Альдегиды изомерны
8. Этаналь и ацетальдегид являются
9. При гидрировании альдегидов образуются
10. Продуктом восстановления кетонов являются
11. При восстановлении пропанона образуется
12. При восстановлении этаналя образуется
13. При окислении бутаналя образуется
14. В реакции, схема которой HCОН + X→ HCOOH + Cu2O + Н2О, веществом Х может быть
15. Реакция «серебряного зеркала» характерна для
16. С аммиачным раствором оксида серебра взаимодействует каждое из двух веществ
17. С гидроксидом меди(II) взаимодействует каждое из двух веществ
18. Уксусный альдегид взаимодействует с
19. Метаналь взаимодействует с
20. И бутаналь, и бутанол-1 реагируют с
21. И пропаналь, и пропанон реагируют с
22. С каждым из трех веществ: Н2, [Ag(NH3)2]OH, Cu(OH)2 – может реагировать
23. Для непредельного альдегида акролеина, формула которого СН2=СН-СОН, справедливо утверждение
24. Для обнаружения альдегидов можно использовать каждое из двух веществ
25. Пропаналь можно отличить от пропанола-1 с помощью
26. Метанол окисляется до формальдегида под действием
27. Пропаналь можно получить в результате реакции
28. Ацетон можно получить в результате реакции
29. Фенолформальдегидную смолу получают по реакции
30. Пропаналь в отличие от пропанона взаимодействует с
31. Какие из приведенных утверждений об альдегидах и кетонах верны? А. Температуры кипения и плавления альдегидов и кетонов выше, чем у спиртов с тем же числом атомов углерода в молекуле. Б. При гидрировании альдегидов и кетонов образуются карбоновые кислоты.
32. Какие из приведенных утверждений об альдегидах и кетонах верны? А. Атом углерода в карбонильной группе находится в sp2-гибридном состоянии. Б. При окислении альдегидов и кетонов образуются спирты.
33. Какие из приведенных утверждений об альдегидах и кетонах верны? А. Альдегиды и кетоны – структурные изомеры одного класса. Б. Качественной реакцией на альдегиды и кетоны является реакция «серебряного зеркала».
34. Какие из приведенных утверждений об альдегидах и их свойствах верны? А. Альдегиды способны вступать в реакции восстановления и окисления. Б. Формальдегид и ацетальдегид токсичны.
35. Какие из приведенных утверждений об альдегидах и их свойствах верны? А. Между молекулами альдегидов водородные связи практически не образуются. Б. Низшие альдегиды вступают в реакцию полимеризации.
36. Какие из приведенных утверждений о метанале и его свойствах верны? А. Метаналь способен вступать в реакцию полимеризации. Б. 40%-ный водный раствор метаналя называется формалином.
37. Какие из приведенных утверждений о формальдегиде и его свойствах верны? А. Формальдегид – газ с резким запахом. Б. Формальдегид вступает в реакцию поликонденсации с фенолом.
38. В схеме превращений C2H2 → X → CH3COOH веществом Х может быть
39. В схеме превращений CH2=CH─CH3 → X → CH3COCH3 веществом Х может быть
40. В схеме превращений C2H2 веществами Х1 и Х2 соответственно являются
41. В схеме превращений C2H5ОН веществами Х1 и Х2 соответственно могут быть
4 2. В схеме превращений СН3СОН веществами Х1 и Х2 соответственно могут быть
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 1132; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.143.219 (0.13 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 X → C2H4 → C2H5OH
X → C2H4 → C2H5OH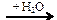 Х1 → CH3Cl
Х1 → CH3Cl 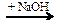 X2 → CH3-O-CH3 → CO2
X2 → CH3-O-CH3 → CO2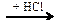 Х2
Х2  X3
X3 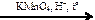 X4
X4 Х1
Х1  X3 → X2
X3 → X2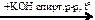 Х2
Х2 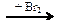 Х3
Х3  X5
X5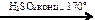 Х1
Х1  X3
X3 X1
X1  X2
X2  X4 → CO2
X4 → CO2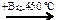 X1
X1  X2
X2  X3
X3  X4
X4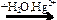 X1
X1  Х2
Х2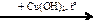 X2
X2 X1
X1 


