
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Условие термодинамического равновесия в раствореСодержание книги
Поиск на нашем сайте Взаимосвязь между энергией Гиббса раствора и химическими потенциалами отдельных компонентов описывается уравнением (2.3):
Приняв, что химический потенциал является постоянной величиной, проинтегрируем полученное уравнение:
Продифференцируем теперь при условии переменных массы раствора и его состава:
При равновесии dG = 0, тогда
следовательно,
Разделим на
где Уравнение (2.4) – уравнение Гиббса-Дюгема – является условием равновесия в гомогенном многокомпонентном растворе. Для двухкомпонентного раствора условие равновесия имеет вид:
Условие равновесия в гетерогенной системе Рассмотрим систему, состоящую из k независимых компонентов и m фаз, находящуюся в состоянии термодинамического равновесия при р, Т = const. Общее условие равновесия в системе имеет вид: dG = 0. Общая энергия Гиббса складывается из энергий Гиббса каждой из фаз:
Продифференцируем:
Для каждой из фаз
Подставим значение dG для каждой фазы:
Пусть без нарушения равновесия из первой фазы во вторую перешло бесконечно малое число моль 1-го компонента. При этом числа моль всех остальных компонентов постоянны во всех фазах и значения внешних параметров не изменяются: р, Т = const. Тогда условие равновесия приобретает вид:
Произведение равно нулю, если хотя бы один из множителей равен нулю, но согласно условию
Следовательно, химический потенциал первого компонента одинаков в обеих фазах. Рассматривая аналогичные частные случаи для других компонентов и фаз, получим:
Полученное уравнение является условием равновесия в m -фазной условием термодинамического равновесия в гетерогенной системе является равенство химических потенциалов каждого компонента во всех фазах при Р, Т = const или V, Т = const В качестве примера рассмотрим двухфазную трехкомпонентную систему. Условие равновесия для такой системы имеет вид:
где
Правило фаз Гиббса
Пусть при р, Т = const в состоянии равновесия существует система, состоящая из k компонентов и m фаз. На систему оказывают влияние s внешних параметров (на практике обычно s = 2 – это р и Т). Поставим задачу рассчитать число термодинамических степеней свободы данной системы. Число термодинамических степеней свободы – это число независимых параметров состояния данной системы, оно равно общему числу параметров состояния системы за вычетом числа уравнений, связывающих эти параметры. Для определения состава любой фазы, содержащей k компонентов достаточно указать содержание (k – 1) компонентов. Так как концентрации компонентов обычно выражены в массовых или мольных долях и концентрация одного из компонентов будет определена, если известны концентрации остальных компонентов. Например, двухкомпонентная система представляет собой 20 %-й водный раствор уксусной кислоты. Тогда массовую долю второго компонента – воды можно рассчитать: 100 – 20 = 80 %. Поэтому указывать, сколько в системе содержится воды необязательно. Если в системе m фаз, то для описания их состава требуется m(k–1) переменных. Кроме того, на систему влияют внешние параметры, количество которых равно s. Следовательно, общее количество переменных,влияющих на состояние системы равно: m(k – 1) + s. Однако не все эти переменные независимы друг от друга, та как при равновесии распределение каждого из компонентов между различными фазами должно удовлетворять теореме равновесия Гиббса:
Очевидно, что таких уравнений для каждого из компонентов будет на единицу меньше числа фаз. Например, если m = 3, то для первого компонента запишется только два уравнения:
тогда число уравнений, связывающих химические потенциалы одного компонента равно m – 1, а всех k компонентов – k(m – 1). Для определения числа термодинамических степеней свободы вычтем из общего числа параметров, описывающих состояние данной системы число уравнений, связывающих их:
После преобразований получим:
Уравнение (2.5) выражает основной закон фазового равновесия – правило фаз Гиббса. Если на систему влияют два внешних параметра (р и Т), то правило фаз Гиббса записывается
|
||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 416; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.007 с.) |

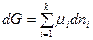


 ,
, .
.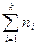 :
: , (2.4)
, (2.4) – мольная доля i -го компонента.
– мольная доля i -го компонента. .
. .
. .
. .
.

 , тогда
, тогда

 ,
, – химические потенциалы 1, 2 и 3-го компонентов в одной фазе;
– химические потенциалы 1, 2 и 3-го компонентов в одной фазе; – химические потенциалы 1, 2 и 3-го компонентов в другой фазе.
– химические потенциалы 1, 2 и 3-го компонентов в другой фазе.
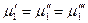 ,
,
 . (2.5)
. (2.5) .
.


