
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Расчеты показывают, что при учете движения других молекулСодержание книги
Поиск на нашем сайте
<z>= Тогда средняя длина свободного пробега < т.е. < Явления переноса в термодинамически неравновесных системах В термодинамически неравновесных системах возникают особые необратимые процессы, называемые явлениями переноса, в результате которых происходит пространственный перенос энергии, массы, импульса. К явлениям переноса относятся теплопроводность (обусловлена переносом энергии), диффузия (обусловлена переносом массы) и внутреннее трение (обусловлено переносом импульса). Для простоты ограничимся одномерными явлениями переноса. Систему отсчета будем выбирать так, чтобы ось х была ориентирована в на- 1. Теплопроводность. Если в одной области газа средняя кинетическая энергия молекул больше, чем в другой, то с течением времени вследствие постоянных столкновений молекул происходит процесс выравнивания средних кинетических энергий молекул, т.е., иными словами, выравнивание температур. Перенос энергии в форме теплоты подчиняется закону Фурье:
где Можно показать, что
где сv - удельная теплоемкость газа при постоянном объеме, р - плотность газа, 2. Диффузия. Явление диффузии заключается в том, что происходит самопроизвольное проникновение и перемешивание частиц двух соприкасающихся газов, жидкостей и даже твердых тел; диффузия сводится к обмену масс частиц этих тел, возникает и продолжается, пока существует градиент плотности. Во время становления молекулярно-кинетической теории по вопросу диффузии возникли противоречия. Так как молекулы движутся с огромными скоростями, диффузия должна происходить очень быстро. Если же открыть в комнате сосуд с пахучим веществом, то запах распространяется очень медленно. Однако противоречия здесь нет. Молекулы при атмосферном давлении обладают малой длиной свободного пробега и сталкиваясь с другими молекулами, в основном "стоят" на месте. Явление диффузии для химически однородного газа подчиняется
Диффузия D численно равна плотности потока массы при градиенте плотности равном единице. Согласно кинетической теории газов,
3. Внутреннее трение (вязкость). Механизм возникновения внутреннего трения между параллельными слоями газа (жидкости), движущимися с различными скоростями, заключается в том, что из-за хаотического теплового движения происходит обмен молекулами между слоями, в результате чего импульс слоя, движущегося быстрее, уменьшается, движущегося медленнее - увеличивается, что приводит к торможению слоя, движущегося быстрее, и ускорению слоя, движущегося медленнее. Согласно формуле (6.8), сила внутреннего трения между двумя слоями газа (жидкости) подчиняется закону Ньютона:
Взаимодействие двух слоев согласно второму закону Ньютона можно рассматривать как процесс, при котором от одного слоя к другому в единицу времени передается импульс, по модулю равный действующей силе. Тогда выражение (1.26) можно представить в виде
Динамическая вязкость h численно равна плотности потока импульса при градиенте скорости равном единице; она вычисляется по формуле
Рассмотренные законы Фурье, Фика и Ньютона не вскрывают молекул молекулярно-кинетического смысла коэффициентов l, D и h. Выражения для коэффициентов переноса выводятся из кинетической теории. Они записаны без выводов, т.к. строгое рассмотрение явлений переноса довольно громоздко, а качественное не имеет смысла. Формулы (1.23), (1.25) и (1-28) связывают коэффициенты переноса и характеристики теплового движения молекул. Из этих формул вытекают простые зависимости между l, D и h: h=rD,
ОСНОВЫ ТЕРМОДИНАМИКИ 2.1. Число степеней свободы молекулы. Важной характеристикой термодинамической системы является ее внутренняя энергия U - энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.д.) и энергия взаимодействия этих частиц. Из этого определения следует, что к внутренней энергии не относятся кинетическая энергия движения системы как целого и потенциальная энергия системы во внешних полях. Внутренняя энергия - однозначная функция термодинамического состояния системы, т.е. в каждом состоянии система обладает вполне определенной внутренней энергией. Это означает, что при переходе системы из одного состояния в другое изменение внутренней энергии определяется только разностью значений внутренней энергии этих состояний и не зависит от пути перехода. Ранее было введено понятие степеней свободы - числа независимых переменных (координат), полностью определяющих положение системы в пространстве. В ряде задач молекулу одноатомного газа (рис. 55 а) рассматривают как материальную точку, которой приписывают три степени свободы поступательного движения. При этом энергию вращательного движения можно не учитывать (r®0, J=mr2 ®0,
Рис. 55 В классической механике молекула двухатомного газа в первом приближении рассматривается как совокупность двух материальных точек, жестко связанных Недеформируемой связью (рис. 55 6). Эта система кроме трех степеней свободы поступательного движения имеет еще две степени свободы вращательного движения. Вращение вокруг третьей оси (оси, проходящей через оба атома) лишено смысла, так как момент инерции относительно этой оси»0. Таким образом, двухатомный газ обладает пятью степенями свободы (i = 5). Трехатомная (рис. 55 в) и многоатомная нелинейные молекулы имеют шесть степеней свободы: три поступательных и три вращательных. Естественно, что жесткой связи между атомами не существует. Поэтому для реальных молекул необходимо учитывать также степени свободы колебательного движения. Независимо от общего числа степеней свободы молекул, три степени свободы всегда поступательные. Ни одна из поступательных степеней свободы не имеет преимущества перед другими, поэтому на каждую из них приходится в среднем одинаковая энергия, равная 1/3 значения <e0>в (2.18):
В классической статистической физике выводится закон Больцмана о равномерном распределении энергии по степеням свободы молекул: для статистической системы, находящейся в состоянии термодинамического равновесия, на каждую поступательную и вращательную степени свободы приходится в среднем кинетическая энергия, равная kT/2, а на каждую колебательную степень свободы - в среднем энергия, равная kT. Колебательная степень обладает вдвое большей энергией потому, что на нее приходится не только кинетическая энергия, но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы. Таким образом, средняя энергия молекулы
где i - сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы:
В классической теории рассматривают молекулы с жесткой связью между атомами; для них i совпадает с числом степеней свободы молекулы. Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю, то внутренняя энергия, отнесенная к одному молю газа, равна сумме кинетических энергий NA молекул:
Внутренняя энергия для произвольной массы m газа
Первое начало термодинамики Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Внутренняя энергия системы может изменяться в результате различных процессов, например, совершения над системой работы и сообщения ей теплоты. Так, вдвигая поршень в цилиндр, в котором находится газ, мы сжимаем этот газ, в результате чего его температура повышается, т.е. тем самым изменяется (увеличивается) внутренняя энергия газа. С другой стороны, температуру газа и его внутреннюю энергию можно повысить за счет сообщения ему некоторого количества теплоты - энергии, переданной: системе внешними телами путем теплообмена. Таким образом, можно говорить о двух формах передачи энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии; применительно к термодинамическим процессам этим законом и является первое начало термодинамики, установленное в результате обобщения многовековых опытных данных. Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U1, получила некоторое количество теплоты Q и, перейдя в новое состояние, характеризующееся внутренней энергией U2, совершила работу А над внешней средой, т.е. против внешних сил. Количество теплоты считается положительным, когда оно подводится к системе, а работа - положительной, когда система совершает ее против внешних сил. Опыт показывает, что в соответствии с законом сохранения энергии при любом способе перехода системы из первого состояния во второе изменение внутренней энергии DU=U2 –U1 будет одинаковым и равным разности между количеством теплоты Q, полученным системой, и работой А, совершенной системой против внешних сил:
или
Выражение (2.2) в дифференциальной форме будет иметь вид
или в более корректной форме
Из формулы (2.3) следует, что в системе СИ количество теплоты выражается в тех же единицах, что работа и энергия, т.е. в джоулях (Дж). Если система периодически возвращается в первоначальное состояние, то изменение ее внутренней энергии DU=0. Тогда, согласно первому началу термодинамики, А=Q, т.е. вечный двигатель первого рода - периодически действующий двигатель, который совершал бы большую работу, чем сообщенная ему извне энергия, - невозможен (одна из формулировок первого начала термодинамики).
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 344; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.17.210 (0.008 с.) |

 pd2n<
pd2n<  >.
>. >=
>=  ,
, , (1.22)
, (1.22)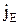 - плотность теплового потока – величина, определяемая энергией, переносимой в форме теплоты в единицу времени через единичную площадку.перпендикулярную оси х, l - теплопроводность,
- плотность теплового потока – величина, определяемая энергией, переносимой в форме теплоты в единицу времени через единичную площадку.перпендикулярную оси х, l - теплопроводность,  - градиент температуры, равный скорости изменения температуры на единицу длины х в направлении нормали к этой площадке. Знак минус показывает, что при теплопроводности энергия переносится в направлении убывания температуры (поэтому знаки
- градиент температуры, равный скорости изменения температуры на единицу длины х в направлении нормали к этой площадке. Знак минус показывает, что при теплопроводности энергия переносится в направлении убывания температуры (поэтому знаки  , (1.23)
, (1.23) - средняя скорость теплового движения молекул, <
- средняя скорость теплового движения молекул, <  , (1.24)
, (1.24) - плотность потока массы - величина, определяемая массой вещества, диффундирующего в единицу времени через единичную площадку, перпендикулярную оси х; D - диффузия (коэффициент диффузии);
- плотность потока массы - величина, определяемая массой вещества, диффундирующего в единицу времени через единичную площадку, перпендикулярную оси х; D - диффузия (коэффициент диффузии);  - градиент плотности на единицу длины х в направлении нормали к этой площадке. Знак минус показывает, что перенос массы происходит в направлении убывания плотности (поэтому знаки
- градиент плотности на единицу длины х в направлении нормали к этой площадке. Знак минус показывает, что перенос массы происходит в направлении убывания плотности (поэтому знаки  . (1.23)
. (1.23) , (1.26)
, (1.26) - градиент скорости, показывающий быстроту изменения скорости в направлении х, перпендикулярном направлению движения слоев, S -площадь, на которую действует сила F.
- градиент скорости, показывающий быстроту изменения скорости в направлении х, перпендикулярном направлению движения слоев, S -площадь, на которую действует сила F. , (1.27)
, (1.27) - плотность потока импульса – величина, определяемая полным импульсом, переносимым в единицу времени в положительном направлении оси х через единичную площадку, перпендикулярную осих;
- плотность потока импульса – величина, определяемая полным импульсом, переносимым в единицу времени в положительном направлении оси х через единичную площадку, перпендикулярную осих;  . (1.28)
. (1.28) . Используя эти формулы, можно по найденным из опыта одним величинам определить другие.
. Используя эти формулы, можно по найденным из опыта одним величинам определить другие. ).
).
 .
. ,
, .
. . (2.1)
. (2.1) , где k - постоянная Больцмана, n -количество вещества.
, где k - постоянная Больцмана, n -количество вещества.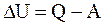
 . (2.2)
. (2.2)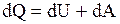
 , (2.3)
, (2.3)


