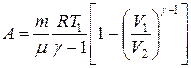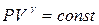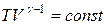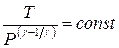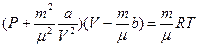| №
| Наименование физической величины или физического закона
| Математическая запись
|
|
| Закон Бойля – Мариотта
| P1V1=P2V2
|
|
| Закон Гей – Люссака
| V1/V2=T1/T2
|
|
| Закон Шарля
| P1/P2=T1/T2
|
|
| Связь между массой (m), количеством
вещества (n) и молярной массой (m)
| m=nm
|
| №
| Наименование физической величины или физического закона
| Математическая запись
|
|
| Уравнение Менделеева – Клапейрона для смеси компонентов газа
| 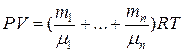
|
|
| m – масса молекулы;
NA – число Авогадро, число молекул в одном моле вещества.
|  ,
где NA =6.02 ·10 23моль –1 ,
где NA =6.02 ·10 23моль –1
|
|
| N – число молекул в веществе
| 
|
|
|  - средняя кинетическая энергия движения молекулы;
i – число степеней свободы молекулы;
i =3 для одноатомного газа;
i =5 для двухатомного;
i =6 для многоатомного. - средняя кинетическая энергия движения молекулы;
i – число степеней свободы молекулы;
i =3 для одноатомного газа;
i =5 для двухатомного;
i =6 для многоатомного.
|
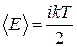
|
|
| Основное уравнение молекулярно-кинетической теории
| 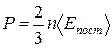
|
|
| U – внутренняя энергия газа;
R - молярная газовая постоянная;
k – постоянная Больцмана.
| 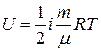 R= 8.31 Дж/(моль·К);
k = R/NA
k = 1.38·10-23 Дж/К
R= 8.31 Дж/(моль·К);
k = R/NA
k = 1.38·10-23 Дж/К
|
|
| 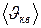 - средняя квадратичная скорость молекул; - средняя квадратичная скорость молекул;
 - средняя арифметическая скорость молекул; - средняя арифметическая скорость молекул;
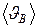 - наивероятнейшая скорость молекул. - наивероятнейшая скорость молекул.
| 

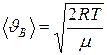
|
|
| Q –количество теплоты, необходимое для нагревания вещества массой m от температуры Т1 до Т2;
с – удельная теплоемкость вещества
|
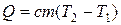
|
|
| СV – удельная теплоемкость газа при постоянном объеме;
СР - удельная теплоемкость газа при постоянном давлении.
| 

|
| №
| Наименование физической величины или физического закона
| Математическая запись
|
|
| 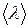 - средняя длина свободного пробега молекул;
d –эффективный диаметр молекул;
n – концентрация молекул. - средняя длина свободного пробега молекул;
d –эффективный диаметр молекул;
n – концентрация молекул.
|

|
|
| Закон диффузии (закон Фика):
масса определенного компонента газа(dm), диффундирующая за время dt через площадку ds, расположенную перпендикулярно оси Х.
D – коэффициент диффузии;
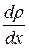 - градиент плотности; - градиент плотности;
|
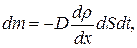

|
|
| Закон теплопроводности (закон Фурье):
Количество теплоты dQ, переносимое за время dt через площадку ds, расположенную перпендикулярно оси Х.
 - коэффициент теплопроводности; - коэффициент теплопроводности;
 - градиент температуры;
r - плотность газа. - градиент температуры;
r - плотность газа.
|


|
|
| Закон вязкости (закон Ньютона):
Сила внутреннего трения dF между двумя слоями площадью ds, движущимися с различными скоростями.
 - коэффициент динамической вязкости; - коэффициент динамической вязкости;
 - градиент скорости течения газа в направлении, перпендикулярном к площадке ds. - градиент скорости течения газа в направлении, перпендикулярном к площадке ds.
|

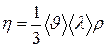
|
|
| Распределение Максвелла
 - число молекул, скорости которых лежат в интервале от - число молекул, скорости которых лежат в интервале от  до до  ;
N –общее число молекул;
m0 – масса молекулы. ;
N –общее число молекул;
m0 – масса молекулы.
| 
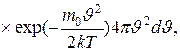
|
|
| Барометрическая формула
P и P0 – давление на высоте h и h0.
| 
|
| №
| Наименование физической величины или физического закона
| Математическая запись
|
|
| Распределение Больцмана
n0 и Е0 – концентрация и потенциальная энергия частиц на высоте h0.
| 
|
|
| Первое начало термодинамики
| 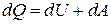
|
|
| Работа газа при изотермическом процессе:
| 
|
|
| Работа газа при изобарическом процессе:
| 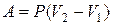
|
|
| Работа газа при адиабатическом процессе:
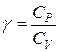 - показатель адиабаты. - показатель адиабаты.
| 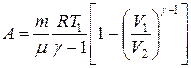
|
|
| Уравнения Пуассона:
| 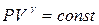
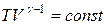
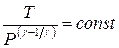
|
|
| Коэффициент полезного действия тепловой машины:
Q1 – количество теплоты, полученное рабочим телом от нагревателя;
Q2 – количество теплоты, переданной рабочим телом холодильнику;
А – работа, совершенная машиной.
|

|
|
| Коэффициент полезного действия цикла Карно:
Т1 – температура нагревателя;
Т2 – температура холодильника.
|

|
|
| Уравнение Ван-дер-Ваальса для произвольной массы m газа:
Р – давление газа,
V – молярный объем газа,
m – масса газа,
μ – молярная масса газа,
Т – температура,
a, b – (коэффициенты пропорциональности) постоянные Ван – дер –Ваальса.
|
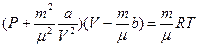
|
Приложение Б.



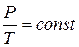
 A=0
A=0


 A=pDV
A=pDV


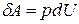 A = -DU=
=-CVDТ
A = -DU=
=-CVDТ
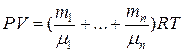
 ,
где NA =6.02 ·10 23моль –1
,
где NA =6.02 ·10 23моль –1

 - средняя кинетическая энергия движения молекулы;
i – число степеней свободы молекулы;
i =3 для одноатомного газа;
i =5 для двухатомного;
i =6 для многоатомного.
- средняя кинетическая энергия движения молекулы;
i – число степеней свободы молекулы;
i =3 для одноатомного газа;
i =5 для двухатомного;
i =6 для многоатомного.
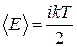
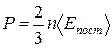
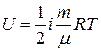 R= 8.31 Дж/(моль·К);
k = R/NA
k = 1.38·10-23 Дж/К
R= 8.31 Дж/(моль·К);
k = R/NA
k = 1.38·10-23 Дж/К
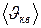 - средняя квадратичная скорость молекул;
- средняя квадратичная скорость молекул;
 - средняя арифметическая скорость молекул;
- средняя арифметическая скорость молекул;
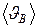 - наивероятнейшая скорость молекул.
- наивероятнейшая скорость молекул.


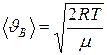
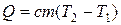


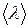 - средняя длина свободного пробега молекул;
d –эффективный диаметр молекул;
n – концентрация молекул.
- средняя длина свободного пробега молекул;
d –эффективный диаметр молекул;
n – концентрация молекул.

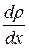 - градиент плотности;
- градиент плотности;
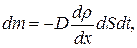

 - коэффициент теплопроводности;
- коэффициент теплопроводности;
 - градиент температуры;
r - плотность газа.
- градиент температуры;
r - плотность газа.


 - коэффициент динамической вязкости;
- коэффициент динамической вязкости;
 - градиент скорости течения газа в направлении, перпендикулярном к площадке ds.
- градиент скорости течения газа в направлении, перпендикулярном к площадке ds.

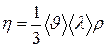
 - число молекул, скорости которых лежат в интервале от
- число молекул, скорости которых лежат в интервале от  до
до  ;
N –общее число молекул;
m0 – масса молекулы.
;
N –общее число молекул;
m0 – масса молекулы.

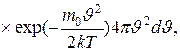


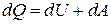
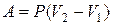
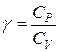 - показатель адиабаты.
- показатель адиабаты.