Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кооперативное связывание гемоглобина с кислородомСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Гемоглобин связывает и передает тканям за сутки около 600 л О2, в тканях образуется примерно 500 л СО2, который выводится из организма при участии гемоглобина. Скорость оксигенирования и транспорт кислорода из лёгких в ткани зависит от изменений сродства гемоглобина к О2. Присоединением О2 к одному из протомеров гемоглобина в лёгких при высоком рО2, (100 мм рт. ст.) вызывает конформационные изменения во всей олигомерной структуре гемоглобина и облегчает присоединение последующих молекул О2. Это явление носит название кооперативных изменений гемоглобина или кооперативного связывания О2, благодаря которому гемоглобин максимально связывает О2 в легких и легко отдает О2 в периферических тканях при более низких значениях рО2 (рис кривая насыщения миоглобина и гемоглобина).
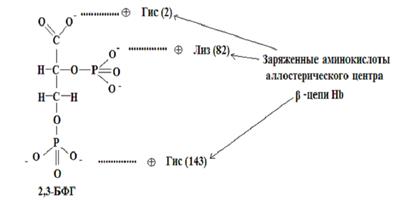
Давление в капиллярах Давление в лёгочных работающей мышцы а л ь в е о л а х Рис. Кривые насыщения (диссоциации) миоглобина и гемоглобина кислородом. Кривая насыщения для гемоглобина имеет сигмоидную форму (S-образную). Это указывает на кооперативное связывание О2 (в легких при высоком рО2) и освобождении О2 (в тканевых капиллярах при более низком рО2). Эффект Бора Гемоглобин не только переносит О2 от легких к периферическим тканям, но и ускоряет транспорт СО2 и протонов от тканей к легким. Эффект Бора – это влияние концентрации СО2 и Н+ на сродство гемоглобина к О2. Увеличение концентрации протонов и СО2 снижает сродство О2 к гемоглобину и усиливает транспорт О2 в ткани. Разные органы потребляют неодинаковые количества кислорода. Наиболее активно извлекают кислород из крови работающие мышцы (до 85%). Если гемоглобин насыщен кислородом почти на 100%, то все молекулы гемоглобина находятся в R-форме, Нb(О2)4. Такое состояние гемоглобина возникает при высоком парциальном О2 в капиллярах легких (100 мм рт. ст.) и при высоком сродстве Нb к О2. В капиллярах мышц и других тканей более низкое парциальное давление О2, в этих условиях от гемоглобина могут отщепляться молекулы О2 и поступать в ткани. Например, при парциальном давлении кислорода в капиллярах 40 мм рт. ст. гемоглобин имеет насыщение ≈ 65%. Далее действуют другие факторы, приводящие к снижению сродства гемоглобина к О2, тем самым увеличивая доставку кислорода в ткани: а) гемоглобин протонируется, связывая три пары Н+ в пептидных цепях гемоглобина, вновь формируется Т-структура; б) гемоглобин обратимо присоединяет часть СО2 (до 15%) к концевым аминогруппам пептидных цепей, образуется карбогемоглобин: R-NH-COO- +Н+, где R-белковая цепь гемоглобина. Это также снижает сродство гемоглобина к О2. Большая часть СО2 транспортируется кровью в виде бикарбоната НСО3 -. Таким образом, диоксид углерода, образовавшийся в тканях реагирует с водой, образуя угольную кислоту, которая диссоциирует на бикарбонат- ион и Н+. Синтез углекислоты, как и её разложение на СО2 и Н2О происходит при участии фермента карбоангидразы. В периферических тканях гемоглобин отдает О2, сам протонируется и связывает часть СО2, его R-форма переходит в Т-форму, сродство к О2 резко снижается. В легких происходят обратные процессы. Влияние 2,3-БФГ на сродство гемоглобина к кислороду 2,3-биcфосфоглицерат (2,3-дифосфоглицерат) – образуется в эритроцитах в ходе анаэробного гликолиза из промежуточного соединения 1,3-биcфосфоглицерата. 2,3-БФГ является аллостерическим регулятором гемоглобина (от греч. «аллос» – другой), он соединяется ионными связями с дезоксигемоглобином не в области гема, а в другом участке, т. е. аллостерическом центре, содержащим положительно заряженные радикалы аминокислот Лиз 82 и Гис 143 β- цепей.
Структура 2,3-бифосфоглицерата
Образовавшиеся дополнительные солевые мостики (или ионные связи) делают структуру дезоксигемоглобина ещё более жесткой и поэтому сродство Нb к О2 снижается. Концентрация 2,3-БФГ в крови близка к концентрации гемоглобина и одинакова в артериальной и венозной крови. 2,3-БФГ реагирует только с дезоксигемоглобином, т. е. Т-формой, т. к. он имеет доступную центральную полость с центром связывания 2,3-БФГ. В оксигемоглобине (R-форма) эта полость закрыта.
|
||||
|
Последнее изменение этой страницы: 2016-09-20; просмотров: 1176; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.51.72 (0.006 с.) |