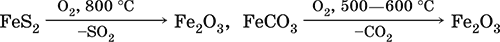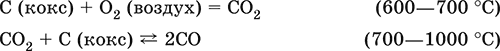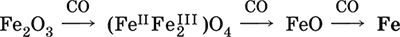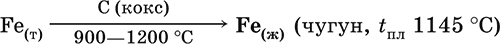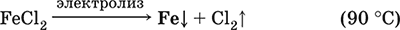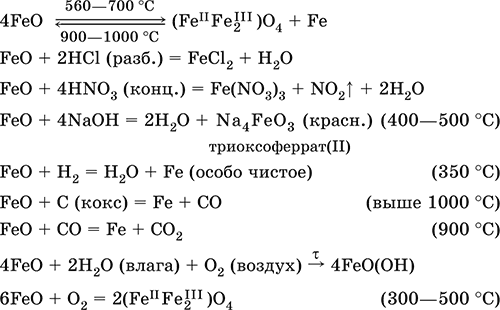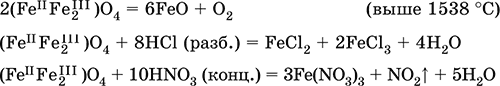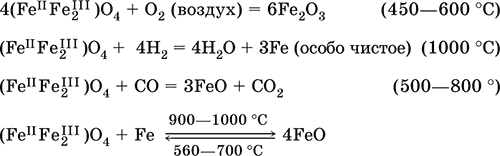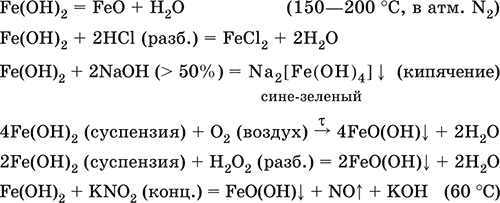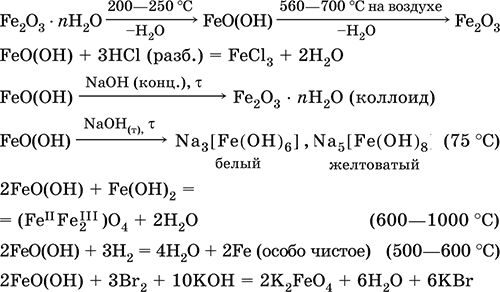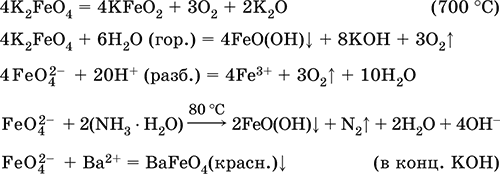Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Доменный процесс производства чугунаСодержание книги
Поиск на нашем сайте
Доменный процесс производства чугуна составляют следующие стадии: а) подготовка (обжиг) сульфидных и карбонатных руд – перевод в оксидную руду:
б) сжигание кокса при горячем дутье:
в) восстановление оксидной руды угарным газом СО последовательно (см. рубрики соответствующих оксидов):
г) науглероживание железа (до 6,67 % С) и расплавление чугуна:
В чугуне всегда в виде зерен присутствуют цементит Fe2C и графит.
Производство стали
Передел чугуна в сталь проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева; температура процесса 1700–2000 °C. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (СO2, SO2), либо связываются в легко отделяемый шлак – смесь Са3(РO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов. Получение чистого железа в промышленности – электролиз раствора солей железа, например:
(существуют и другие специальные методы, в том числе восстановление оксидов железа водородом). Чистое железо применяется в производстве специальных сплавов, при изготовлении сердечников электромагнитов и трансформаторов, чугун – в производстве литья и стали, сталь – как конструкционный и инструментальный материалы, в том числе износо‑, жаро– и коррозионно‑стойкие. Оксид железа(II) FeO. Амфотерный оксид с большим преобладанием основных свойств. Черный, имеет ионное строение Fe2+O2‑. При нагревании вначале разлагается, затем образуется вновь. Не образуется при сгорании железа на воздухе. Не реагирует с водой. Разлагается кислотами, сплавляется со щелочами. Медленно окисляется во влажном воздухе. Восстанавливается водородом, коксом. Участвует в доменном процессе выплавки чугуна. Применяется как компонент керамики и минеральных красок. Уравнения важнейших реакций:
Получение в лаборатории: термическое разложение соединений железа (II) без доступа воздуха: Fe(OH)2 = FeO + H2O (150–200 °C) FeCO3 = FeO + СO2 (490–550 °C) Оксид дижелеза (III) – железа(II) (FeIIFe2III)O4. Двойной оксид. Черный, имеет ионное строение Fe2+(Fe3+)2(O2‑)4. Термически устойчив до высоких температур. Не реагирует с водой. Разлагается кислотами. Восстанавливается водородом, раскаленным железом. Участвует в доменном процессе производства чугуна. Применяется как компонент минеральных красок (железный сурик), керамики, цветного цемента. Продукт специального окисления поверхности стальных изделий (чернение, воронение). По составу отвечает коричневой ржавчине и темной окалине на железе. Применение брутто‑формулы Fe3O4 не рекомендуется. Уравнения важнейших реакций:
Получение: сгорание железа (см.) на воздухе. В природе – оксидная руда железа магнетит. Оксид железа(III) Fe2O3. Амфотерный оксид с преобладанием основных свойств. Красно‑коричневый, имеет ионное строение (Fe3+)2(O2‑)3. Термически устойчив до высоких температур. Не образуется при сгорании железа на воздухе. Не реагирует с водой, из раствора выпадает бурый аморфный гидрат Fe2O3 nН2O. Медленно реагирует с кислотами и щелочами. Восстанавливается монооксидом углерода, расплавленным железом. Сплавляется с оксидами других металлов и образует двойные оксиды – шпинели (технические продукты называются ферритами). Применяется как сырье при выплавке чугуна в доменном процессе, катализатор в производстве аммиака, компонент керамики, цветных цементов и минеральных красок, при термитной сварке стальных конструкций, как носитель звука и изображения на магнитных лентах, как полирующее средство для стали и стекла. Уравнения важнейших реакций:
Получение в лаборатории – термическое разложение солей железа(III) на воздухе: Fe2(SO4)3 = Fe2O3 + 3SO3 (500–700 °C) 4{Fe(NO3)3 9 H2O} = 2FeaO3 + 12NO2 + 3O2 + 36H2O (600–700 °C) В природе – оксидные руды железа гематит Fe2O3 и лимонит Fe2O3 nН2O. Гидроксид железа (II) Fe(OH)2. Амфотерный гидроксид с преобладанием основных свойств. Белый (иногда с зеленоватым оттенком), связи Fe – ОН преимущественно ковалентные. Термически неустойчив. Легко окисляется на воздухе, особенно во влажном состоянии (темнеет). Нерастворим в воде. Реагирует с разбавленными кислотами, концентрированными щелочами. Типичный восстановитель. Промежуточный продукт при ржавлении железа. Применяется в изготовлении активной массы железоникелевых аккумуляторов. Уравнения важнейших реакций:
Получение: осаждение из раствора щелочами или гидратом аммиака в инертной атмосфере: Fe2+ + 2OН(разб.) = Fe(OH)2↓ Fe2+ + 2(NH3 H2O) = Fe(OH)2 ↓ + 2NH4+ Метагидроксид железа FeO(OH). Амфотерный гидроксид с преобладанием основных свойств. Светло‑коричневый, связи Fe – О и Fe – ОН преимущественно ковалентные. При нагревании разлагается без плавления. Нерастворим в воде. Осаждается из раствора в виде бурого аморфного полигидрата Fe2O3 nН2O, который при выдерживании под разбавленным щелочным раствором или при высушивании переходит в FeO(OH). Реагирует с кислотами, твердыми щелочами. Слабый окислитель и восстановитель. Спекается с Fe(OH)2. Промежуточный продукт при ржавлении железа. Применяется как основа желтых минеральных красок и эмалей, поглотитель отходящих газов, катализатор в органическом синтезе. Соединение состава Fe(OH)3 не известно (не получено). Уравнения важнейших реакций:
Получение: осаждение из раствора солей железа(III) гидрата Fe2O3 nН2O и его частичное обезвоживание (см. выше). В природе – оксидная руда железа лимонит Fe2O3 nН2O и минерал гётит FeO(OH). Феррат калия K2FeO4. Оксосоль. Красно‑фиолетовый, разлагается при сильном нагревании. Хорошо растворим в концентрированном растворе КОН, реагирует с кипящей водой, неустойчив в кислотной среде. Сильный окислитель. Качественная реакция – образование красного осадка феррата бария. Применяется в синтезе ферритов – промышленно важных двойных оксидов железа (III) и других металлов. Уравнения важнейших реакций:
Получение: образуется при окислении соединений железа, например метагидроксида FeO(OH), бромной водой, а также при действии сильных окислителей (при спекании) на железо Fe + 2KOH + 2KNO3 = K2FeO4 + 3KNO2 + H2O (420 °C) и электролизе в растворе:
(феррат калия образуется на аноде). Качественные реакции на ионы Fe2+ и Fe3+. Обнаружение ионов Fe2+ и Fe3+ в водном растворе проводят с помощью реактивов K3[Fe(CN)6] и K4[Fe(CN)6] соответственно; в обоих случаях выпадает синий продукт одинакового состава и строения, KFeIII[FeII(CN)6]. В лаборатории этот осадок называют берлинская лазурь, или турнбуллева синь: Fe2+ + К+ + [Fe(CN)6]3‑ = KFeIII[FeII(CN)6]↓ Fe3+ + K+ + [Fe(CN)6]4‑ = KFeIII[FeII(CN)6]↓ Химические названия исходных реактивов и продукта реакций: K3[Fe(CN)6] – гексацианоферрат (III) калия K4[Fe(CN)6] – гексацианоферрат (II) калия KFeIII[FeII(CN)6] – гексацианоферрат (II) железа(III) калия Кроме того, хорошим реактивом на ионы Fe3+ является тиоцианат‑ион NCS‑, железо (III) соединяется с ним, и появляется ярко‑красная («кровавая») окраска: Fe3+ + 6NCS– = [Fe(NCS)6]3‑ Этим реактивом (например, в виде соли KNCS) можно обнаружить даже следы железа (III) в водопроводной воде, если она проходит через железные трубы, покрытые изнутри ржавчиной.
|
||||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 97; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.77.73 (0.009 с.) |