
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Окисление этанола в печени. Первичные эффекты этанола.Содержание книги
Поиск на нашем сайте
Окисление этанола NAD-зависимой алкогольдегидрогеназой - Основную роль в метаболизме этанола играет цинксодержащий NAD+- зависимый фермент - алкогольдегидрогеназа, локализующаяся в основном в цитозоле и митохондриях печени (95%). В ходе реакции происходит дегидрирование этанола, образуются ацетальдегид и восстановленный кофермент NADH. Алкогольдегидрогеназа катализирует обратимую реакцию, направление которой зависит от концентрации ацетальдегида и соотношения NADH/NAD+ в клетке. С2Н5ОН + HAD+ ↔ СН3СНО + NADH + H+. Фермент алкогольдегидрогеназа - димер, состоящий из идентичных или близких по первичной структуре полипептидных цепей, кодируемых аллелями одного гена. Существуют 3 изоформы алкогольдегидрогеназы (АДГ): АДГ1, АДГ2, АДГ3, различающиеся по строению протомеров, локализации и активности. Для европейцев характерно присутствие изоформ АДГ1 и АДГ3. У некоторых восточных народов преобладает изоформа АДГ2, характеризующаяся высокой активностью, это может быть причиной их повышенной чувствительности к алкоголю. При хроническом алкоголизме количество фермента в печени не увеличивается, т.е. он не является индуцируемым ферментом. Окисление этанола каталазой - Второстепенную роль в окислении этанола играет каталаза, находящаяся в пероксисомах цитоплазмы и митохондрий клеток печени. Этот фермент расщепляет примерно 2% этанола, но при этом утилизирует пероксид водорода. СН3СН2ОН + Н2О2 → СН3СНО + 2Н2О. 101. Метаболические нарушения при алкогольной интоксикации. Особенности катаболизма лекарственных средств при участии микросомальной системы окисления в условиях алкогольной интоксикации. Характеристика компонентов микросомальной системы окисления. Роль цитохрома Р450. Окисление этанола при участии цитохром Р450 - зависимой микросомальной этанолокисляющей системы системы - Цитохром Р450-зависимая микросомальная этанолокисляющая сисгема (МЭОС) локализована в мембране гладкого ЭР гепатоцитов. МЭОС играет незначительную роль в метаболизме небольших количеств алкоголя, но индуцируется этанолом, другими спиртами, лекарствами типа барбитуратов и приобретает существенное значение при злоупотреблении этими веществами. Этот путь окисления этанола происходит при участии одной из изоформ Р450 - изофермента Р450 II E1. При хроническом алкоголизме окисление этанола ускоряется на 50 - 70% за счёт гипертрофии ЭР и индукции цитохрома Р450 II E1. С2Н5ОН + NADPH + Н+ + О2 → СН3СНО + NADP+ + 2Н2О. Кроме основной реакции, цитохром Р450 катализирует образование активных форм кислорода (О2-, Н2О2), которые стимулируют ПОЛ в печени и других органах. Ацетальдегид, образовавшийся из этанола, окисляется до уксусной кислоты двумя ферментами: FAD -зависимой альдегидоксидазой и NAD+ -зависимой ацетальдегиддегидрогеназой (АлДГ). СН3СНО + О2 + H2O → СН3СООН + Н2О2. Повышение концентрации ацетальдегида в клетке вызывает индукцию фермента алъдегидоксидазы. В ходе реакции образуются уксусная кислота, пероксид водорода и другие активные формы кислорода, что приводит к активации ПОЛ. Другой фермент ацетальдегиддегидрогеназа (АлДГ) окисляет субстрат при участии кофермента NAD+. СН3СНО + Н2О + NAD+ → СН3СООН + NADH + H+. Полученная в ходе реакции уксусная кислота активируется под действием фермента ацетил-КоА-синтетазы. Реакция протекает с использованием кофермента А и молекулы АТФ. Образовавшийся ацетил-КоА, в зависимости от соотношения АТФ/АДФ и концентрации окса-лоацетата в митохондриях гепатоцитов, может "сгорать" в ЦТК, идти на синтез жирных кислот или кетоновых тел. В разных тканях организма человека встречаются полиморфные варианты АлДГ. Они характеризуются широкой субстратной специфичностью, разным распределением по клеткам тканей (почки, эпителий, слизистая оболочка желудка и кишечника) и в компартментах клетки. Например, изоформа АлДГ, локализованная в митохондриях гепатоцитов, обладает более высоким сродством к ацетальдегиду, чем цитозольная форма фермента. Ферменты, участвующие в окислении этанола, - алкогольдегидрогеназа и АлДГ по разному распределены: в цитозоле - 80%/20% и митохондриях - 20%/80%. При поступлении больших доз алкоголя (более 2 г/кг) из-за разных скоростей окисления этанола и ацетальдегида в цитозоле резко повышается концентрация последнего. Ацетальдегид - очень реакционно-способное соединение; он неферментативно может ацетилировать SH-, NH2- группа белков и других соединений в клетке и нарушать их функции. В модифицированных (ацетилированных) белках могут возникать "сшивки", нехарактерные для нативной структуры (например, в белках межклеточного матрикса - эластине и коллагене, некоторых белках хроматина и липопротеинов, формирующихся в печени). Ацетилирование ядерных, цитоплазматических ферментов и структурных елков приводит к снижению синтеза экспортируемых печенью в кровь белков, например альбумина, который, удерживая Na+, поддерживает коллоидно-осмотическое давление, а также участвует в транспорте многих гидрофобных веществ в крови. Нарушение функций альбумина в сочетании с повреждающим действием ацетальдегида на мембраны сопровождается поступлением в клетки по градиенту концентрации ионов натрия и воды, происходит осмотическое набухание этих клеток и нарушение их функций. Активное окисление этанола и ацетальдегида приводит к увеличению отношения NADH/NAD+, что снижает активность NAD+-зависимых ферментов в цитозоле и менее значительно в митохондриях. Равновесие следующей реакции смещается вправо: Дигидроксиацетонфосфат + NADH + Н+ ↔ Глицерол-3-фосфат + NAD+, Пируват + NADH + Н+ ↔ Лактат + NAD+. Восстановление дигидроксиацетонфосфата, промежуточного метаболита гликолиза и глюконеогенеза, приводит к снижению скорости глюконеогенеза. Образование глицерол-3-фосфата повышает вероятность синтеза жира в печени. Увеличение концентрации NADH по сравнению с NAD+ (NADH>NAD+) замедляет реакцию окисления лактата, увеличивается соотношение лактат/пируват и ещё больше снижается скорость глюконеогенеза. В крови возрастает концентрация лактата, это приводит к гиперлактацидемии и лактоацидозу. NADH окисляется ферментом дыхательной цепи NADH-дегидрогеназой. Возникновение трансмембранного электрического потенциала на внутренней митохондриальной мембране не приводит к синтезу АТФ в полном объёме. Этому препятствует нарушение структуры внутренней мембраны митохондрий, вызванное мемб-ранотропным действием этилового спирта и повреждающим действием ацетальдегида на мембраны. Можно сказать, что ацетальдегид опосредованно активирует ПОЛ, так как связывая SH-группы глутатиона, он снижает количество активного (восстановленного) глутатиона в клетке, который необходим для функционирования фермента глутатионпероксидазы, участвующего в катаболизме Н2О2. Накопление свободных радикалов приводит к активации ПОЛ мембран и нарушению структуры липидного бислоя. На начальных стадиях алкоголизма окисление ацетил-КоА в ЦТК - основной источник энергии для клетки. Избыток ацетил-КоА в составе цитрата выходит из митохондрий, и в цитоплазме начинается синтез жирных кислот. Этот процесс, помимо АТФ, требует участия NADPH, который образуется при окислении глюкозы в пентозофосфатном цикле. Из жирных кислот и глицерол-3-фосфата образуются ТАГ, которые в составе ЛПОНП секретируются в кровь. Повышенная продукция ЛПОНП печенью приводит к гипертриацилглицеролемии. При хроническом алкоголизме снижение синтеза фосфолипидов и белков в печени, в том числе и апобелков, участвующих в формировании ПОНП, вызывает внутриклеточное накопление ТАГ и ожирение печени. Однако в период острой алкогольной интоксикации, несмотря на наличие большого количества ацетил-КоА, недостаток оксалоацетата снижает скорость образования цитрата. В этих условиях избыток ацетил-КоА идёт на синтез кетоновых тел, которые выходят в кровь. Повышение в крови концентрации лактата, ацетоуксусной кислоты и β-гидроксибутирата служит причиной метаболического ацидоза при алкогольной интоксикации. Реакция образования ацетальдегида из этанола протекает под действием алкогольдегидрогеназы. Поэтому при повышении концентрации ацетальдегида и NADH в клетках печени направление реакции меняется - образуется этанол. Этанол - мембранотропное соединение, он растворяется в липидном бислое мембран и нарушает их функции. Это негативно отражается на трансмембранном переносе веществ, межклеточных контактах, взаимодействиях рецепторов клетки с сигнальными молекулами. Этанол может проходить через мембраны в межклеточное пространство и кровь и далее в любую клетку организма. Влияние этанола и ацетальдегида на метаболизм ксенобиотиков и лекарств в печени - Характер влияния этанола на метаболизм ксенобиотиков и лекарств зависит от стадии алкогольной болезни: начальная стадия алкоголизма, хронический алкоголизм или острая форма алкогольной интоксикации. Микросомальная этанолокисляющая сисгема (МЭОС) наряду с метаболизмом этанола участвует в детоксикации ксенобиотиков и лекарств. На начальной стадии алкогольной болезни биотрансформация лекарственных веществ протекает более активно вследствие индукции ферментов системы. Этим объясняют феномен лекарственной "устойчивости". Однако при острой интоксикации этиловым спиртом тормозится био-трансформация лекарственных веществ. Этанол конкурирует с ксенобиотиками за связывание с цитохромом Р450П E1, вызывая гиперчувствительность (лекарственную "неустойчивость") к некоторым принятым одновременно с ним лекарственным препаратам. Кроме того, у людей, страдающих хроническим алкоголизмом, наблюдают избирательную индукцию изоформы Р450II E1 и конкурентное ингибирование синтеза других изоформ, принимающих участие в метаболизме ксенобиотиков и лекарств. При злоупотреблении алкоголем индуцируется также синтез глюкуронилтрансфераз, но снижается образование УДФ-глюкуроната. Алкогольдегидрогеназа обладает широкой субстратной специфичностью и может окислять разные спирты, в том числе и метаболиты сердечных гликозидов - дигитоксина, дигоксина и гитоксина. Конкуренция этанола с сердечными гликозидами за активный центр алкогольдегидрогеназы приводит к снижению скорости биотрансформации этой группы лекарств и повышает опасность их побочного эффекта у лиц, принимающих большие дозы алкоголя. Повышение концентрации ацетальдегида вызывает целый ряд нарушений в структуре белков (ацетилирование), мембран (ПОЛ), модификацию глутатиона, необходимого для одного из самых важных ферментов обезвреживания ксенобиотиков - глутатионтрансферазы и фермента антиоксидазной защиты глутатионпероксидазы. Таким образом, представленные данные свидетельствуют, что алкогольное поражение печени сопровождается нарушением важнейшей функции этого органа - детоксикационной.
|
||||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 975; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.4.50 (0.01 с.) |

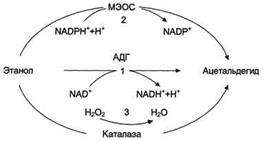 Катаболизм этилового спирта осуществляется главным образом в печени. Здесь окисляется от 75% до 98% введённого в организм этанола. Окисление алкоголя - сложный биохимический процесс, в который вовлекаются основные метаболические процессы клетки. Превращение этанола в печени осуществляется тремя путями с образованием токсического метаболита - ацетальдегида.
Катаболизм этилового спирта осуществляется главным образом в печени. Здесь окисляется от 75% до 98% введённого в организм этанола. Окисление алкоголя - сложный биохимический процесс, в который вовлекаются основные метаболические процессы клетки. Превращение этанола в печени осуществляется тремя путями с образованием токсического метаболита - ацетальдегида.


