Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Классическая антипиретическая терапияСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Авторы: Абатуров А.Е., Агафонова Е.А., Кривуша Е.Л., Петренко Л.Л. - ГУ «Днепропетровская медицинская академия Министерства здравоохранения Украины»; Абатурова Н.И. - КУ «Днепропетровская областная детская клиническая больница»; Днепропетровского областного совета
Резюме / Abstract В работе дано современное представление о механизмах развития лихорадки при инфекционных заболеваниях у детей, охарактеризованы побочные действия антипиретических средств, которые необходимо учитывать при дифференцированном выборе препарата. Обоснован выбор ибупрофена при лечении гипертермического синдрома у детей. У роботі дане сучасне уявлення про механізми розвитку лихоманки при інфекційних захворюваннях у дітей, охарактеризовано побічні дії антипіретичних засобів, які необхідно враховувати при диференційованому виборі препарату. Обґрунтовано вибір ібупрофену при лікуванні гіпертермічного синдрому в дітей. The paper presents a contemporary view on the mechanisms of fever development in infectious diseases in children, characterized adverse effects of antipyretic agents, which should be taken into consideration in differentiated selection of the preparation. The choice of ibuprofen in the treatment of hyperthermic syndrome in children is substantiated.
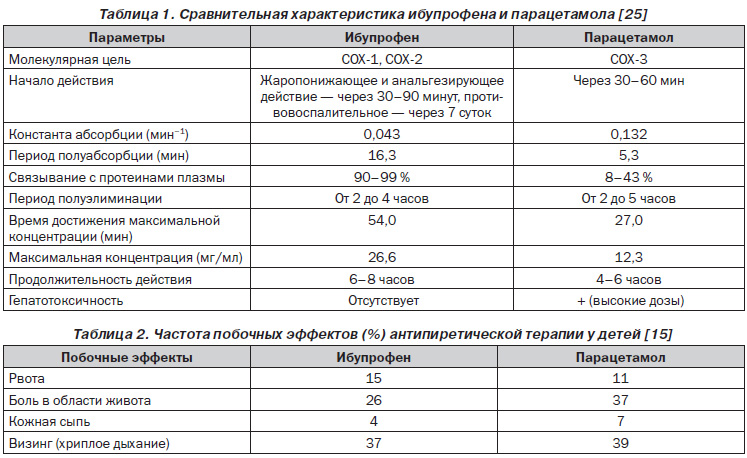
Ключевые слова / Key words жаропонижающая терапия, дети, ибупрофен. антипіретична терапія, діти, ібупрофен. antipyretic therapy, children, ibuprofen. Лихорадка является одним из самых надежных признаков большинства инфекционных заболеваний. Однако необходимо отметить, что лихорадочная реакция — это физиологический механизм, который оказывает саногенетическое влияние на процессы эрадикации инфекционных агентов. Повышение температуры тела до определенного уровня ингибирует рост и размножение бактерий, репликацию вирусов, способствует продукции острофазовых белков, пролиферации иммуноцитов [9, 10]. После появления доказательств наличия ассоциации между применением салицилатов и развитием синдрома Рейе парацетамол и ибупрофен заменили аспирин в качестве препарата выбора при симптоматической терапии больных с гипертермическим синдромом [8, 20, 21]. Точный механизм действия парацетамола остается неизвестным. Было сделано предположение, что парацетамол блокирует синтез PGE2 в гипоталамусе, ингибируя циклооксигеназу (СОХ)3, которая является продуктом сплайсмутированного гена СОХ1 [7]. Парацетамол не является эффективным противовоспалительным средством, так как не ингибирует синтез простагландинов за пределами центральной нервной системы. Парацетамол, принятый внутрь, быстро всасывается в тонком кишечнике и начинает действовать через 30–60 минут. Продолжительность действия разово принятой дозы парацетамола составляет около 4 часов [14, 24]. Назначение парацетамола в дозе от 10 до 15 мг/кг каждые 4–6 часов считается безопасным и эффективным. Таким образом, рекомендуемая суточная доза парацетамола для детей в среднем составляет 60–75 мг/кг, в то время как суточная доза — 90 мг/кг парацетамола, по мнению многих авторов, является супертерапевтической, иными словами, потенциально токсической дозой. Небольшой диапазон между терапевтической и потенциально токсической дозой парацетамола (менее 2 суточных доз, 90 мг/кг массы тела) является одним из неблагоприятных факторов и может приводить к развитию токсического эффекта при случайной передозировке. Использование ибупрофена, который обладает высоким порогом потенциально токсической дозы (до 10 суточных доз), позволяет избежать возникновения побочных эффектов при случайной передозировке. То есть прием препаратов ибупрофена не вызывает побочных реакций вследствие случайной передозировки [14, 24]. Парацетамол противопоказан детям с выраженными нарушениями функции печени и почек, дефицитом глюкозо6фосфатдегидрогеназы, высокой восприимчивостью к ацетаминофену. Одновременный прием парацетамола с барбитуратами, противоэпилептическими лекарственными средствами, рифампицином, алкоголем значительно повышает риск гепатотоксического действия парацетамола. Эффект гепатотоксичности связан с действием не самого парацетамола, а его нестабильного метаболита — Nацетилраминобензохинона (NAPQI), который инактивируется глутатионом. В норме лишь небольшая фракция парацетамола конвертируется в активный метаболит, который связывается с глутатионом и затем экскретируется в виде меркаптуровой кислоты. Большие дозы парацетамола приводят к повышенному образованию его активного метаболита — NAPQI. Когда истощаются запасы связывающего NAPQI глутатиона, этот метаболит ковалентно связывается с белками плазмы с образованием комплексов, вызывающих некроз. Таким образом, гепатотоксичность парацетамола зависит: от дозы препарата; скорости его трансформации; тканевых запасов глутатиона; обстоятельств или агентов, потенциально способных индуцировать соответствующее звено цитохрома Р450 или сокращать запасы глутатиона (например, прием противоэпилептических препаратов) [1]. Парацетамолиндуцированная гепатотоксичность ассоциирована с приемом доз, превышающих 150 мг/кг в сутки. Признаки парацетамолиндуцированной гепатотоксичности могут появиться не сразу, а через 4–6 дней. У детей парацетамолиндуцированное поражение печени составляет 25 % всех случаев острой печеночной недостаточности [12, 16]. Противопоказаниями к назначению парацетамола являются: повышенная индивидуальная чувствительность к компонентам препарата, гипербилирубинемия, дефицит глюкозо6фосфатдегидрогеназы, тяжелые нарушения функции печени и/или почек, нарушения со стороны системы кроветворения, в том числе анемия и лейкопения. Лечение парацетамолом может сопровождаться побочными эффектами: тошнотой, болями в эпигастрии, повышением активности печеночных ферментов, развитием анемии, в том числе гемолитической, агранулоцитоза, тромбоцитопении, панцитопении, метгемоглобинемии, анафилактоидной и других аллергических реакций (кожная сыпь, зуд, крапивница, мультиформная экссудативная эритема, токсический эпидермальный некролиз), снижением уровня глюкозы в крови вплоть до гипогликемической комы, возникновением бронхоспазма (отмечается преимущественно у пациентов с повышенной индивидуальной чувствительностью к нестероидным противовоспалительным препаратам (НПВП)), папиллярного некроза и интерстициального нефрита. Длительное применение высоких доз парацетамола может сопровождаться гепато и нефротоксическим действием [11, 13, 17, 18]. В 2008 году было проведено рандомизированное исследование, в котором проанализирована вероятность развития отдаленных эффектов терапии парацетамолом у 200 000 детей из 31 страны. Было установлено, что использование парацетамола как жаропонижающего средства ассоциировано с повышенным риском развития бронхиальной астмы (отношение шансов 1,46). Данная связь носит дозозависимый характер [5]. Также продемонстрирована вероятность наличия ассоциации между приемом парацетамола и риском последующего возникновения атопического дерматита [23]. Авторами проведено изучение влияния приема парацетамола на развитие аллергических заболеваний у 28 717 детей в возрасте от 13 до 14 лет. Было установлено, что использование парацетамола ассоциировано с увеличением распространенности аллергических процессов у детей. Показатель ассоциации для атопического дерматита составлял 1,81, аллергического ринита и бронхиальной астмы — 2,20 и 3,03 соответственно. Ибупрофен ингибирует активность СОХ1 и СОХ2 и, как следствие, синтез (не только в центральной нервной системе) простагландинов, участвующих в воспалительной реакции. Жаропонижающее, противовоспалительное и анальгезирующее действие ибупрофен реализует через центральное и периферическое ингибирование СОХ2. Подавление активности СОХ1 ассоциировано с развитием неблагоприятных эффектов. В отличие от парацетамола ибупрофен оказывает более длительное антипиретическое действие (до 8 часов), а уровень безопасности его применения не меньше, чем у парацетамола [2, 25]. Высокий профиль безопасности обусловливает широкое применение ибупрофена. Так, ибупрофен как жаропонижающее средство применяется в практической медицине не менее 80 стран мира. Принятый внутрь ибупрофен быстро всасывается в пищеварительном тракте и примерно через 30–90 минут начинает оказывать антипиретическое действие, которое длится от шести до восьми часов. Ибупрофен в периферическом русле крови связан с белками плазмы. Попадая в печень, ибупрофен метаболизируется при участии фермента CYP2C9. Ибупрофен назначают в разовой дозе 10 мг/кг, максимальная суточная доза составляет 30 мг/кг массы тела. Назначение ибупрофена противопоказано при эрозивноязвенных заболеваниях пищеварительного тракта в фазе обострения, тяжелой печеночной и почечной недостаточности, «аспириновой» бронхиальной астме, лейкопении, тромбоцитопении, нарушениях свертываемости крови, скотоме, амблиопии, нарушениях цветового зрения. Применение ибупрофена может иногда сопровождаться побочными эффектами: тошнотой, рвотой, развитием НПВПгастропатии, сухостью слизистых оболочек, изъязвлением слизистой оболочки десен, афтозным стоматитом, запором или диареей, нарушением функции печени, головной болью, сонливостью или тревожностью, раздражительностью, тахикардией, повышением артериального давления, острой почечной недостаточностью, полиурией, анемией, тромбоцитопенической пурпурой, агранулоцитозом, лейкопенией, психомоторным возбуждением, галлюцинациями, асептическим менингитом, нарушением слуха, обратимой токсической амблиопией [4, 6, 17]. Прием ибупрофена не связан с риском развития бронхиальной астмы, а назначение низких доз препарата (5 мг/кг) даже снижает риск ее возникновения [14]. Рекомендуют воздержаться от назначения ибупрофена у детей с обезвоживанием [19]. Сравнение некоторых характеристик ибупрофена и парацетамола представлено в табл. 1. Исследования, в которых проводилось сравнение антипиретической эффективности ибупрофена и парацетамола, показали, что оба препарата являются более эффективными, чем плацебо. Ибупрофен (в разовой дозе 10 мг/кг) характеризуется такой же, а возможно, и более высокой степенью эффективности, чем парацетамол (в разовой дозе 15 мг/кг) [3, 10, 21, 22].
Paul Little и соавт. [15] в 2013 году провели рандомизированное контролируемое исследование эффективности ибупрофена и парацетамола у 889 детей с острыми респираторными инфекциями, по результатам которого было сделано заключение о том, что ибупрофен, вероятно, более эффективен как жаропонижающее средство у детей, чем парацетамол. Авторами показано, что частота побочных эффектов при применении ибупрофена у детей ниже, чем при назначении парацетамола (табл. 2). Несмотря на небольшую разницу (ибупрофен — 0,96, парацетамол — 0,82) в эффективности лечения этими препаратами, авторы советуют при острых респираторных инфекциях применять препараты ибупрофена. В последнее время при гипертермическом синдроме достаточно широко применяются препараты производства компании «Польфарма» Ибуфен® Д, Ибуфен® Форте, содержащие в 5 мл суспензии 100 мг и 200 мг ибупрофена соответственно, и Ибуфен® Юниор, в желатиновой капсуле которого содержится 200 мг ибупрофена. Ибуфен® Д можно назначать детям с 3месячного возраста и с массой тела более 5 кг, Ибуфен® Форте — детям старше 1 года и с массой тела более 10 кг, Ибуфен® Юниор — детям старше 6 лет и с массой тела более 20 кг. Ибуфен® Д обеспечивает точность дозирования ибупрофена детям раннего возраста, Ибуфен® Форте — более высокий комплайенс приема детям с 1 года жизни, а особенность капсулы Ибуфен® Юниор — легкость приема препарата, отсутствие неприятных вкусовых ощущений и, соответственно, уверенность в эффективном и безопасном лечении. Интересна форма Ибуфен® Форте — единственная в Украине суспензия ибупрофена 200 мг/5 мл. Ребенку с лихорадкой необходимо принять вдвое меньший объем лекарственного средства, что позволяет увеличить готовность ребенка к приему лекарственных средств, обеспечивает более легкое проглатывание и уменьшает риск срыгивания. Таким образом, при проведении лечебных мероприятий, направленных на снижение интенсивности лихорадочной реакции у детей, рекомендуется назначение ибупрофена, который оказывает более эффективное и пролонгированное жаропонижающее действие (до 8 часов). По профилю безопасности ибупрофен не уступает, а возможно, и превосходит парацетамол, так как в отличие от последнего у ибупрофена нет токсических метаболитов.
Список литературы / References 1. Ивашкин В.Т., Фисенко В.П., Маевская М.В., Макарьянц М.Л. Основные принципы метаболизма лекарств и безопасное применение парацетамола // http://www.provisor.com.ua/archive/1999/N21/ivashkin.php. 2. Allan G.M., Ivers N., Shevchuk Y. Treatment of pediatric fever: Are acetaminophen and ibuprofen equivalent? // Can. Fam. Physician. — 2010 Aug. — 56(8). — 773. PMC2920778. 3. Argentieri J., Morrone K., Pollack Y. Acetaminophen and Ibuprofen overdosage // Pediatr. Rev. — 2012 Apr. — 33(4). — 1889. doi: 10.1542/pir.334188. 4. AutretLeca E., BensoudaGrimaldi L., Maurage C., JonvilleBera A.P. Upper gastrointestinal complications associated with NSAID’s in children // Therapie. — 2007. — 62(2). — 173176. 5. Beasley R. Association between paracetamol use in infancy and childhood, and risk of asthma, rhinoconjunctivitis, and eczema in children aged 6–7 years: analysis from Phase Three of the ISAAC programme / R. Beasley, T. Clayton, J. Crane, E. von Mutius, C.K. Lai, S. Montefort, A. Stewart; ISAAC Phase Three Study Group // Lancet. — 2008, Sep 20. — 372(9643). — 103948. doi: 10.1016/S01406736(08)614452. 6. Bianciotto M. Drug use and upper gastrointestinal complications in children: a casecontrol study / M. Bianciotto, E. Chiappini, I. Raffaldi, C. Gabiano, P.A. Tovo, S. Sollai, M. de Martino, F. Mannelli, V. Tipo, R. Da Cas, G. Traversa, F. MennitiIppolito // Arch. Dis. Child. — 2013 Mar. — 98(3). — 21821. doi: 10.1136/archdischild2012302100. 7. Botting R., Ayoub S.S. COX3 and the mechanism of action of paracetamol/acetaminophen // Prostaglandins Leukot. Essent. Fatty Acids. — 2005 Feb. — 72(2). — 857. doi.org/10.1016/j.plefa.2004.10.005. 8. Chiappini E. Update of the 2009 Italian Pediatric Society Guidelines about management of fever in children / E. Chiappini, E. Venturini, N. Principi, R. Longhi, P.A. Tovo, P. Becherucci, F. Bonsignori, S. Esposito, F. Festini, L. Galli, B. Lucchesi, A. Mugelli, M. de Martino // Clin. Ther. — 2012 Jul. — 34(7). — 16481653.e3. doi: 10.1016/j.clinthera.2012.06.011. 9. ElRadhi A.S. Why is the evidence not affecting the practice of fever management? // Arch. Dis. Child. — 2008. — 93(11). — 918920. 10. Goldman R.D., Ko K., Linett L.J., Scolnik D. Antipyretic efficacy and safety of ibuprofen and acetaminophen in children // Ann. Pharmacother. — 2004. — 38(1). — 146150. 11. http://www.piluli.kharkov.ua/drugs/drug/panadol/ 12. Jefferies S., Saxena M., Young P. Paracetamol in critical illness: a review // Crit. Care Resusc. — 2012 Mar. — 14(1). — 7480. 13. Kang L.W. Severe anaphylactic reaction to ibuprofen in a child with recurrent urticaria / L.W. Kang, M.I. Kidon, C.W. Chin, L.S. Hoon, C.Y. Hwee, N.K. Chong // Pediatrics. — 2007 Sep. — 120(3). — e7424. doi: 10.1542/peds.20062634. 14. Lesko S.M., Mitchell A.A. An assessment of the safety of pediatric ibuprofen. A practitionerbased randomized clinical trial // JAMA. — 1995, Mar 22–29. — 273(12). — 92933. doi:10.1001/jama.1995.03520360043037. 15. Little P. Ibuprofen, paracetamol, and steam for patients with respiratory tract infections in primary care: pragmatic randomised factorial trial / P. Little, M. Moore, J. Kelly, I. Williamson, G. Leydon, L. McDermott, M. Mullee, B. Stuart; PIPS Investigators // BMJ. — 2013, Oct 25. — 347. — f6041. doi: 10.1136/bmj.f6041. 16. Mahadevan S.B., McKiernan P.J., Davies P., Kelly D.A. Paracetamol induced hepatotoxicity // Arch. Dis. Child. — 2006 Jul. — 91(7). — 598603. doi: 10.1136/adc.2005.076836. 17. McGill M.R. The mechanism underlying acetaminopheninduced hepatotoxicity in humans and mice involves mitochondrial damage and nuclear DNA fragmentation / M.R. McGill, M.R. Sharpe, C.D. Williams, M. Taha, S.C. Curry, H. Jaeschke // J. Clin. Invest. — 2012, Apr 2. — 122(4). — 157483. doi: 10.1172/JCI59755. 18. Miller A.L. Liver damage from chronic acetaminophen dosing is dangerous, but not the only risk // Altern. Med. Rev. — 2009 Dec. — 14(4). — 3223. 19. Moghal N.E., Hegde S., Eastham K.M. Ibuprofen and acute renal failure in a toddler // Arch. Dis. Child. — 2004 Mar. — 89(3). — 2767. doi: 10.1136/adc.2002.024141. 20. Pereira G.L., Tavares N.U., Mengue S.S., Dal Pizzol T.S. Therapeutic conducts and alternating antipyretics in the management of fever in children // J. Pediatr. (Rio J.). — 2012, Dec 28. doi.org/10.2223/JPED.2239. 21. Pierce C.A., Voss B. Efficacy and safety of ibuprofen and acetaminophen in children and adults: a metaanalysis and qualitative review // Ann. Pharmacother. — 2010 Mar. — 44(3). — 489506. doi: 10.1345/aph.1M332. 22. Southey E.R., SoaresWeiser K., Kleijnen J. Systematic review and metaanalysis of the clinical safety and tolerability of ibuprofen compared with paracetamol in paediatric pain and fever // Curr. Med. Res. Opin. — 2009 Sep. — 25(9). — 220722. doi: 10.1185/03007990903116255. 23. SuarezVarela M.M. Is acetaminophen use associated with atopic eczema and other allergic diseases in adolescents? / M.M. SuarezVarela, L. GarciaMarcos, J.F. FernandezEspinar et al. // Iran J. Allergy Asthma Immunol. — 2013, May 15. — 12(2). — 11523. 24. Sullivan J.E., Farrar H.C. Fever and antipyretic use in children // Pediatrics. — 2011 Mar. — 127(3). — 5807. doi: 10.1542/peds.20103852. 25. Tucci J. Paracetamol and Ibuprofen for Paediatric Pain and Fever / J. Tucci, E. Bandiera, R. Darwiche, Z. Medos, R. Nashed, D. Trinh // J. Pharmacy Practice and Research. — 2009. — 39(3). — 223225.
|
||||
|
Последнее изменение этой страницы: 2016-06-26; просмотров: 410; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.63.107 (0.008 с.) |