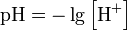Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Соотношение между степенью диссоциации и концентрации слабых электролитовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Принцип Паули В атоме не могут одновременно находиться два электрона с одинаковым набором четырех квантовых квантовых чисел (заполнение электронами орбиталей происходит следующим образом: сначала на каждой орбитали располагается по одному электрону, затем, после заполнения всех орбиталей происходит распределение вторых электронов с противоположным спином). Правило Хунда При данном значении квантового числа 1 (т.е. в пределах одного подуровня) в основном состоянии электроны располагаются таким образом, что значение суммарного спина атома максимально. Это означает, что на подуровне должно быть максимально возможное число неспаренных электронов. S-, p-, d-, f- элементы В зависимости от состояния электронов в атомах различают s-, p-, d-, f-орбитали и соответствующие им s-, p-, d-, f-подуровни. В зависимости от того, какой подуровень (s, p, d или f) заполняет очередной электрон, соответственно различают s-, p-, d- или f-элементы. В главных подгруппах ПСХЭ Д.И.Менделеева находятся s- и р-элементы, а в побочных подгруппах – d- и 2. Слабые электролиты — химические соединения, молекулы которых даже в сильно разбавленных растворах незначительно диссоциированны на ионы, которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым электролитам относится большинство органических кислот и многие органические основания в водных и неводных растворах. Слабыми электролитами являются:
Закон разбавления Оствальда Закон разбавления Оствальда — соотношение, выражающее зависимость эквивалентной электропроводности разбавленного раствора бинарного слабого электролита от концентрации раствора:
Здесь К — константа диссоциации электролита, с — концентрация, λ и λ∞ — значения эквивалентной электропроводности соответственно при концентрации с и при бесконечном разбавлении. Соотношение является следствием закона действующих масс и равенства
где α — степень диссоциации.
Соотношение между степенью диссоциации и концентрации слабых электролитов
ά ≈ √К/С
Это уравнение показывает связь между концентрацией слабого электролита и степенью его диссоциации, а именно степень диссоциации возрастает при разбавлении раствора.
3.
4HNO3 (разб.) + Fe = Fe(NO3)3 + NO↑ + 2H2O 2NaAlO2+4H2SO4=Al2(SO4)3+Na2SO4+4H2O не уверен
№3 Окислитенельно-восстановительные реакции ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕРЕАКЦИИ (р-ции окисления-восстановления) происходят с изменением степени окисления атомов, входящих в состав реагирующих в-в. При окислении в-в степень окисления элементов возрастает, при восстановлении - понижается.
Типичные окислители и восстановители Вещества, являющиеся окислителями во многих реакциях, представляют собой типичные (сильные) окислители. К ним относятся F2, Cl2, O2, KClO3, H2SO4, HNO3, KMnO4, MnO2, K2Cr2O7, PbO2 и др.
Типичными (сильными) восстановителями являются H2, C (графит), Zn, Al, Ca, KI, HCl (конц.), H2S, CO и др.
Соединения с двойственной функцией Многие вещества могут проявлять как окислительные, так и восстановительные свойства. К таким веществам принадлежат KNO2, H2O2, SO2, Nа2SO3 и др.
2. Принцип Ле Шателье Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, стремящиеся свести это изменение к минимуму.
Смещение химического равновесия при изменении: Концентрации
Давления При повышении давления равновесие сдвигается в направлении, в котором уменьшается суммарное количество молей газов и наоборот. В реакции синтеза аммиака количество газов уменьшается вдвое: N2 + 3H2 ↔ 2NH3 Значит, при повышении давления равновесие смещается в сторону образования NH3 Температура При повышении температуры химическое равновесие смещается в направлении эндотермической реакции, при понижении температуры — в направлении экзотермической реакции.
3. KMnO4 + H2S + HCl→ MnCl2 + S + KCl + H2O K2CO3 + H2O = KHCO3 + KOH
№5 1. Метод валентных связей Основные положения метода валентных связей, базирующиеся на квантово-механической теории строения атома, были разработаны Вальтером Гейтлером и Фритцем Лондоном в 1928 году. В последующем значительный вклад в развитие этого метода внесли Лайнус Полинг и Джон Слейтер. С точки зрения этого метода: 1. В образовании связи участвуют только электроны внешней электронной оболочки атома (валентные электроны). 2. Химическая связь образуется двумя валентными электронами различных атомов с антипараллельными спинами. При этом происходит перекрывание электронных орбиталей и между атомами появляется область с повышенной электронной плотностью, обусловливающая связь между ядрами атомов. Таким образом, в основе МВС лежит образование двухэлектронной, двухцентровой связи. 3. Химическая связь осуществляется в том направлении, в котором обеспечивается наибольшее перекрывание атомных орбиталей. 4. Из нескольких связей данного атома наиболее прочной будет связь, которая получилась в результате наибольшего перекрывания атомных орбиталей. 5. При образовании молекул электронная структура (кроме внешней электронной оболочки) и химическая индивидуальность каждого атома в основном сохраняются. Валентность Валентность (от лат. valentia - сила), способность атома к образованию химических связей. 2. Термохимическое уравнение
Термохимические уравнения реакций - это уравнения, в которых около символов химических соединений указываются агрегатные состояния этих соединений или кристаллографическая модификация и в правой части уравнения указываются численные значения тепловых эффектов Например, термохимическое уравнение 4NH3(г) + 3O2(г) → 2N2(г) + 6H2O(ж), ΔН=-1531 кДж показывает, что данная химическая реакция сопровождается выделением 1531 кДж теплоты, при давлении 101 кПа, и относится к тому числу молей каждого из веществ, которое соответствует стехиометрическому коэффициенту в уравнении реакции.
Константа скорости реакции. Константа скорости реакции — коэффициент пропорциональности в кинетическом уравнении.
Константа скорости реакции имеет физический смысл скорости реакции, когда произведение концентраций реагирующих веществ равно единице.
Константа скорости реакции зависит от температуры, от природы реагирующих веществ, но не зависит от их концентрации. Обменный механизм К обменному механизму образования химической связи относят случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону.
Показать на любом примере (Допустим HCl)
Произведение растворимости Произведение концентраций ионов в насыщенном растворе малорастворимого электролита представляет собой величину постоянную при данной температуре.
Комплексные соединения Комплексные соединения содержат катионный, анионный или нейтральный комплекс, состоящий из центр. атома (или иона) и связанных с ним молекул или ионов - лигандов. Центр. атом (комплексообразователь) - обычно акцептор, а лиганды - доноры электронов, и при образовании комплекса между ними возникает донорно-акцепторная, или координационная, связь.
Внутренняя сфера комплексного соединения — центральный атом со связанными с ним лигандами, то есть, собственно, комплексная частица.
Внешняя сфера комплексного соединения — остальные частицы, связанные с комплексной частицей ионной или межмолекулярными связями, включая водородные.
Центральный атом с окружающими его лигандами образуют внутреннюю сферу комплекса. Ее обычно заключают в квадратные скобки. Все остальное в комплексном соединении составляет внешнюю сферу и пишется за квадратными скобками.
ЛИГАНДЫ (от лат. ligo - связываю), нейтральные молекулы, ионы или радикалы, связанные с центр. атомом комплексного соединения. Ими м. б. ионы (Н-, Наl-, NO3-, NCS- и др.), неорг. молекулы (Н2, Сn, N2, Рn, О2, Sn, СО, СО2, NH3, NO, SO2, NO2, COS и др.), орг. соед., содержащие элементы главных подгрупп V, VI, VII гр. периодич. системы или p-донорную ф-цию.
Важнейшая количеств. характеристика донорно-акцепторной способности лигандов - дентатность, определяемая числом донорных центров лигандов, участвующих в координации.
Координационное число (КЧ) — число связей, образуемых центральным атомом с лигандами. Для комплексных соединений с монодентантными лигандами КЧ равно числу лигандов, а в случае полидентантных лигандов — числу таких лигандов, умноженному на дентатность.
Наиб. распространенные координационные числа - 4 и 6, но известно много комплексов, центр. атом к-рых имеет координационные числа 2, 3, 5, 7, 8 и более.
Геометрическая конфигурация Геометрическая конфигурация строения внутренней сферы комплексов бывает различной: линейная, треугольная, квадратная, тетраэдрическая, октаэдрическая, пирамидальная, бипирамидальная и т.д., в зависимости от природы центрального атома металла, лигандов, внешнесферного окружения. Структура комплексов экспериментально обычно устанавливается рентгеноструктурным и спектральными методами.
Оптическая изомерия Оптическая изомерия связана со способностью некоторых комплексных соединений существовать в виде двух форм, не совмещаемых в трехмерном пространстве и являющихся зеркальным отображением друг друга, как левая рука и правая. Поэтому оптическую изомерию называют иногда ещё зеркальной изомерией. Структурная изомерия Гидратная (сольватная) изомерия заключается в различном распределении молекул растворителя между внутренней и внешней сферами комплексного соединения, в различном характере химической связи молекул воды с комплексообразователем. Классическим примером гидратной изомерии является существование трех изомерных гидратов хлорида хрома(III) с общей формулой CrCl3. 6 H2O.
Ионная изомерия
Ионизационная изомерия определяется различным распределением заряженных лигандов между внутренней и внешней сферами комплекса и характеризует способность координационных соединений с одним и тем же элементным составом давать в растворе разные ионы. Пример ионных изомеров – бромид дихлоротетраамминплатины(IV) и хлорид дибромотетраамминплатины(IV): [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 Координационная изомерия Координационная изомерия связана с переходом лигандов от одного комплексообразователя к другому: [Co(NH3)6][Cr(CN)6] и [Cr(NH3)6][Co(CN)6]. 2. Вода Вода́ (оксид водорода) — химическое вещество в виде прозрачной жидкости, не имеющей цвета (в малом объёме), запаха и вкуса (при стандартных условиях). Химическая формула: Н2O. Водородный показатель Водоро́дный показа́тель, pH — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр:
Например, концентрация ионов водорода [H+] равна 10^-5 моль/л, то lg10^-5 = -5, a –lg10^-5 = 5 (^ это значит, что в степени). Значит, pH = 5
На всякий случай, pH + pOH=14 ==> pOH = 14 -5 = 9
Водородная связь Водородная связь, вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом (А). Группа А — Н выступает донором протона (акцептором электрона), а другая группа (или атом) В — донором электрона (акцептором протона). Иначе говоря, группа А — Н проявляет функцию кислоты, а группа В — основания. Для обозначения водородной связи употребляют, в отличие от обычной валентной чёрточки, пунктир, т. е. А — Н···В Наиболее известный пример соединения с водородной связью-это вода.
3. H2S + 2HNO3 = S + 2NO2 (NO) + 2H2O (не уверен) BaCO3 + H2SO4 = BaSO4 + CO2 + H2O №19 1. Вставные декады Элементы побочных подгрупп образуют вставные декады: это Sc-Zn; Y-Cd; La-Hf-Hg; начало четвертой вставной декады Ас - в незавершенном седьмом периоде. Элементы этих декад называют d - элементами. Группа химических элементов, у которых происходит заполнение электронных оболочек d - электронами; в виде простых тел являются металлами. Концентрация Как правило, увеличение концентрации или давления (для реакций с участием газов) реагентов приводит к повышению скорости реакции. Температура Изменение температуры оказывает резкое влияние на константу скорости, а следовательно, и на скорость химической реакции. В подавляющем большинстве случаев скорость химической реакции с нагреванием возрастает. Катализаторы Катализаторами называют вещества, которые влияют на скорость реакции, но сохраняют свой химический состав после промежуточных реакций. Катализаторы, которые ускоряют реакцию, называют положительными, которые замедляют – отрицательными. Принцип Паули В атоме не могут одновременно находиться два электрона с одинаковым набором четырех квантовых квантовых чисел (заполнение электронами орбиталей происходит следующим образом: сначала на каждой орбитали располагается по одному электрону, затем, после заполнения всех орбиталей происходит распределение вторых электронов с противоположным спином). Правило Хунда При данном значении квантового числа 1 (т.е. в пределах одного подуровня) в основном состоянии электроны располагаются таким образом, что значение суммарного спина атома максимально. Это означает, что на подуровне должно быть максимально возможное число неспаренных электронов. S-, p-, d-, f- элементы В зависимости от состояния электронов в атомах различают s-, p-, d-, f-орбитали и соответствующие им s-, p-, d-, f-подуровни. В зависимости от того, какой подуровень (s, p, d или f) заполняет очередной электрон, соответственно различают s-, p-, d- или f-элементы. В главных подгруппах ПСХЭ Д.И.Менделеева находятся s- и р-элементы, а в побочных подгруппах – d- и 2. Равновесие в насыщенных растворах малорастворимых электролитов (солей) <---- твердая раствор
Энергия активации ЭНЕРГИЯ АКТИВАЦИИ в элементарных р-циях, миним. энергия реагентов (атомов, молекул и др. частиц), достаточная для того, чтобы они вступили в хим. р-цию, т. е. для преодоления барьера на поверхности потенциальной энергии, отделяющего реагенты от продуктов р-ции. Потенциальный барьер - максимум потенциальной энергии, через который должна пройти система в ходе элементарного акта хим. превращения. Уравнение Аррениуса:
k = A e– E a/ RT
k — константа скорости реакции, R – универсальная газовая постоянная, T – температура в кельвинах, Еа -энергия активации, A – Предэкспоненциальный коэффициент, связанный с вероятностью и числом столкновений, е – основание натуральных логарифмов.
Из этого уравнения видно, что чем больше энергия активации, тем меньше константа скорости реакции, т.е. тем меньше скорость реакции. 3. 5H2SO4(конц.) + 8KI(т) = H2S↑ + 4I2↓ + 4H2O + 4K2SO4 3NaOH(конц.) + H3PO4 = Na3PO4 + 3H2O Принцип Паули В атоме не могут одновременно находиться два электрона с одинаковым набором четырех квантовых квантовых чисел (заполнение электронами орбиталей происходит следующим образом: сначала на каждой орбитали располагается по одному электрону, затем, после заполнения всех орбиталей происходит распределение вторых электронов с противоположным спином). Правило Хунда При данном значении квантового числа 1 (т.е. в пределах одного подуровня) в основном состоянии электроны располагаются таким образом, что значение суммарного спина атома максимально. Это означает, что на подуровне должно быть максимально возможное число неспаренных электронов. S-, p-, d-, f- элементы В зависимости от состояния электронов в атомах различают s-, p-, d-, f-орбитали и соответствующие им s-, p-, d-, f-подуровни. В зависимости от того, какой подуровень (s, p, d или f) заполняет очередной электрон, соответственно различают s-, p-, d- или f-элементы. В главных подгруппах ПСХЭ Д.И.Менделеева находятся s- и р-элементы, а в побочных подгруппах – d- и 2. Слабые электролиты — химические соединения, молекулы которых даже в сильно разбавленных растворах незначительно диссоциированны на ионы, которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым электролитам относится большинство органических кислот и многие органические основания в водных и неводных растворах. Слабыми электролитами являются:
Закон разбавления Оствальда Закон разбавления Оствальда — соотношение, выражающее зависимость эквивалентной электропроводности разбавленного раствора бинарного слабого электролита от концентрации раствора:
Здесь К — константа диссоциации электролита, с — концентрация, λ и λ∞ — значения эквивалентной электропроводности соответственно при концентрации с и при бесконечном разбавлении. Соотношение является следствием закона действующих масс и равенства
где α — степень диссоциации.
Соотношение между степенью диссоциации и концентрации слабых электролитов
ά ≈ √К/С
Это уравнение показывает связь между концентрацией слабого электролита и степенью его диссоциации, а именно степень диссоциации возрастает при разбавлении раствора.
3.
4HNO3 (разб.) + Fe = Fe(NO3)3 + NO↑ + 2H2O 2NaAlO2+4H2SO4=Al2(SO4)3+Na2SO4+4H2O не уверен
№3
|
||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 786; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.116.61 (0.009 с.) |