Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физико-химические методы анализа никеляСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
КУРСОВАЯ РАБОТА по дисциплине
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА НИКЕЛЯ Выполнила Студент гр.320601 Елисеева А.И.
Проверила кан. хим. наук Пастушенко В.Г Содержание
I. Общие методы анализа алюминия. Алюминий………………………………………………………………………………3 Алюминий в природе………………………………………………………………….3 1. Фотометрический метод анализа. 1.1 Фотометрический метод с экстракцией гидроксихинолята алюминия..............3 2. Комплексонометрический метод анализа. 2.1 Сущность метода…………………………………………………...………….....5 2.2 Реактивы и растворы……………………………………………………………..5 2.3 Проведение анализа……………………………………………………………....5 3. Определение малых концентраций алюминия …………………………..….6 4. Титриметрический метод анализа. 4.1 Сущность метода …………………………………………………..…………….7 4.2 Реактивы и растворы……………………………………………………………..7 4.3 Проведение анализа 4.3.1 Для сплава куниаль 4.3.1.1 Определение с визуальной индикацией конечной точки титрования …...8 4.3.2 Для сплава алюмель 4.3.2.1 Определение с визуальной индикацией конечной точки титрования…....8 4.3.3 Обработ к а результатов…………………………………………………….....9 II. Атомно-абсорбционный анализ алюминия. 1. Сущность метода………………………………………………………………….9 2. Аппаратура, реактивы и растворы ……………………………………………..12 3. Проведение анализа….…………………………………………………………...16 4. Обработка результатов …………………………………………………………..19 III. Индивидуальное задание ……………………………………………………….21 1. Методом калибровочного графика……………………………………………...21 2. Методом сравнения……………………………………………………………….22 3. Методом добавок………………………………………………………………….23 I Общие методы анализа алюминия. Алюми́ний — элемент главной подгруппы третьей группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 13. Обозначается символом Al (лат. Aluminium). Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости химический элемент в земной коре (после кислорода и кремния). Простое вещество алюминий — лёгкий, парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия. Алюминий в природе. Природный алюминий состоит практически полностью из единственного стабильного изотопа 27Al со следами 26Al, радиоактивного изотопа с периодом полураспада 720 тыс. лет, образующегося в атмосфере при бомбардировке ядер аргона протонами космических лучей. По распространённости в земной коре Земли занимает 1-е среди металлов и 3-е место среди элементов, уступая только кислороду и кремнию. Процент содержания алюминия в земной коре по данным различных исследователей составляет от 7,45 до 8,14 % от массы земной коры Фотометрический метод анализа. Фотометрический метод с экстракцией гидроксихинолята алюминия Сущность метода: Метод основан на том, что гидроксихинолят количественно экстрагируется хлороформом в слабокислой среде (рН == 4,35-4,5), окрашивая хлороформный слой в желто-зеленый цвет. Измерение проводят при к = 387--400 нм, молярный коэффициент поглощения имеет значения соответственно от 6,4 * 10-3 до 5-10-3.
Мешающие вещества. Мешающее определению железо (II) предварительно окисляют до трехвалентного и извлекают хлороформом в более кислой среде (рН = 1,7-2,0). Приборы и реактивы. Соляная кислота, 1 н. раствор. Гидроксихинолин, 2%-ный раствор в хлороформе, Стандартный раствор соли алюминия. Растворяют 1,759 t алюмокалиевых квасцов чда в дистиллированной воде и разбавляют раствор до 1 л; 1 мл полученного раствора содержит 0,1 мг алюминия. При определении очень малых количеств алюминия применяют в 10 раз более разбавленный раствор, в 1 мл которого содержится 0,01 мг алюминия. Персульфат аммония. Ход определения. Отбирают такой объем анализируемой пробы, чтобы в нем содержалось от 5 до 200 мкг алюминия. Если, надо, разбавляют дистиллированной водой до 25-50 мл, прибавляют немного (на кончике ножа) персульфата аммония, перемешивают до растворения и дают раствору постоять несколько минут. Переносят раствор в делительную воронку и нейтрализуют 0,1 н. кислотой или щелочью. Необходимое для нейтрализации количество кислоты или щелочи находят, титруя отдельную порцию анализируемой воды по метиловому оранжевому. Затем подкисляют раствор, добавляя 0,4 мл соляной кислоты на каждые 25 мл раствора (после подкисления рН раствора; должен быть 1,7-1,95), приливают 1,5-2 мл раствора 8-гидроксихинолина в хлороформе, сильно встряхивают, оставляют до разделения слоев и сливают окрашенный оксихинолятом железа нижний слой.
Извлечение железа из раствора повторяют еще раз, прибавляя вторую такую же порцию раствора 8-гидроксихинолина в хлорозной форме. Если содержание железа меньше 8 мг/л, как это обычно бывает, при втором экстрагировании получается очень бледно окрашенный слой хлороформа, и в этом случае двумя экстракциями можно ограничиться.
При большем содержании железа экстрагирование продолжают, добавляя новые порции хлороформного раствора до получения бесцветного экстракта.
К раствору, не содержащему железа, приливают 2,5-3,0 мл раствора 8-гидроксихинолина в хлороформе, 10 мл ацетатного буферного раствора (рН = 4,5) и, энергично встряхивая, извлекают оксихинолят алюминия. При указанном выше содержании алюминия практически полное извлечение его достигается одной экстракцией. Дают постоять 1-2 мин для разделения слоев и затем переносят нижний, окрашенный в желто-зеленый цвет, слой хлороформа в кювету фотометра и измеряют оптическую плотность при λ = 387-400 нм.
Определение малых концентраций алюминия Для определения алюминия, находящегося в растворе в малых концентрациях, предложено большое число фотометрических методов. Большинство из них (например, методы с применением алюминона, ализаринсульфоната), основано на образовании коллоидных окрашенных растворов (лаков) соединений этих реагентов с алюминием. Поскольку как интенсивность получаемых окрасок, так и оттенки их зависят от степени дисперсности образующихся коллоидных частиц лаков, а последняя в свою очередь зависит от многих факторов (присутствия различных солей в растворе и их концентраций, температуры, скорости влияния реактива и т. д.), методы эти нами не рекомендуются. Истинные растворы окрашенных веществ получаются при применении двух фотометрических методов, описанных ниже. Для сплава куниаль Определение с визуальной индикацией конечной точки титрования Навеску сплава массой 0,25 г помешают в коническую колбу вместимостью 500 см3, добавляют 10 см3 азотной кислоты и растворяют при нагревании. После растворения сплава стенки колбы ополаскивают водой и раствор кипятят 1—2 мин для удаления окислов азота. Раствор охлаждают, добавляют 10 см* раствора мочевины и нейтрализуют раствором аммиака до образования неисчезающего осадка, который растворяют добавлением соляной кислоты. После чего прибавляют еще две капли кислоты, добавляют 20 см1 раствора трилона Б, 100 см3 горячей воды. Для сплава алюмель Определение с визуальной индикацией конечной точки титрования Навеску сплава массой 0,25 г помещают в платиновую чашку, добавляют 10 см3 азотной кислоты, 2—3 см3 фтористоводородной кислоты, накрывают крышкой из фторопласта или платины н растворяют при нагревании. После растворения сплава крышку и стенки чашки ополаскивают водой, добавляют 10 см3 серной кислоты (1:1) и упаривают до начала выделения белого дыма серной кислоты. Охлажденный остаток растворяют в 50 см3 воды при нагревании. Раствор переносят в коническую колбу вместимостью 500 см* и нейтрализуют раствором аммиака до образования неисчезающего осадка, который растворяют добавлением соляной кислоты. после чего прибавляют еще две капли кислоты. Обработка результатов 2.4.1. Массовую долю алюминия (X) в процентах вычисляют по формуле
где V — обьем раствора меди, израсходованный на второе титрование, см3; Т — массовая концентрация раствора меди, выраженная в г/см3 алюминия; m — масса навески сплава, г.
Сущность метода анализа. Метод основан на измерении атомной абсорбции алюминия в пламени закись азота ацетилен при длине волны 309,3 нм. Атомизацию проводят из солянокислых растворов. 1. Сущность метода анализа заключается в обработке проб почвы при комнатной температуре дистиллированной водой и определении в полученном, растворе водорастворимых соединений металлов атомно-абсорбционным анализом. 2. Метод атомно-абсорбционного анализа основан на свойстве атомов металлов поглощать в основном состоянии свет определенных длин волн, который они испускают в возбужденном состоянии. Необходимую для поглощения резонансную линию чаще всего получают от лампы с полым катодом, изготовленным из определяемого элемента. В атомно-абсорбционной спектроскопии, так же как и в молекулярной, допускает закон Ламберта-Бугера-Бера: А = k · C где А - величина, характеризующая поглощение света (оптическая плотность, абсорбция), мБ или %; k - коэффициент поглощения; С - концентрация определяемого элемента, мкг/мл.
Величина поглощения света пропорциональна содержанию определяемых элементов, на чем и основано их количественное определение.
3. Блок-схема атомно-абсорбционного спектрофотометра.
1 – источник питания; 2 – лампа с полым катодом; 3 – пламя (зона атомизации); 4 – монохроматор; 5 – фотоумножитель; 6 – усилитель; 7 – гальванометр; 8 – распылитель; 9 – анализируемый раствор.
Анализируемый раствор 9 в виде аэрозоля из распылителя 8 вводят в пламя горелки 3 (пламя ацетилен-воздух, температура от 2000 до 3000 °С). В пламени происходит испарение растворителя, плавление и испарение пробы почвы, термическая диссоциация молекул и образование свободных атомов, которые могут поглощать излучение внешнего источника света 2. Световой поток от лампы проходит через пламя горелки 3 и монохроматор 4. Монохроматор выделяет узкую спектральную линию (обычно 0,2-2,0 нм), в которой находится измеряемая спектральная линия определяемого элемента. Атомы исследуемого элемента поглощают световой поток лампы. Выходящий световой поток с помощью фотоумножителя 5 превращается в электрический сигнал и после усилителя 6 регистрируется гальванометром 7. 4. Оптимизация аппаратурных условий атомно-абсорбционного анализа. Оптимизации подлежат: а) ток лампы; б) рабочая высота пламени; в) соотношение горючего газа и окислителя; г) ширина спектральной щели.
а) При увеличении тока лампы (но не более максимального) улучшается воспроизводимость, но уменьшается время жизни лампы, особенно для легколетучих элементов. Поэтому высокие токи лампы следует применять при очень низких концентрациях вблизи предела обнаружения, вызывающего абсорбцию, эквивалентную двойной флуктуации фона.
б) Оптимальная высота пламени для воздушно-ацетиленового пламени 5-13 мм.
в) Соотношение горючее/окислитель влияет на окислительно-восстановительные свойства пламени, на его собственное поглощение и эмиссию. Легкоатомизирующиеся элементы (медь, свинец, цинк, никель, кадмий, кобальт, марганец) определяются в окислительном воздушно-ацетиленовом пламени, которое обычно более прозрачно, характеризуется меньшими шумами и боолее высокой температурой. Хром определяется в восстановительном воздушно-ацетиленовом пламени. Оптимальное давление и расход окислителя и восстановителя зависят от конструкции распылителя и обычно указаны фирмой - изготовителем прибора. г) Спектральная ширина щели составляет 0,1-2,0 нм. Как правило, используют максимальную спектральную ширину щели, при которой меньше дрейф установленной длины волны и в спектральный интервал не попадают посторонние линии. При наличии в спектре источника линий, близких к резонансной, следует работать с малой спектральной шириной щели. Так, для меди рекомендуемая ширина спектральной щели - 0,7 нм, для цинка - 0,7-2,0 нм, для никеля - 0,1-0,2 нм.
Оборудование, материалы. Шкаф сушильный лабораторный типа Аквадистиллятор типа ДЭ-4-2 – 1 шт. Аппарат для бидистилляции воды типа БД-2 – по ТУ 25-11-1102 – 1шт. Ступки с пестиком - 3 шт. Фильтры обеззоленные с "белой лентой" - 1000 шт Колбы конические плоскодонные вместимостью 250 мл - 40 шт. Стеклянные воронки диаметром 60-80 мм - 50 шт Стаканчики для взвешивания (бюксы) –20 шт. Эксикатор - по ГОСТ 23932 - 2 шт. Сита капроновые (хозяйственные) с диаметром отверстий 1 мм - 2 шт. Отбор проб. 1.Метод отбора проб почвы зависит от целей исследования. В целях контроля загрязнения почв металлами отбор проб почв следует производить в соответствии с: "Методическими рекомендациями по проведению полевых и лабораторных исследований почв и растений при контроле загрязнения окружающей среды металлами" - М.: Гидрометеоиздат, 1981. - С. 9-33; "Временными методическими рекомендациями по контролю загрязнения почв" - М.: Гидрометеоиздат, 1983. - С. 82-84. 2.При отборе проб почвы должна быть определена протяженность и топография зон загрязнения, которая зависит от розы ветров по сезонам года, скорости и продолжительности ветров, периода выпадения осадков.
3. Участки для отбора проб почвы должны хорошо отражать структуру района исследования: почвенного покрова, материнской породы, рельефа, геологии и гидрологии.
4.Объединенные пробы почвы, отобранные с участков должны быть представительными. Площадки для отбора проб почвы должны быть размером 100×100 м или 100×200 м, и объединенные пробы почвы должны составляться из единичных проб почвы, отобранных по методу конверта (четыре точки в углах площадки и одна в центре). Вокруг каждой из пяти точек делается еще по четыре прикопки.
5.Пробы почвы на целине необходимо отбирать на глубину 0-5 см, на пашне - 0-20 см (или на глубину пахотного горизонта).
6. Необходимым условием при отборе проб почвы является предохранение их от вторичных загрязнений на всех этапах подготовки.
7. Инструменты для отбора проб почвы должны быть из прочной пластмассы. Можно применять инвентарь из любой стали, предварительно тщательно очистив его от ржавчины. Слой почвы, который соприкасается с металлами, следует удалить острым ножом из пластмассы.
8. При отборе проб почвы не следует использовать оцинкованные ведра, медные изделия, эмалированные тазы, окрашенные инструменты.
9. Отобранные пробы почвы необходимо зарегистрировать в журнале и пронумеровать, заполнив сопроводительный талон по ГОСТ 17.4.4.02, приложение 3.
10. В качестве упаковочного материала для транспортировки и хранения отобранных проб почвы можно применять мешочки из хлопчатобумажной плотной ткани. На мешочке должны быть шнуры для завязки и пришитая полоска ткани, на которой пишут те же сведения, что и на сопроводительном талоне.
11. При дальнейшей обработке, транспортировке и хранении пробы почвы не должны подвергаться воздействию атмосферных осадков и других источников вторичного загрязнения.
Подготовка к анализу. Подготовка проб почвы и раствора к анализу.
1. Из воздушно-сухой объединенной пробы почвы, поступившей в лабораторию, тщательно удалить корки, другие инородные частицы и взять методом квартования пробу почвы массой 0,2 кг.
2. Отобранную пробу почвы следует перетереть в большой фарфоровой ступке и просеять через капроновое сито с диаметром отверстий 1 мм. Непросеянные комочки почвы растереть и снова просеять. Из полученной пробы почвы следует взять навески на анализ.
3. Для приготовления раствора одномолярной азотной кислоты в коническую термостойкую колбу вместимостью 1000 мл цилиндром вместимостью 1000 мл отобрать 938 мл бидистиллированной воды. Цилиндром вместимостью 100 мл следует отобрать 62 мл азотной кислоты (удельный вес 1,42 г/мл) и ввести ее в бидистиллированную воду, осторожно помешивая раствор стеклянной палочкой. Полученный раствор следует охладить до комнатной температуры. Приготовление раствора необходимо проводить в вытяжном шкафу. Требования к использованной посуде.
1. Для проведения анализа следует применять исключительно стеклянную или пластмассовую (полиэтиленовую, полипропилленовую или тефлоновую) посуду.
2. Посуду, используемую для анализов и хранения растворов необходимо промыть моющим веществом (сода, стиральный порошок), промыть водопроводной водой, вымочить в течение 24 ч в разбавленной азотной кислоте (кислота: вода = 1:5), тщательно промыть водопроводной водой и ополоснуть дистиллированной водой.
3. Определение гигроскопической воды в пробах почвы.
а) С целью пересчета воздушно-сухой пробы почвы на абсолютно-сухую следует провести определение гигроскопической воды в пробах почвы.
б) Массу абсолютно-сухой пробы почвы следует рассчитывать по формуле: где ΔРсух. - масса абсолютно-сухой пробы почвы, г; ΔРвозд.-сух. - масса воздушно-сухой пробы почвы, г; К - коэффициент пересчета.
в) Дня определения массы воздушно-сухой пробы почвы в сухие стаканчики (бюксы) с притертыми крышками следует взять не менее трех навесок воздушно-сухой почвы на аналитических весах (около 1,00 г с точностью 0,01 г). Сначала необходимо взвесить пустую бюксу и записать ее массу (Ро), затем взвесить эту же бюксу с навеской пробы почвы и записать ее массу (Рвозд.-сух.). Массу воздушно-сухой пробы почвы (ΔРвозд.-сух.) рассчитать по формуле ΔРвозд.-сух. = Рвозд.-сух. - Ро г) Коэффициент (К) необходимо рассчитать по формуле где q - содержание гигроскопической воды в пробах почвы, %.
д) Для определения содержания гигроскопической воды в пробах почвы, бюксы с воздушно-сухими пробами почвы необходимо поставить открытыми в сушильный шкаф с температурой от 105 до 115 °С. После трехчасового нагревания бюксы закрыть крышками к перенести в эксикатор, наполненный ангидроном или безводным хлористым кальцием и после остывания (через 20 мин) взвесить нa аналитических весах. После взвешивания пробы почвы следует снова нагреть в течение 2 часов, затем охладить в эксикаторе и снова взвесить. После первой и второй сушки допустимое расхождение в массе не должно превышать 0,003-0,005 г, В противном случае высушивание следует снова повторить. Содержание гигроскопической воды (q) в пробе почвы следует рассчитать по формуле где ΔРсух. - масса абсолютно-сухой пробы почвы г; ΔРсух. следует рассчитать по формуле: ΔРсух. = Рсух. - Ро,
где Рсух. - масса бюксы с абсолютно-сухой пробой почвы, г; Ро - масса пустой бюксы, г. е) Результаты измерений при определении гигроскопической воды в пробах почвы представлять по формуле в соответствии с таблицей Проведение анализа. 1. Извлечение водорастворимых форм соединений металлов из проб почв. 1. В бюксу вместимостью 30 мл на аналитических весах необходимо отобрать навеску воздушно-сухой пробы почвы (массой около 5,00 г с точностью до 0,01 г), одновременно определив содержание гигроскопической вода (q) для пересчета навески на абсолютно-сухую пробу почвы по п. 4.3.
2. Мерным цилиндром вместимостью 250 мл отобрать 125 мл дистиллированной воды и перелить ее в коническую колбу вместимостью 250 мл. Наполнить таким образом дистиллированной водой количество колб, кратное количеству взятых навесок проб почвы. Колбы с водой поставить напротив навесок с пробами почвы так, чтобы для каждой навески была своя колба с дистиллированной водой.
3. Прилить к пробе почвы из колбы (от объема 125 мл) небольшое количество дистиллированной воды (около 20 мл) и перемешать почву с водой, встряхивая вращательными движениями бюксу.
4. Полученную суспензию почвы с водой сразу же перевести на воронку с фильтром "белая лента". Добавляя дистиллированную воду в бюксу, ополаскивать ее и таким образом переводить остатки почвы на фильтр. В процессе фильтрования постепенно добавлять в фильтруемую пробу почвы дистиллированную воду из конической колбы. Следить, чтобы процесс фильтрования был равномерным. Фильтрат собрать в чистой конической колбе вместимостью 250 мл.
5. После того, как все 125 мл дистиллированной воды будут израсходованы на фильтрование пробы почвы, фильтр с пробой почвы убрать, а коническую колбу с фильтратом и воронкой поставить на включенную в сеть электроплитку и выпарить фильтрат до объема около 25 мл.
6. Снять колбу с воронкой с электроплитки и оставить остывать до комнатной температуры.
7. После остывания воронку снять, ополоснув ее из промывалки так, чтобы промывная вода попала в колбу.
8. Перевести из колбы упаренный фильтрат в мерную пробирку вместимостью 25 мл. Ополоснуть колбу 2-3 раза дистиллированной водой, переводя таким образом раствор в пробирку. Добавить 2-3 капли концентрированной азотной кислоты и довести объем раствора в пробирке до метки дистиллированной водой.
9. В полученном растворе определить водорастворимые формы соединений металлов атомно-абсорбционным анализом. Подготовка средств измерений к работе. Пример построения калибровочного графика
Выполнение измерений. Метод сравнения.
Дано: Концентрация раствора сравнения. С1 = 8 мкг/мл А1 = 29 мм Ах = 72 мм Определить: Сх -? Решение:


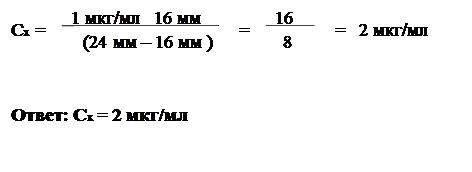
Ответ: Cх = 19,86 мкг/мл Метод добавок. Дано: Концентрация добавки Сдоб = 1 мкг/мл Адоб = 24 мм Определить: Ах = 16 мм Сх -?
КУРСОВАЯ РАБОТА по дисциплине
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА НИКЕЛЯ Выполнила Студент гр.320601 Елисеева А.И.
Проверила кан. хим. наук Пастушенко В.Г Содержание
|
||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 639; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.12.161.29 (0.014 с.) |



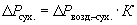
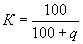 ,
,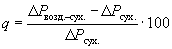
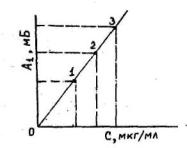 1, 2, 3 - точки, для построения калибровочной прямой
1, 2, 3 - точки, для построения калибровочной прямой