

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Инактивация аденилатциклазы и протеинкиназы А
Содержание книги
- Адреналин, химическая природа, биосинтез, роль в регуляции метаболизма.
- Кальций-фосфолипидный механизм
- Регуляция синтеза и секреции. Активируют: тиреолиберин, охлаждение (закаливание, обливание холодной водой); также
- Кортикостероиды, химическая природа, влияние на обмен веществ, регуляция биосинтеза.
- Противовоспалительное и иммунодепрессивное действие
- Биохимические нарушения при сахарном диабете. Механизмы развития диабетической комы.
- Гормональная регуляция обмена воды и электролитов. Механизм действия вазопрессина и альдостерона.
- Роль гормонов в регуляции фосфорно-кальциевого обмена. Причины гипо- и гиперкальциемии.
- Строение двух форм витамина D
- Половые гормоны, химическая природа, регуляция биосинтеза, влияние на обмен веществ.
- Регуляция синтеза и секреции
- Регуляция синтеза и секреции. Активируют: синтез эстрогенов – лютеинизирующий и фолликулостимулирующий гормоны
- Коллаген, особенности состава, строения и биосинтеза. Нарушения при дефиците витамина С.
- Гидроксилирование пролина и лизина. Роль витамина С
- Б. Особенности структуры и функции разных типов коллагенов
- Коллагены, образующие сетеподобные структуры
- Коллагены, образующие микрофибриллы
- Особенности обмена коллагена
- Значение десмозина и лизиннорлейцина
- А. Строение и классы гликозаминогликанов
- Б. Синтез и разрушение гликозаминогликанов
- В. Строение и виды протеогликанов
- Протеогликаны базальных мембран
- V. структурная организация межклеточного матрикса
- Нидоген формирует с ламинином нековален-тно связанный комплекс. Кроме этого, нидоген имеет центр связывания коллагена IV типа и,
- Тема 12. 2. Обезвреживание продуктов катаболизма аминокислот в кишечнике
- Тема 12. 3. Биотрансформация лекарств
- Тема 12. 5. Химический канцерогенез
- Строение гемоглобина, биологическая роль. Формы гемоглобина. Гемоглобинопатии.
- Что «показывает» уровень билирубина?
- Результаты/Норма/Расшифровка анализа
- Биосинтез гема и гемоглобина. Регуляция этих процессов. Нарушения синтеза гема. Порфирии.
- Обмен железа: всасывание, транспорт, депонирование, суточная потребность. Нарушения обмена.
- Транспорт кислорода и диоксида углерода кровью.
- Гиповитаминозы очень распространены
- Строение окисленных форм фад и фмн
- Строение пиридоксина и ео коферментных форм
- Витамин В12 и фолиевая кислота, их биологическое значение. Потребность, проявления авитаминоза
- Химическая природа витамина С. Биологическая роль. Потребность, проявления авитаминоза.
- Витамин А и его провитамины. Биологическая роль. Потребность, источники.
- Витамины Е и К. Химическая природа, биологическая роль. Потребность, источники, проявления гиповитаминоза.
- Химический состав и свойства мочи. Патологические компоненты мочи.
- Клинико диагностическое значение
- Клинико диагностическое значение. Выведение бикарбонатов с мочой в значительной мере коррелирует с величиной ее рн
- Механизм мышечного сокращения
- Молекулярные механизмы синаптической передачи нервного импульса. Нейромедиаторы.
- Мембраны, химический состав, свойства. Механизмы мембранного транспорта химических веществ.
- Инактивация аденилатциклазы и протеинкиназы А
- Последовательность событий передачи сигнала первичных мессенджеров с помощью инозитолфосфатной системы
- Последовательность событий, приводящих к изменению скорости транскрипции
α,,-Субъединица в комплексе с ГТФ при взаимодействии с аденилатциклазой начинает проявлять ферментативную (ГТФ-фосфатазную) активность, она гидролизует ГТФ. Образующаяся молекула ГДФ остается в активном центре α,,-субъединицы, изменяет ее конформацию и уменьшает сродство к АЦ. Комплекс АЦ и α,,-ГДФ диссоциирует, α,,-ГДФ включается в G..-белок. Отделение α,,-ГДФ от аденилатциклазы инактивирует фермент и синтез цАМФ прекращается.
Фосфодиэстераза - «заякоренный» фермент цитоплазматической мембраны гидролизует образовавшиеся ранее молекулы цАМФ до АМФ. Снижение концентрации цАМФ в клетке вызывает расщепление комплекса цАМФ4К"2 и повышает сродство R- и С-субъединиц, образуется неактивная форма ПКА.
Фосфорилированные ферменты и белки под действием фосфопротеинфосфатазы переходят в дефосфорилированную форму, изменяется их конформация, активность и скорость процессов, в которых участвуют эти ферменты. В результате система приходит в исходное состояние и готова вновь активироваться при взаимодействии гормона с рецептором. Таким образом, обеспечивается соответствие содержания гормона в крови и интенсивности ответа клеток-мишеней.
3. Участие аденилатциклазной системы в регуляции экспрессии генов. Многие белковые гормоны: глюкагон, вазопрессин, паратгормон и др., передающие свой сигнал посредством аденилатциклазной системы, могут не только вызвать изменение скорости реакций путем фосфорилирования уже имеющихся в клетке ферментов, но и увеличивать или уменьшать их количество, регулируя экспрессию генов (рис. 4.12). Активная протеинкиназа А может проходить в ядро и фосфорилировать фактор транскрипции (СRЕВ). Присоединение фосфорного
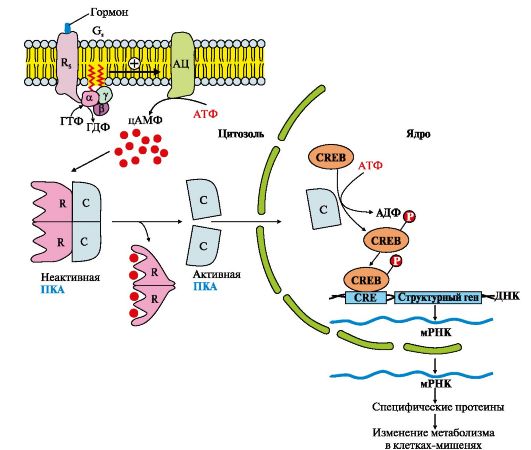 Рис. 4.12. Аденилатциклазный путь, приводящий к экспрессии специфических генов Рис. 4.12. Аденилатциклазный путь, приводящий к экспрессии специфических генов
остатка повышает сродство фактора транскрипции (СRЕВ-(Р) к специфиче-ской последовательности регуляторной зоны ДНК-СRЕ (цАМФ-response element) и стимулирует экспрессию генов определенных белков.
Синтезированные белки могут быть ферментами, увеличение количества которых повышает скорость реакций метаболических процессов, или мембранными переносчиками, обеспечивающими поступление или выход из клетки определенных ионов, воды или других веществ.
 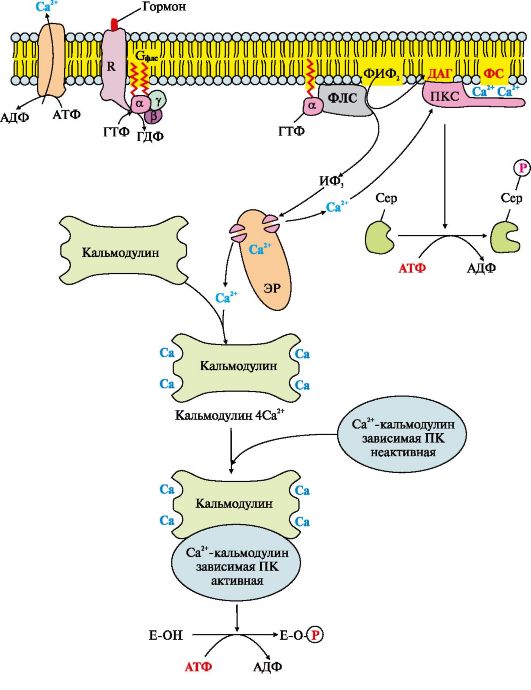 Рис. 4.13. Инозитолфосфатная система Рис. 4.13. Инозитолфосфатная система
Работу системы обеспечивают белки: кальмодулин, фермент протеинкиназа С, Са2+-кальмодулин-зависимые протеинкиназы, регулируемые Са2+-каналы мембраны эндоплазматического ретикулума, Са2+-АТФазы клеточной и митохондриальной мембран.
|