Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Б. Синтез и разрушение гликозаминогликанов
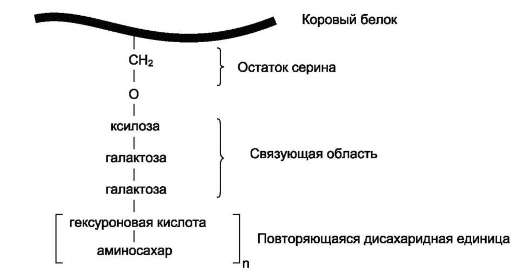
Метаболизм гликозаминогликанов зависит от соотношения скорости их синтеза и распада. Синтез гликозаминогликанов Полисахаридные цепи гликозаминогликанов практически всегда связаны с белком, который называется ко'ровым, или сердцевинным. Присоединение полисахарида к белку осуществляется через связующую область, в состав которой чаще всего входит трисахарид галактоза-галактоза-ксилоза (рис. 15-14). Олигосахариды связующей области присоединяются к кóровому белку ковалентными связями 3 типов: 1. О-гликозидной связью между серином и ксилозой; 2. О-гликозидной связью между серином или треонином и N-ацетилгалактозамином; 3. N-гликозиламиновой связью между амид-ным азотом аспарагина и N-ацетилглюко-замином. Полисахаридные цепи гликозаминоглика-нов синтезируются путём последовательного присоединения моносахаридов. Донорами моносахаридов обычно являются соответствующие нуклеотид-сахара. Реакции синтеза гликозамино-гликанов катализируют ферменты семейства трансфераз, обладающие абсолютной субстратной специфичностью. Эти трансферазы локализованы на мембранах аппарата Гольджи. Сюда по каналам ЭР поступает коровый белок, синтезированный на полирибосомах, к которому присоединяются моносахариды связующей области и затем наращивается вся полисахаридная цепь. Сульфатирование углеводной части происходит здесь с помощью сульфотрансферазы, донором сульфатной группы выступает ФАФС (см. раздел 12). Аминосахара синтезируются из глюкозы; в соединительной ткани ~20% глюкозы используется таким образом. Непосредственным предшественником N-ацетилглюкозамина, N-аце-тилгалактозамина и сиаловой кислоты является фруктозо-6-фосфат. Источником NH2-группы в этих сахарах служит глутамин. Аминосахар далее ацетилируется с помощью ацетил-КоА. Активированными формами этих аминосахаров служат их УДФ-производные (схема на след. стр., рис. 15-15). Источниками глюкуроновой кислоты в организме человека могут быть пища, внутриклеточное лизосомальное разрушение гликозами-ногликанов и синтез глюкуроновой кислоты. Активированная форма глюкуроновой кислоты
Рис. 15-14. Связующая область гликозаминогликанов.
(УДФ-глюкуронат) образуется при окислении УДФ-глюкозы (см. схему ниже). L-идуроновая кислота образуется после включения D-глюкуроновой кислоты в углеводную цепь в результате реакции эпимеризации. На синтез гликозаминогликанов влияют глю-кокортикоиды: они тормозят синтез гиалуроно-
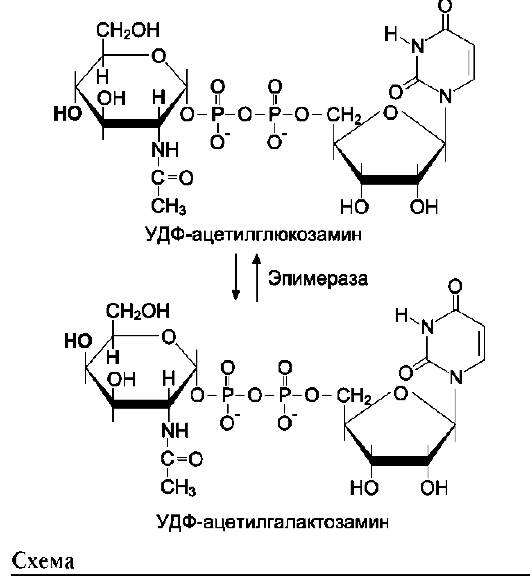
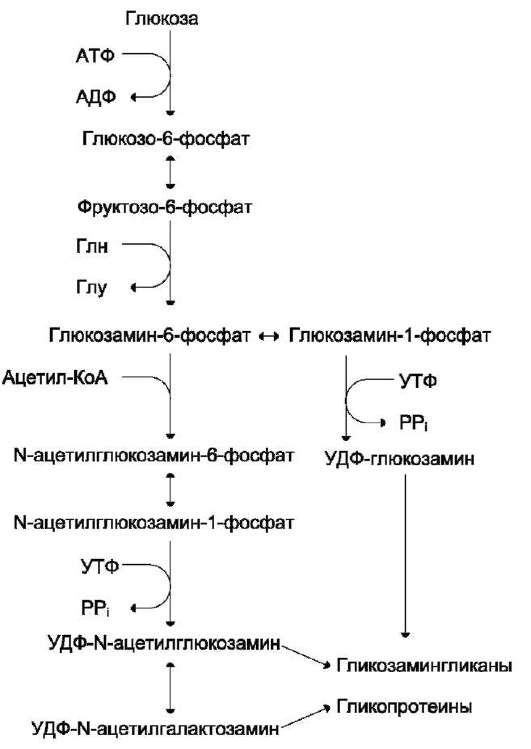
Рис. 15-15. Схема синтеза аминосахаров.
вой кислоты и сульфатированньгх гликозаминогликанов. Показано также тормозящее действие половых гормонов на синтез сульфатированных гликозаминогликанов в органах-мишенях.
|
|||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 117; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.118.198 (0.003 с.) |