

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Обмен железа: всасывание, транспорт, депонирование, суточная потребность. Нарушения обмена.
Содержание книги
- Адреналин, химическая природа, биосинтез, роль в регуляции метаболизма.
- Кальций-фосфолипидный механизм
- Регуляция синтеза и секреции. Активируют: тиреолиберин, охлаждение (закаливание, обливание холодной водой); также
- Кортикостероиды, химическая природа, влияние на обмен веществ, регуляция биосинтеза.
- Противовоспалительное и иммунодепрессивное действие
- Биохимические нарушения при сахарном диабете. Механизмы развития диабетической комы.
- Гормональная регуляция обмена воды и электролитов. Механизм действия вазопрессина и альдостерона.
- Роль гормонов в регуляции фосфорно-кальциевого обмена. Причины гипо- и гиперкальциемии.
- Строение двух форм витамина D
- Половые гормоны, химическая природа, регуляция биосинтеза, влияние на обмен веществ.
- Регуляция синтеза и секреции
- Регуляция синтеза и секреции. Активируют: синтез эстрогенов – лютеинизирующий и фолликулостимулирующий гормоны
- Коллаген, особенности состава, строения и биосинтеза. Нарушения при дефиците витамина С.
- Гидроксилирование пролина и лизина. Роль витамина С
- Б. Особенности структуры и функции разных типов коллагенов
- Коллагены, образующие сетеподобные структуры
- Коллагены, образующие микрофибриллы
- Особенности обмена коллагена
- Значение десмозина и лизиннорлейцина
- А. Строение и классы гликозаминогликанов
- Б. Синтез и разрушение гликозаминогликанов
- В. Строение и виды протеогликанов
- Протеогликаны базальных мембран
- V. структурная организация межклеточного матрикса
- Нидоген формирует с ламинином нековален-тно связанный комплекс. Кроме этого, нидоген имеет центр связывания коллагена IV типа и,
- Тема 12. 2. Обезвреживание продуктов катаболизма аминокислот в кишечнике
- Тема 12. 3. Биотрансформация лекарств
- Тема 12. 5. Химический канцерогенез
- Строение гемоглобина, биологическая роль. Формы гемоглобина. Гемоглобинопатии.
- Что «показывает» уровень билирубина?
- Результаты/Норма/Расшифровка анализа
- Биосинтез гема и гемоглобина. Регуляция этих процессов. Нарушения синтеза гема. Порфирии.
- Обмен железа: всасывание, транспорт, депонирование, суточная потребность. Нарушения обмена.
- Транспорт кислорода и диоксида углерода кровью.
- Гиповитаминозы очень распространены
- Строение окисленных форм фад и фмн
- Строение пиридоксина и ео коферментных форм
- Витамин В12 и фолиевая кислота, их биологическое значение. Потребность, проявления авитаминоза
- Химическая природа витамина С. Биологическая роль. Потребность, проявления авитаминоза.
- Витамин А и его провитамины. Биологическая роль. Потребность, источники.
- Витамины Е и К. Химическая природа, биологическая роль. Потребность, источники, проявления гиповитаминоза.
- Химический состав и свойства мочи. Патологические компоненты мочи.
- Клинико диагностическое значение
- Клинико диагностическое значение. Выведение бикарбонатов с мочой в значительной мере коррелирует с величиной ее рн
- Механизм мышечного сокращения
- Молекулярные механизмы синаптической передачи нервного импульса. Нейромедиаторы.
- Мембраны, химический состав, свойства. Механизмы мембранного транспорта химических веществ.
- Инактивация аденилатциклазы и протеинкиназы А
- Последовательность событий передачи сигнала первичных мессенджеров с помощью инозитолфосфатной системы
- Последовательность событий, приводящих к изменению скорости транскрипции
Железо входит в состав гемсодержащих белков, а также металлофлавопротеинов, железосерных белков, трансферрина, ферритина.
1. Источником железа при биосинтезе белков, содержащих железо, являются пищевые продукты. Обычно всасывается не более 10% железа пищи. Железо, освобождающееся при постоянном распаде эритроцитов в клетках печени и селезенки, может повторно использоваться для синтеза железосодержащих белков.
Кислая среда желудка и присутствие в пище аскорбиновой кислоты, восстанавливающей Fe 3+, способствуют освобождению железа из солей органических кислот пищи (рис. 13.3).
2. Поступление железа из энтероцитов в кровь зависит от скорости синтеза в них белка апоферритина. Апоферритин улавливает железо в клетках слизистой кишечника и превращается в ферритин, который остается
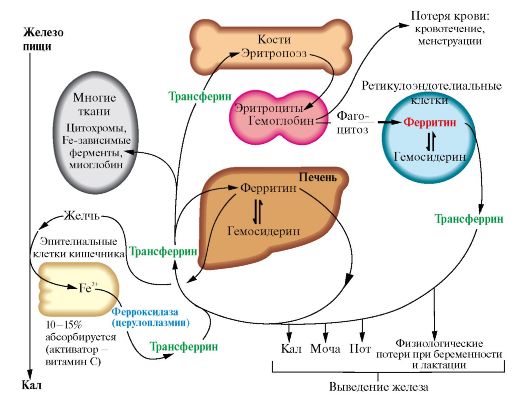 Рис. 13.3. Обмен железа. Рис. 13.3. Обмен железа.
• Железо поступает с пищей, транспортируется кровью в форме трансферрина, запасается в виде ферритина и используется для синтеза цитохромов, железосодержащих ферментов, гемоглобина и миоглобина.
• Организм теряет железо с мочой, калом, потом и при кровотечениях.
• Гемосидерин аккумулирует избыток железа
в энтероцитах. Это снижает поступление железа в кровь из клеток кишечника. Когда потребности в железе невелики, скорость синтеза апоферритина повышается. Слущивание клеток слизистой оболочки кишечника освобождает организм от излишков железа. При недостатке железа в организме апоферритин в энтероцитах почти не синтезируется.
Фермент крови ферроксидаза (церулоплазмин) окисляет железо, оно связывается с гликопротеином крови трансферрином и транспортируется кровью (рис. 13.4).
3. Трансферрин взаимодействует со специфическими рецепторами и поступает в клетки. Количество рецепторов трансферрина зависит от содержания железа в клетках и регулируется на уровне транскрипции гена белкарецептора. При снижении содержания железа в клетках скорость синтеза рецепторов повышается, и наоборот.
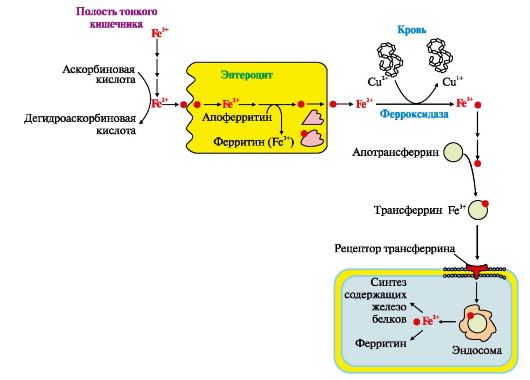 Рис. 13.4. Поступление экзогенного железа в ткани. Рис. 13.4. Поступление экзогенного железа в ткани.
В полости кишечника Fe3+ высвобождается из белков и солей органических кислот пищи. Усвоение Fe3+ улучшает аскорбиновая кислота, восстанавливающая его до Fe+2. Поступление Fe2+ из слизистой оболочки кишечника в кровь сопровождается окислением железа медьсодержащим ферментом плазмы крови ферроксидазой. Избыток поступившего в клетки слизистой оболочки кишечника железа соединяется с белком апоферритином, который окисляет железо и превращается в ферритин. В крови Fe3+ транспортирует белок плазмы крови трансферрин. В тканях Fe2+ используется для синтеза железосодержащих белков или депонируется в составе ферритина.
4. Белок ферритин играет роль депо железа в клетках печени, селезенки, костного мозга. Избыток железа аккумулируется в печени и других тканях в составе гранул гемосидерина. Если количество железа в клетках превышает объем ферритинового депо, то оно откладывается в белковой части молекулы ферритина. Таким образом ферритин превращается в гемосидерин, который плохо растворим в воде и может содержать до 37% железа. Накопление гранул гемосидерина в ретикулоэндотелиоцитах печени и селезенки может привести к повреждению органа - гемохроматозу.
При недостаточном поступлении или нарушении утилизации железа развивается железодефицитная анемия.
|