
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кількісне визначення сульфат-іонівСодержание книги
Поиск на нашем сайте
Кількісно сульфат-іони визначають комплексонометричним методом за допомогою трилону Б. Сутність методу полягає в тому, що до проби води додають надлишок іонів Методика кількісного визначення сульфат-іонів [2] Дослід 1. У конічну колбу місткістю 200–250 мл піпеткою набирають 50 мл проби води, циліндром додають 5 мл амонійного буферного розчину (для створення і підтримки рН ~ 10), додають шпателем 10–15мг сухої суміші кристалів індикатора хромогену чорного з Дослід 2 (холостий дослід). У конічну колбу на 200–250 мл піпеткою набирають 50 мл дистильованої води і піпеткою додають 1 мл стандартного розчину Дослід 3. У конічну колбу на 200–250 мл піпеткою набирають 50 мл досліджуваної води, додають 2–3 краплі розчину індикатора метилового червоного (рТ = 5,5) і підкисляють пробу води 0,1 М розчином хлоридної кислоти до появи червоного забарвлення. Колбу встановлюють на газовий пальник и кип’ятять 3–5 хв. від початку закипання. При цьому спостерігають, щоб протягом усього процесу кип’ятіння колір розчину залишався червоним. Якщо він стане блідим або жовтим, потрібно додати ще декілька краплин 0,1 М розчину
Після кип’ятіння до розчину додають 1 мл стандартного розчину Вміст сульфат–іонів (Х) розраховують за формулою де С – молярна концентрація еквівалента трилону Б
(дослід 1), мл;
(дослід 2), мл;
Лабораторна робота № 10
|
||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 193; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.169 (0.009 с.) |

 – стандартний розчин
– стандартний розчин 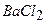 і
і 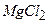 (10 г
(10 г 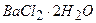 і 4 г
і 4 г 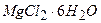 в 1 л води). Частина іонів барію зв’язує сульфат-іони в нерозчинний осад
в 1 л води). Частина іонів барію зв’язує сульфат-іони в нерозчинний осад 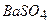 . Іони
. Іони 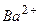 , що залишилися в розчині, відтитровують стандартним розчином трилону Б, з яким іони барію утворюють комплексні сполуки. Вміст сульфат-іонів розраховують за різницею витрат трилону Б, який іде на зв’язування іонів барію до і після осаджування сульфат-іонів. Оскільки досліджувана вода завжди містить іони
, що залишилися в розчині, відтитровують стандартним розчином трилону Б, з яким іони барію утворюють комплексні сполуки. Вміст сульфат-іонів розраховують за різницею витрат трилону Б, який іде на зв’язування іонів барію до і після осаджування сульфат-іонів. Оскільки досліджувана вода завжди містить іони 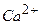 і
і  , які також утворюють комплексні сполуки з трилоном Б, то на присутність цих іонів потрібно ввести відповідні поправки.
, які також утворюють комплексні сполуки з трилоном Б, то на присутність цих іонів потрібно ввести відповідні поправки. . Отриманий розчин титрують 0,05 н. розчином трилону Б
. Отриманий розчин титрують 0,05 н. розчином трилону Б  від вишнево-червоного до синього забарвлення і занотовують до журналу об’єм трилону Б (
від вишнево-червоного до синього забарвлення і занотовують до журналу об’єм трилону Б (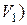 , витрачений на титрування проби води. Таким чином, визначають загальний вміст іонів
, витрачений на титрування проби води. Таким чином, визначають загальний вміст іонів 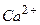 і
і 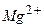 у воді (загальна твердість води).
у воді (загальна твердість води).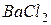 , що містить іони магнію. Іони магнію потрібні для більш точного встановлення точки еквівалентності. Далі циліндром додають 5 мл амонійного буферного розчину і 10–15 мг індикатора хромогену чорного з
, що містить іони магнію. Іони магнію потрібні для більш точного встановлення точки еквівалентності. Далі циліндром додають 5 мл амонійного буферного розчину і 10–15 мг індикатора хромогену чорного з 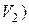 , витрачений на титрування холостої проби води.
, витрачений на титрування холостої проби води.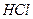 . Присутність
. Присутність 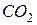 , який утворюється в результаті реакцій:
, який утворюється в результаті реакцій: 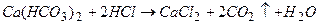 ,
, .
.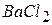 , що містить іони магнію, і кип’ятять ще 10–15 сек. для більш повного осадження іонів
, що містить іони магнію, і кип’ятять ще 10–15 сек. для більш повного осадження іонів 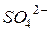 іонами
іонами 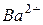 . Далі пробу води охолоджують 10–15 хв. і нейтралізують 0,1 М розчином
. Далі пробу води охолоджують 10–15 хв. і нейтралізують 0,1 М розчином 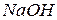 до появи жовтого забарвлення. Потім до проби води циліндром додають 5 мл амонійного буферного розчину і 10–15 мг індикатора хромогену чорного з
до появи жовтого забарвлення. Потім до проби води циліндром додають 5 мл амонійного буферного розчину і 10–15 мг індикатора хромогену чорного з 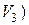 , витрачений на титрування проби води.
, витрачений на титрування проби води. мг/л,
мг/л,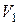 – об’єм трилону Б, який пішов на титрування іонів
– об’єм трилону Б, який пішов на титрування іонів 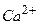 і
і  – об’єм трилону Б, який пішов на титрування іонів
– об’єм трилону Б, який пішов на титрування іонів 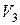 – об’єм трилону Б, який пішов на титрування іонів
– об’єм трилону Б, який пішов на титрування іонів 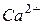 ,
, 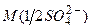 – молярна маса еквівалента іонів
– молярна маса еквівалента іонів 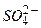 , що дорівнює 48 г/моль;
, що дорівнює 48 г/моль; – об’єм проби води, мл.
– об’єм проби води, мл.


